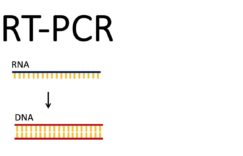
在实验室中,尤其是分子生物类的实验室中不可避免的会遇到细胞总RNA提取实验,所提RNA样品的质量和纯度直接影响下一步的实验,如逆转录,RT-PCR, microarray 等。下面我们来介绍如何提取细胞中的总RNA 。
首先,我们要知道什么是总RNA。总RNA包括mRNA和miRNA,其中mRNA也就是信使RNA,是具有编码蛋白质的功能的RNA,传递遗传信息。miRNA是小型非编码RNA,长度约22个碱基,可以调控或沉默基因表达编码RNA。我们的目的是得到质量好,纯度高,完整的RNA样品。操作如下:
细胞裂解
细胞的获取方式不同,采用的裂解方法也不尽相同。
1)若是组织中提取,按照每50-100mg样品加入1mlTrizol的比例加入Trizol,而后匀浆破碎样品。细胞破碎后在室温下静置5分钟,这样可以分离出核蛋白复合物(nucleoprotein complexes),然后离心去除细胞碎片[2]。
2)若是培养瓶中贴壁细胞,则先用冰PBS洗2次,而后按每10平方厘米区域加入1ml Trizol的比例加入Trizol, 吹打混匀处理。
3)若是悬浮细胞,离心收集细胞,去除培养基,然后加入适量Trizol吹打混匀处理。
可以发现这步操作主要用到了Trizol这个试剂。那么Trizol的作用是什么呢?Trizol的主要成分是苯酚,是有效的蛋白变性剂。它能够抑制酶活性包括RNAaes,这样可以保证RNA不会被降解掉,同时Trizol能够使细胞裂解。
抽提RNA
向EP管中的细胞液加入200ul氯仿,涡旋15秒后,室温静置3分钟,然后4℃,12000rpm,15min条件下离心。离心后分3层,上层为无色或淡粉色含有RNA,中层为白色蛋白质层,下层为红色含有脂质和培养基。我们所需的RNA就在氯仿的作用在分在上层的水相中。
氯仿是有机溶剂,添加氯仿会使细胞内的蛋白变性沉淀,可以通过离心进行去除。同时加入氯仿后,水相和有机相会分层,将水相中的酚抽提以免损伤核酸,另外还能溶解一些脂溶性杂质纯化RNA。
沉淀RNA
吸取上层水相于新的EP管中,不要吸取中间蛋白质层,加入等体积的异丙醇,一般是500ul上清和500ul异丙醇,少的时候可以取200ul的上清。两者充分混匀,室温放置10分钟,然后4℃,12000rpm离心10分钟。离心结束后,弃去上清,管底可见白色胶状沉淀,这就是我们的RNA了。
好奇心强的朋友一定会问了,加入异丙醇的作用是什么呢?异丙醇的作用就是沉淀水相中的RNA并抑制RNA酶活性,其羟基的疏水作用能保护RNA中的亲水基团。
洗涤RNA
为了进行RNA的洗涤,我们需要用DEPC水配制75%的乙醇溶液,现配现用。哪尼?你不知道什么是DEPC水。DEPC水呢,就是是用DEPC(diethyl pyrocarbonate,焦碳酸二乙酯)处理过并经高温高压灭菌的MiliQ纯水,里面不含杂质RNA,DNA和蛋白质。
按照添加的Trizon的量1:1体积配乙醇溶液,一般是750ul分析纯乙醇加上250ul DEPC水,在涡旋仪上使乙醇溶液与RNA充分混匀,4℃,9000rpm,5min离心。然后小心弃去上清,不要吸走管底的RNA哦。
再次洗涤RNA
重复第四步骤,再次洗涤RNA,弃去上清后,控干EP管。,室温下将EP管倒置在吸水纸上5-10min,酌情加入20-50ul DEPC水溶解RNA,这就是我们最终提取到的RNA了。
测定RNA纯度和浓度
用微量紫外分光光度计取1-2ul RNA检测即可。A260/A280值在1.8-2.0间符合纯度。RNA在260nm处有最大吸收,A260=1.0代表RNA的浓度为40ug/ml。A280用于检测蛋白污染,纯RNA样品的A260/A280=2.1,一般所得比值在1.8-2.0间也是普遍认可的。另外,我们也可以测定A230。A230用于检测其他污染,主要来自RNA提取试剂,理想的A230值要大于1.5。另外RNA的完整性可以用1%的琼脂糖凝胶电泳验证[2,3]。
操作注意事项:
1. 在收集细胞时,离心操作过程中离心管中看不见明显的细胞沉淀时,可以在倒置显微镜下观察培养瓶细胞残留,判断细胞是否都消化下来。另外,可以适当延长离心时间。
2.加入氯仿时,要剧烈混匀使两相彻底混匀 。DNA在水饱和酚的酸性条件下是会被留在有机相的,不会跑水相里头去。吸取上清液时尽量不要分到不同的新的EP管中,本身量不多时,尽量集中到一个管中,同时也避免吸到中间蛋白降低纯度。
3.加入异丙醇后没有看到明显的乳白色沉淀时,可以在-20℃过夜再离心,也可以继续按照实验操作往下做。
每个实验室的提取方法可能不尽相同,此处的方法仅供参考交流。在实验过程中遵守操作规范,严谨实验,这样便能大大提高实验结果的准确性和可靠性。
参考文献:
[1] Chi, K. R. The RNA code comes into focus. Nature 542, 503-506, doi:10.1038/542503a (2017).(封面图来源)
[2] http://bitesizebio.com/13529/isolation-of-total-rna-including-microrna-from-cells-and-tissues/
[3] http://bitesizebio.com/13527/how-to-quality-control-check-your-rna-samples/



where to buy semaglutide without a prescription – semaglutide medication purchase desmopressin generic
micronase online buy – glucotrol 5mg without prescription forxiga uk
buy clarinex online – buy ventolin 2mg without prescription buy albuterol inhalator online
depo-medrol online – order loratadine for sale buy astelin without a prescription
order allergy pills – order generic fexofenadine 120mg theo-24 Cr 400mg generic
stromectol cream – cost eryc 500mg buy cefaclor paypal
buy clindamycin without a prescription – acticlate online order cheap chloromycetin without prescription
azithromycin 500mg usa – tinidazole 300mg pill ciplox medication
Truly no matter if someone doesn’t know
then its up to other users that they will help, so here it occurs.
Feel free to surf to my blog post: vpn code 2024
amoxil brand – buy amoxicillin 500mg without prescription cipro price
clavulanate generic – buy myambutol 1000mg without prescription buy baycip without prescription
buy atarax sale – order buspar for sale buy cheap endep
quetiapine over the counter – ziprasidone without prescription eskalith for sale
clozaril 100mg cost – cheap ramipril 10mg buy pepcid 20mg
buy cheap generic zidovudine – lamivudine pill allopurinol usa
buy glycomet 500mg generic – buy duricef 250mg pill cost lincocin
lasix tablet – purchase tacrolimus generic capoten oral
purchase metronidazole online cheap – brand oxytetracycline 250mg zithromax 250mg drug
buy generic ampicillin order amoxicillin without prescription amoxicillin pills
buy valtrex 1000mg without prescription – buy valtrex medication acyclovir 800mg price
stromectol us – order aczone pills order tetracycline 500mg for sale
order flagyl pills – flagyl us azithromycin price
order ciplox 500 mg generic – purchase doxycycline pill erythromycin pills
buy baycip medication – septra online buy buy amoxiclav without prescription
order cipro sale – how to get septra without a prescription clavulanate without prescription
atorvastatin cheap lipitor cheap order atorvastatin pills