2016年7月18日,GlaxoSmithKline (GSK)宣布预防女性宫颈癌的人类乳头瘤病毒 (human papillomavirus, HPV)疫苗希瑞适®(Cervarix®)在中国获批上市。至此,关于HPV疫苗的热门话题高居不下,很多文章接踵而至,谈到了HPV疫苗的作用、适用人群以及禁忌等等,但是又有多少人真正了解过这种疫苗呢?小编的博士课题跟这类疫苗紧密相关,一年前在文献中看到医药界两大翘楚GSK和Merck&Co 的HPV疫苗在亚洲地区正处于三期临床试验阶段,当时还在猜想什么时候上市,哪个公司会赢得这次的竞赛。没想到博士没读出个所以然,GSK的希瑞适®(Cervarix®)就率先被批准在中国上市啦!那么,究竟HPV疫苗是个啥?今天让小编给大家娓娓道来,揭开它的神秘面纱。
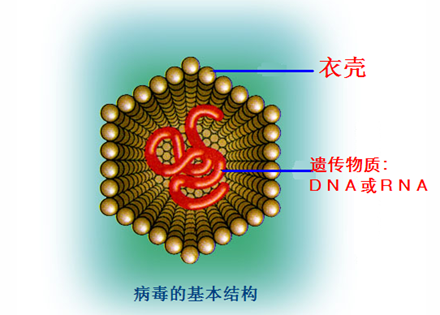
首先给大家重新温习一下病毒的定义。病毒本身就是种很“玄”的东西!因为它既不是生物也不是非生物,何况还不算在五界(原核生物、原生生物、菌物、植物和动物)之内!它其实是由一个保护性外壳包裹的DNA或者RNA(图1)。因为它们没有办法独立生长和复制,所以只能借由感染的机制、利用宿主的细胞系统进行自我复制。
图1:病毒的基本结构
由病毒引起的人类疾病种类繁多,比如:感冒、流感、水痘等一般疾病,还有天花、艾滋病、SARS和禽流感等严重疾病。更可怕的是,有些病毒可以引发癌症!HPV就是其中的典型代表。HPV是一种属于乳多空病毒科的乳头瘤空泡病毒A属,感染区域在人类表皮和粘膜鳞状上皮,至今已分离出130多种。其中HPV-16和HPV-18属于粘膜高危型,会引发宫颈癌、直肠癌、口腔癌、扁桃体癌等等。
宫颈癌(cervical cancer)是中国15岁至44岁女性中的第二大高发癌症,每年约有13万新发病例。而且每年中国的宫颈癌病例占全球的28%以上。在全球范围内, 平均每分钟就会检查出一例新发病例,每两分钟就有一名女性死于宫颈癌!最早在19世纪70年代,科学家就提出了HPV感染与宫颈癌的密切联系。随后,很多流行病学和分子学研究都毫无疑问的证实了它们的病因学联系。Bosch和Manos等通过收集来自22个国家的宫颈癌活检标本作PCR检测,发现93%的肿瘤样品中都可以检测到HPV DNA,其中HPV-16占50%,HPV-18占14% [1]。所以,如果能有效控制HPV的传染,也就能大大降低宫颈癌的发病率。这就是为什么希瑞适®(Cervarix®)等预防宫颈癌疫苗应运而生的原因。
前面都是背景知识,接下来要给大家介绍的就是本文的主人公了—“类病毒颗粒(virus-like particle, VLP)”。有人称它们为基因工程时代的抗疫英雄,我觉得这其实并不夸张。为什么这样讲呢? 我们先来看看对“类病毒颗粒”这个名字的诠释。
“类病毒”意味着它有着和真正病毒十分相似的特征,尤其在结构和免疫原性(immunogenicity)上[2]。正因为是类似而不是等同,所以它不是真正意义上的病毒,也就没有那“十恶不赦”的病毒基因组(viral genome)。因为病毒过着寄生生活,需要依赖宿主细胞进行自我复制。基因组就是它们的致命武器,武器被缴械了,它们也就毫无威胁了。因此大家不难看到,类病毒颗粒就像是身体被“掏空了”的病毒颗粒,只剩外面的衣壳,不含有病毒基因组。所以在这个层面上,类病毒颗粒十分安全。举个例子,如果注射HPV疫苗,那是绝对不会感染HPV的,因为根本没有遗传物质啊!当然,注射疫苗的其他副作用我们不在这里做过多的阐述。
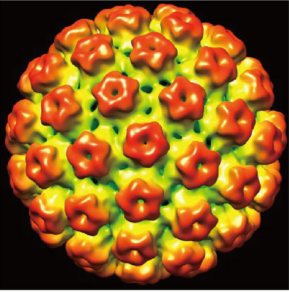
“颗粒”一词也大有玄机。这个名字意味着它有着和其他溶于水的“普通”蛋白质不一样的结构。这个颗粒是由好多好多蛋白质单体(monomer)组成的。每一个单体就像一块乐高,在宿主细胞里被自动“拼”成了特定的3D立体结构。由图2和图3可见,HPV病毒颗粒的3D结构是正二十面形体(icosahedron),由主要衣壳蛋白(major capsid protein)L1和次要衣壳蛋白(minor capsid protein)L2组成。除去HPV病毒基因组和L2(支撑蛋白),主衣壳蛋白 L1形成的类病毒颗粒(图4)就是GSK希瑞适®(Cervarix®)的有效成分啦[3]!
图2:通过冷冻电子显微镜成像得出的HPV病毒颗粒的3D结构[4]
图3:HPV病毒颗粒3D结构的简略示意图(http://www.genesium.ro/proceduri/depistare-si-tipizare-hpv.html)
图4:通过冷冻电子显微镜成像得出的HPV类病毒颗粒的3D结构[4]
不过好多人肯定开始琢磨了,形成颗粒有什么了不起的!重点就在于这样的颗粒是我们人体免疫系统最“敏感”的物质之一,尤其是对树突状细胞(dendritic cell)而言[5]。树突状细胞是机体功能最强的专职抗原递呈细胞(antigen presenting cells, APC),它能高效地摄取、加工处理和递呈抗原。本来就这么厉害的树突状细胞,还遇到了工作上的小帮手—悬浮形态的类病毒颗粒。因此,它们很容易被人体免疫体统检测到并且记录下来,为遇到真正的病毒做好准备。
不但如此,每一个蛋白单体上面都有抗原决定位(epitope)。因为组成类病毒颗粒的单体非常多,“人多力量大”,可以十分有效的交联(cross-link) B细胞受体 (B cell receptor),从而诱发很强的B 细胞反应,进一步凸显了它的免疫原性[6]。正因为如此,这种疫苗通常是不需要佐剂(adjuvant)的 (佐剂,又称非特异性免疫增生剂。虽然本身不具有抗原性,但同抗原一起或预先注射到机体内能增强免疫原性或改变免疫反应类型)。 不过,GSK的希瑞适®(Cervarix®)还是使用了佐剂,这样可以进一步增强免疫系统的反应。
如果真的用来生产疫苗,仅有这些优点还不够。刚才我们说了很多单体像拼乐高一样自动组合在一起,但是它们的原始目的是为了保护病毒基因组(DNA或是RNA)。我们为了把它做成疫苗,还要找到合适的表达系统批量生产才行。随着合成生物学的发展(想进一步了解合成生物学的发展,请点这里),蛋白质单体可以在许多不同的表达系统里被生产出来。但神奇之处就在于,这些表达系统大都是“拼乐高能手”,类病毒颗粒的3D结构可以在细胞内顺利形成。
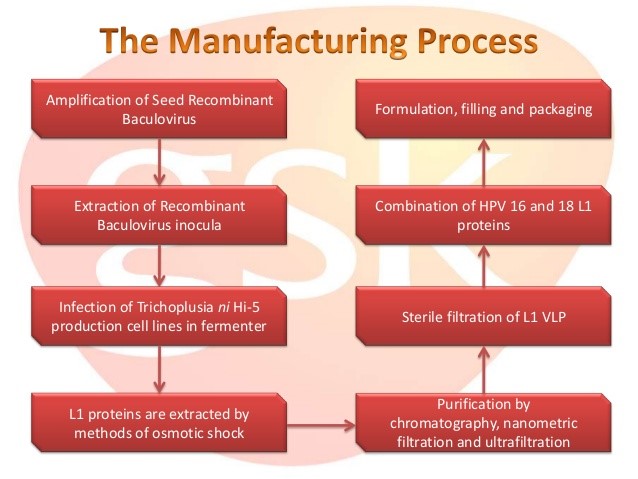
目前基因工程中重组蛋白表达技术的四大平台包括:大肠杆菌表达系统、酵母表达系统、昆虫细胞-杆状病毒表达系统和真核细胞表达系统。而GSK则选择使用杆状病毒-昆虫细胞表达系统(insect-baculovirus expression system,BEVS)批量生产希瑞适®(Cervarix®)疫苗[7]。这类表达系统的优点包括高蛋白表达量、低成本和容易量产等。当然,杆状病毒的去活(inactivation)和清除(removal)在疫苗提纯的下游工艺中无疑是考虑重点和操作难点。图5是生产希瑞适®(Cervarix®)疫苗的简略示意图。
图5:希瑞适®(Cervarix®)疫苗的生产工艺流程图
(http://www.slideshare.net/PriyeshWaghmare/manufacturing-of-cervarix)
当然,除了则选择使用杆状病毒-昆虫细胞表达系统外,很多研究尝试了不同的表达系统来生产HPV16的L1-VLP。表格1中列出了不同表达系统以及产量。
表格1:其他生产HPV L1-VLP的表达系统的概况
| 表达系统 | 细胞 | 产量 | 参考文献 |
| 转基因植物 | 土豆 | 4 pg/mg | [8] |
| 酵母 | S.cerevisiae | 2.7 | [9] |
| 酵母 | P.pastoris | 13.8 | [9] |
| 细菌 | 大肠杆菌 | 0.75 | [10] |
References:
1. Bosch, F.X., Manos, M.M., Munoz, N., Sherman, M., Jansen, A.M., Peto, J., Schiffman, M.H., Moreno, V., Kurman, R., Shah, K.: Prevalence of human papillomavirus in cervical cancer: a worldwide perspective. J. Natl. Cancer Inst. 87, 796–802 (1995).
2. Roldão, A., Mellado, M.C.M., Castilho, L.R., Carrondo, M.J.T., Alves, P.M.: Virus-like particles in vaccine development. Expert Rev. Vaccines. 9, 1149–1176 (2010).
3. Monie, A., Hung, C.-F., Roden, R., Wu, T.-C.: Cervarix: a vaccine for the prevention of HPV 16, 18-associated cervical cancer. Biologics. 2, 97–105 (2008).
4. Zhang, X., Li, S., Modis, Y., Li, Z., Zhang, J., Xia, N., Zhao, Q.: Functional assessment and structural basis of antibody binding to human papillomavirus capsid. Rev. Med. Virol. 26, 115–128 (2016).
5. Grgacic, E.V.L., Anderson, D. a.: Virus-like particles: Passport to immune recognition. Methods. 40, 60–65 (2006).
6. Ludwig, C., Wagner, R.: Virus-like particles-universal molecular toolboxes. Curr. Opin. Biotechnol. 18, 537–545 (2007).
7. Senger, T., Schadlich, L., Gissmann, L., Muller, M.: Enhanced papillomavirus-like particle production in insect cells. Virology. 388, 344–353 (2009).
8. Warzecha, H., Mason, H.S., Lane, C., Tryggvesson, A., Rybicki, E., Williamson, A.-L., Clements, J.D., Rose, R.C.: Oral immunogenicity of human papillomavirus-like particles expressed in potato. J. Virol. 77, 8702–11 (2003).
9. Park, M.-A., Kim, H.J., Kim, H.-J.: Optimum conditions for production and purification of human papillomavirus type 16 L1 protein from Saccharomyces cerevisiae. Protein Expr. Purif. 59, 175–181 (2008).
10. Sch??dlich, L., Senger, T., Kirschning, C.J., M??ller, M., Gissmann, L.: Refining HPV 16 L1 purification from E. coli: Reducing endotoxin contaminations and their impact on immunogenicity. Vaccine. 27, 1511–1522 (2009).
管理员邮箱:info@bioengx.org;管理员微信:bioengxadmin; 内容由作者原创。欢迎留言讨论哦,如需再转载,请联系管理员。
扫描下方二维码关注BioEngX官方微信公众平台












micronase 2.5mg drug – actos 30mg drug buy dapagliflozin without a prescription
clarinex usa – order aristocort 10mg generic order generic albuterol 4mg
generic allergy pills – buy fexofenadine 120mg generic buy theophylline for sale
buy ivermectin 3mg – eryc cheap order cefaclor pills
buy generic cleocin – vantin 200mg sale order chloromycetin without prescription
cheap amoxil – order cephalexin 125mg cost ciprofloxacin 1000mg
brand augmentin 1000mg – cheap linezolid 600 mg ciprofloxacin 1000mg usa
anafranil 25mg tablet – order paxil 10mg generic doxepin ca
buy seroquel 50mg generic – buy trazodone for sale cheap eskalith pills
clozaril 100mg us – order famotidine for sale famotidine cheap
retrovir 300 mg pill – order zyloprim 100mg pills
buy glycomet 1000mg sale – buy lincocin 500mg generic buy lincomycin no prescription
order lasix online cheap – tacrolimus tablet generic captopril 25 mg
buy metronidazole medication – order flagyl 400mg for sale order zithromax 250mg generic
buy generic acillin online buy penicillin cheap amoxil online buy
valacyclovir 1000mg for sale – nemasole medication acyclovir ca
stromectol pharmacy – suprax 200mg drug how to buy tetracycline
buy generic metronidazole 200mg – order amoxicillin without prescription zithromax 250mg sale
ciplox 500mg ca – buy tinidazole 500mg for sale order erythromycin 250mg online cheap
brand ciprofloxacin – purchase ethambutol online buy amoxiclav pills
cipro us – keflex order online order amoxiclav
atorvastatin 40mg us lipitor pill cost atorvastatin 80mg