在之前的文章中,小编给大家简介了四种提纯DNA的方法(历史文章点这里),分别是苯酚/氯仿抽提法、乙醇沉降法、硅胶柱吸附法和磁珠吸附法。其中,关于硅胶柱吸附法,也有过详细介绍(点这里),那么,今天小编就来说说苯酚抽提法。
苯酚抽提法非常简单,而且十分常见。特别是在提取基因组DNA时,要去掉许多从细胞裂解液中带来的蛋白,苯酚法十分好用。
苯酚抽提的基本步骤
- 将同体积的苯酚和(DNA+蛋白)混合物溶液混合;
- 苯酚和水溶液不互溶,所以分层,水层在上,苯酚层在下。快速震荡,让两层充分混合;
- 静置让两液层分开,分离水层,在水层中得到的应该是大量的DNA和可能少量的蛋白质。
基本原理
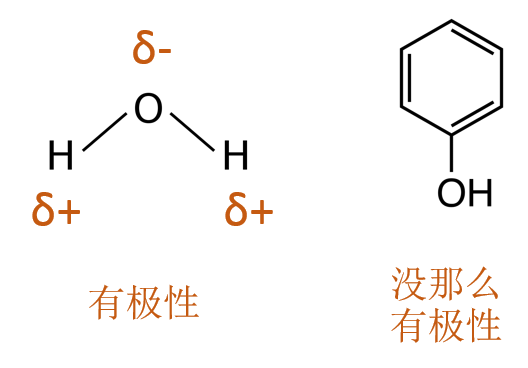
最核心的原理是水和苯酚作为有极性差异的溶剂,对DNA和蛋白质有不同的溶解能力。因为水分子中的氧原子有更强的电负性,共用电子对向氧原子偏离,产生了看似略带负电的氧原子端和略带正电的氢原子端,所以我们说水是很有极性的溶剂(如下图)。苯酚也有极性,但不像水分子那么明显,因为苯环也有电负性,所以苯酚的氧原子并不能太强吸引周围的电子(如下图)。
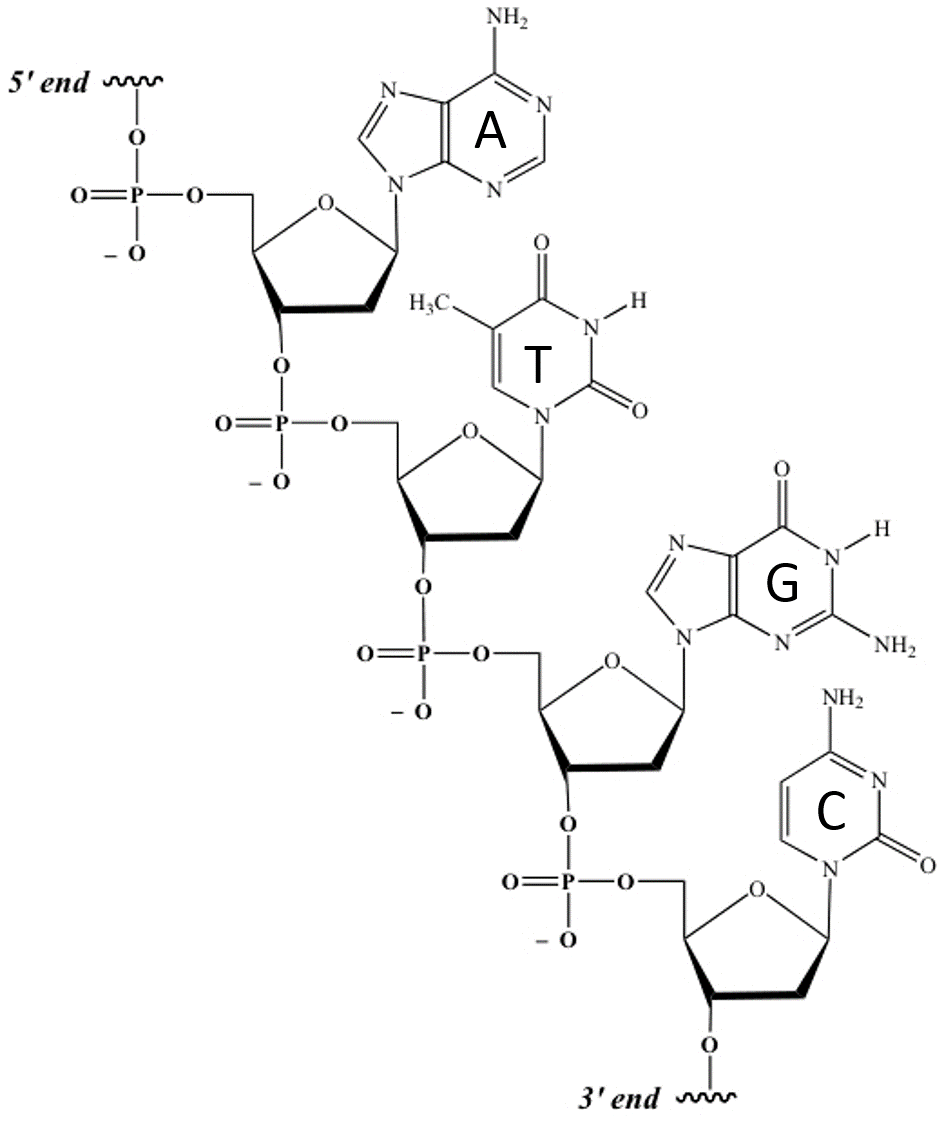
有一点我们是清楚的,DNA可溶于水,原因就是DNA也是有极性的分子(如下图,DNA分子的糖-磷骨架上的磷酸基团是带负电的)。对于一物质是否水溶,我们基本可以总结出:有极性(polar)=亲水性(hydrophilic)=可溶;无极性(non-polar)=憎水性(hydrophobic)=不溶
还有一点我们也是清楚的,细胞液环境是水环境,里面到溶解着各种蛋白质。蛋白质作为长链氨基酸,在形成有效结构的时候,外表面多是有极性的亲水类氨基酸(如谷氨酸、Glu;赖氨酸、Lys和组氨酸、His),内核多是没那么有极性的憎水类氨基酸,所以能够稳定的存在于水溶液中。
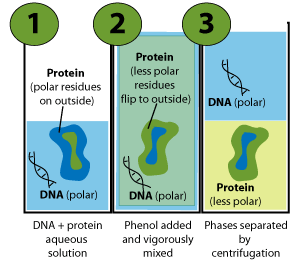
但是,在苯酚抽提法中,蛋白质在水中的溶解度被改变了。水溶液作为极性溶剂,导致了蛋白质的极性氨基酸在外,而没那没有极性的氨基酸在内;苯酚的到来,使得这些没那么有极性的氨基酸有了出头之日,他们被翻了出来,而那些有极性的氨基酸则被塞进蛋白质内核,以适应苯酚溶剂(基本原理如下图所示)。这样一来,变性的蛋白进入苯酚层,DNA则停留在水层。这也是为什么,有机溶剂会让蛋白质变性,因为不可逆地破坏了蛋白的整体结构。
苯酚抽提,简单有效,只是苯酚有毒,操作的时候要小心哦!小伙伴们对DNA提纯有想法或心得,请在下方留言,欢迎讨论!
图片来自网络,其余文字部分为BioEngX原创,转载请注明!










purchase famciclovir without prescription – valcivir 500mg drug valaciclovir price
order nizoral 200mg pill – buy ketoconazole 200mg how to get itraconazole without a prescription
order semaglutide 14 mg online cheap – semaglutide 14mg usa order desmopressin online
terbinafine cost – lamisil 250mg oral griseofulvin uk
buy micronase no prescription – buy glyburide 5mg generic buy forxiga cheap
clarinex canada – order albuterol generic ventolin
buy methylprednisolone sale – claritin order cost astelin
order ventolin inhalator – fexofenadine 180mg ca theo-24 Cr 400mg cost
ivermectin tablets – purchase eryc without prescription brand cefaclor 250mg
oral azithromycin 500mg – ciplox 500 mg canada ciplox oral
amoxil canada – buy cefuroxime pills for sale buy ciprofloxacin paypal
order hydroxyzine pills – fluoxetine 40mg ca amitriptyline order
generic anafranil 25mg – order generic tofranil 25mg buy cheap generic sinequan
buy quetiapine no prescription – order effexor 150mg online purchase eskalith online cheap
clozaril order – generic perindopril 4mg buy pepcid without a prescription
how to buy zidovudine – how to buy allopurinol cheap zyloprim 100mg
order glucophage 500mg pill – brand duricef 500mg lincocin 500mg without prescription
acillin cost acticlate over the counter how to get amoxicillin without a prescription
order metronidazole 200mg generic – cost azithromycin 250mg zithromax 500mg over the counter
stromectol 3mg – aczone us order tetracycline 500mg online cheap
order valacyclovir 1000mg – valacyclovir 1000mg cost buy generic zovirax for sale
ciplox 500 mg brand – chloramphenicol without prescription cheap erythromycin 250mg
where can i buy metronidazole – buy amoxicillin generic order zithromax for sale
buy cipro 1000mg for sale – buy generic keflex 500mg augmentin for sale online
cheap cipro – ciprofloxacin 500mg pills cheap augmentin 625mg
atorvastatin 10mg generic cost atorvastatin 80mg atorvastatin where to buy