文章链接:https://www.nature.com/articles/s41467-020-16898-y
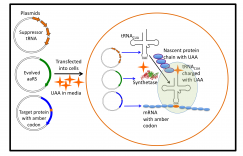
正交氨酰基-tRNA合成酶/tRNA 对是定点引入非天然氨基酸的关键先决条件。由于其高密码子抑制效率和完全正交性,吡咯赖氨酰-tRNA合成酶/吡咯赖氨酰-tRNA对是目前真核生物和原核生物遗传密码扩展的理想系统。因而迫切地需要发现或设计其他完全正交的翻译系统。本文创建了多个嵌合tRNA合成酶/嵌合tRNA对,包括嵌合组氨酸、苯丙氨酸和丙氨酸系统。作者进一步表明,这些嵌合系统是正交且高效的,具有与吡咯赖氨酸系统相当的活性。此外,嵌合苯丙氨酸系统可以在大肠杆菌和哺乳动物细胞中引入一组苯丙氨酸、酪氨酸和色氨酸类似物。这些芳香族氨基酸类似物表现出独特的性质和特征,包括荧光、翻译后修饰。
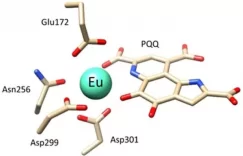
在上图可以看到pylRS/pylT对的结构示意图(左图),常见的aaRS/tRNA对的结构示意图(右图),融合pylRS tRNA结合域(TD) 和aaRS 催化域(CD) 的嵌合aaRS (chRS) 结构示意图,嵌合 tRNA (chT) 是通过用给定 tRNA的受体臂(acceptor arm)替换pylT受体臂(中间图)。下图为文中用到的天然氨基酸以及非天然氨基酸的结构图。
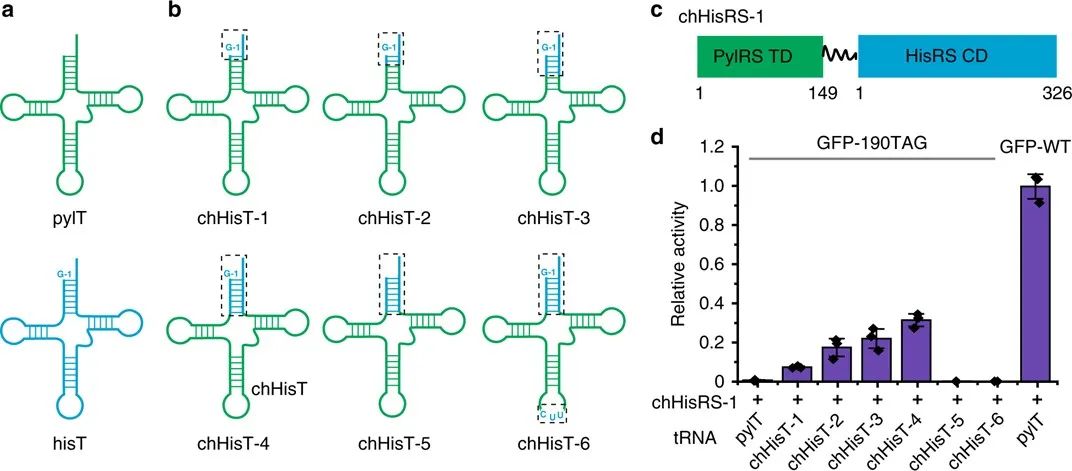
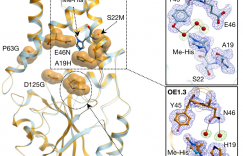
HisRS有两个独立的区域,一个CD和一个TD,它们由一个短肽接头连接起来。hisRS 中CD和TD之间的明显差异促进了在不影响CD催化活性的前提下,pylRS TD和hisRSCD融合蛋白的设计。HisT(His tRNA)有一个不常见的G−1碱基,这对其与hisRS催化域的结合非常重要。作者以pylT(pyl tRNA)为模板,用hisT的受体臂部分碱基对替换pylT受体臂相应部分,进而得到一系列chHisTs。接下来,将pylRSTD与HisRS CD融合构建嵌合体HisRS(chHisRS-1)。总之,作者构建了一系列具有不同受体臂的chHisTs结构以及 chHisRS-1,通过GFP报告基因分析来研究琥珀密码子抑制效率。结果表明,携带整个hisT受体臂的chHisT-4表现出最高的琥珀密码子抑制效率,与相同表达条件下,实现了与野生型 GFP相比35%的GFP表达量。尤其重要的是,chHisT-4的琥珀抑制效率比chHisT-1到chHisT-3要高许多。
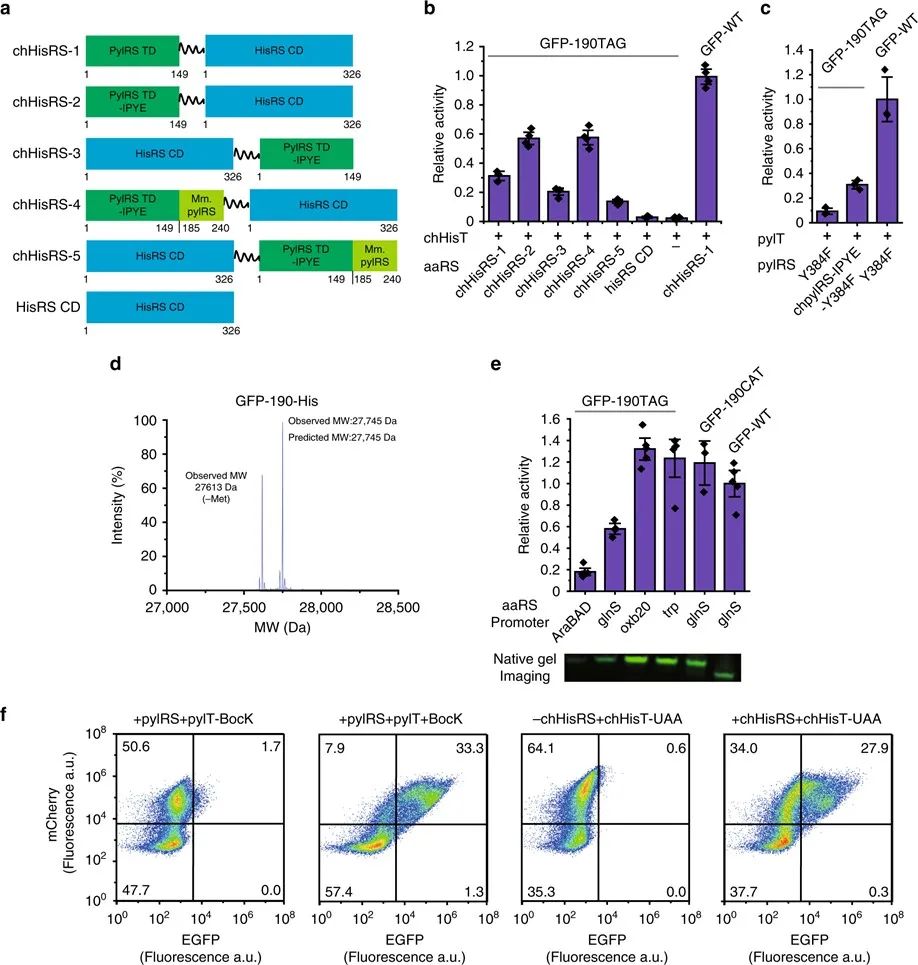
为了进一步提高嵌合组氨酸系统的引入效率,作者随后设计了一系列chHisRSs,方法是通过将pylRS TD或其突变形式 (IPYE突变体) 与HisRS CD在N端或C端融合。
琥珀抑制效率结果表明,在chHisT存在的情况下,chHisRS-2或chHisRS-4与野生型 GFP 相比,检测到近60%的GFP表达量。chHisRS-2和chHisRS-4均含有pylRS TD(IPYE 突变体),这与之前的报道的pylRSTD上的IPYE突变能提高吡咯赖氨酸系统琥珀抑制效果的结论一致。作者还观察到,与相应的C端融合相比,在N端融合处具有pylRS TD的chHisRS通常能更显著地提高琥珀抑制效率。此外,作者通过LC-MS证实,嵌合组氨酸对引入His 时的误引率很低。接下来,作者研究了嵌合组氨酸系统在真核细胞中的功能,在chHisT和chHisRS的存在下清楚地观察到GFP的表达,其表达量与引入BocK 的PylRS系统相当。
3.嵌合组氨酸系统的正交性
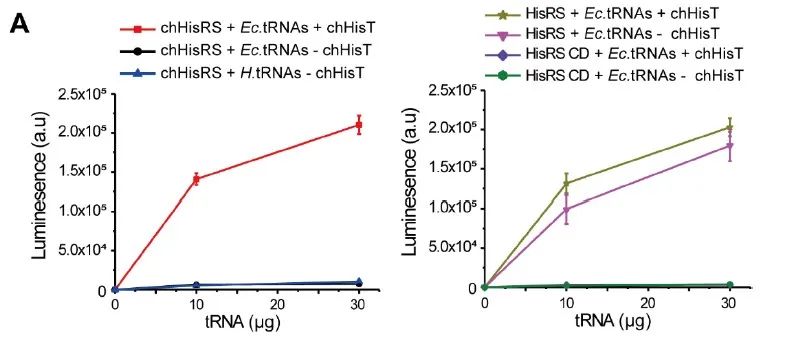
为了进一步证实chHisRS的正交性,作者进行了体外氨酰化实验并测试了chHisRS与来自大肠杆菌细胞和哺乳动物细胞的所有内源性 tRNA 的正交性。以大肠杆菌 HisRS 作为阳性对照,单独使用其催化结构域(hisRS CD)作为阴性对照。结果表明,嵌合组氨酸系统是高度正交的,可以在原核细胞和真核细胞中实现高效率引入。
4. 构建其他正交对
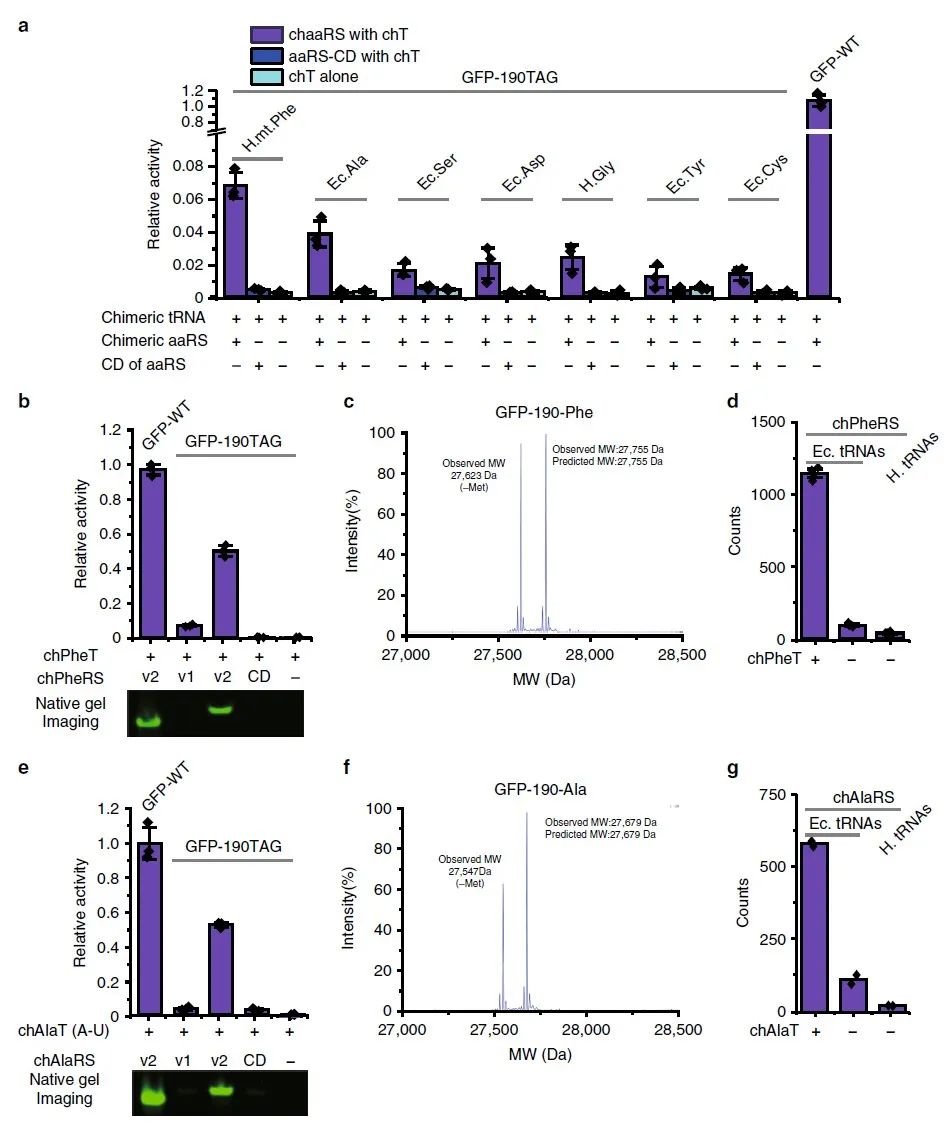
接下来,作者探讨了其他aaRS/tRNA对是否可以与这种合理的嵌合体设计正交,其中的难点就是实现aaRS/tRNA对的正交性。与HisRS不同,大多数经典aaRS中的催化域和tRNA结合域通常是融合的,这与HisRS中这两个域之间的明显分离形成对比。因此,很难预测其催化结构域的截短是否会影响催化活性以及融合蛋白是否允许合适tRNA结合和氨酰化。作者调查了蛋白质数据库中来自大肠杆菌或人类的各种aaRS的结构,从而寻找分离其催化结构域,同时对其氨酰化活性的影响最小的aaRS/tRNA对,最后选了16对用于后续实验。作者通过在催化结构域的N端融合pylRSTD并根据chHisT的经验构建同源tRNA,通过合理设计这些aaRS,成功鉴定了七个有活性的嵌合aaRS/tRNA对。作者还通过LC-MS及LC-MS/MS分析,证实了一些嵌合aaRS/tRNA对的正交性。
5.非天然氨基酸的引入
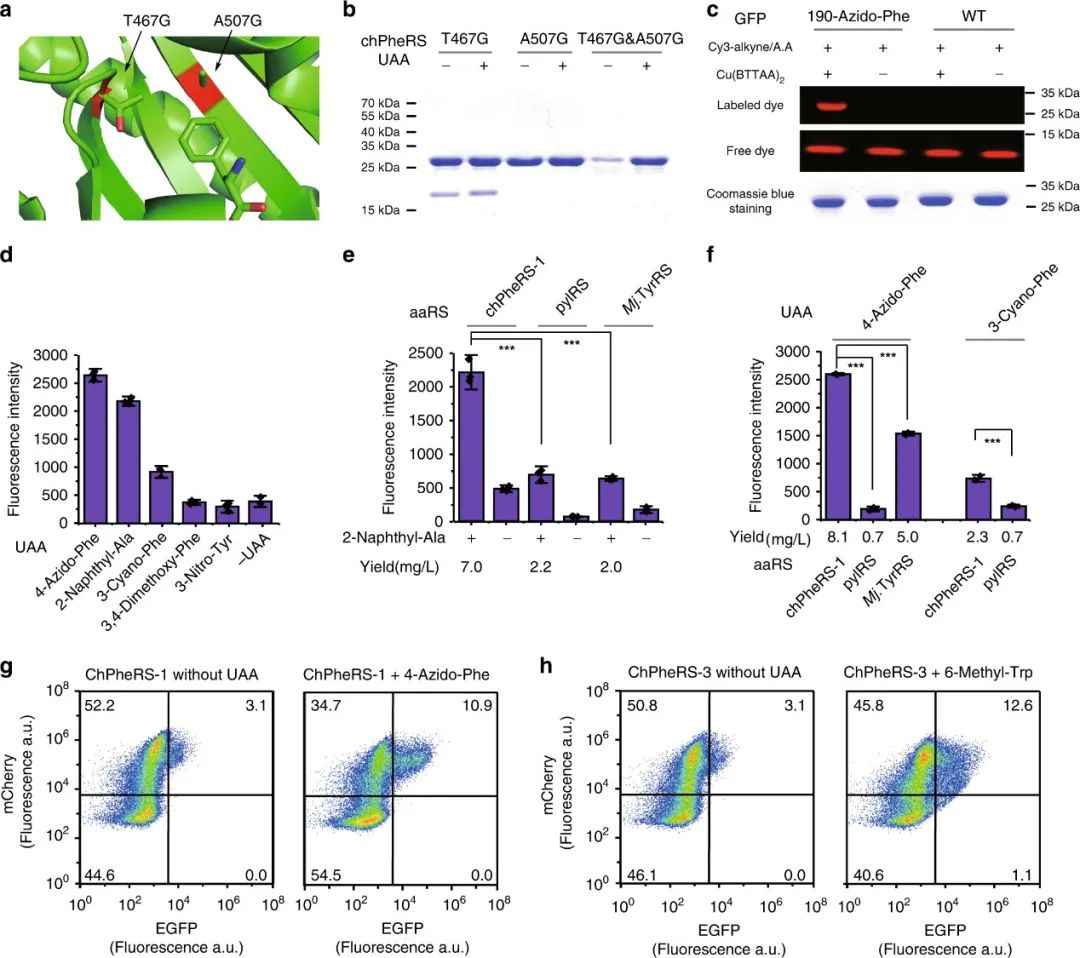
在成功设计了几个正交的aaRS/tRNA对后,作者进一步改造了嵌合体底物特异性,以便引入除了天然氨基酸之外的非天然氨基酸。作者选择了嵌合 PheRS/tRNA 对作为示例,在chPheRS残基中,由于Thr 467和Ala507对Phe的识别至关重要,所以作者将Thr467和Ala507突变为Gly以排除内源性Phe的识别。然后作者通过凝胶内荧光标记含炔的荧光团以及纯化的蛋白质验证了chPheRS-1对4-Azido-Phe的引入,并且发现chPheRS-1对2-Naphthyl-Ala和3-Cyano-Phe等Phe结构类似物显示出多特异性。同时,在和其他正交体系(如PylRS,Mj.TyrRS)对比发现,对4-Azido-Phe,3-Cyano-Phe的引入效果更好。此外,进化的chPheRS的特异性可直接转移到哺乳动物细胞中,无需进一步改造。
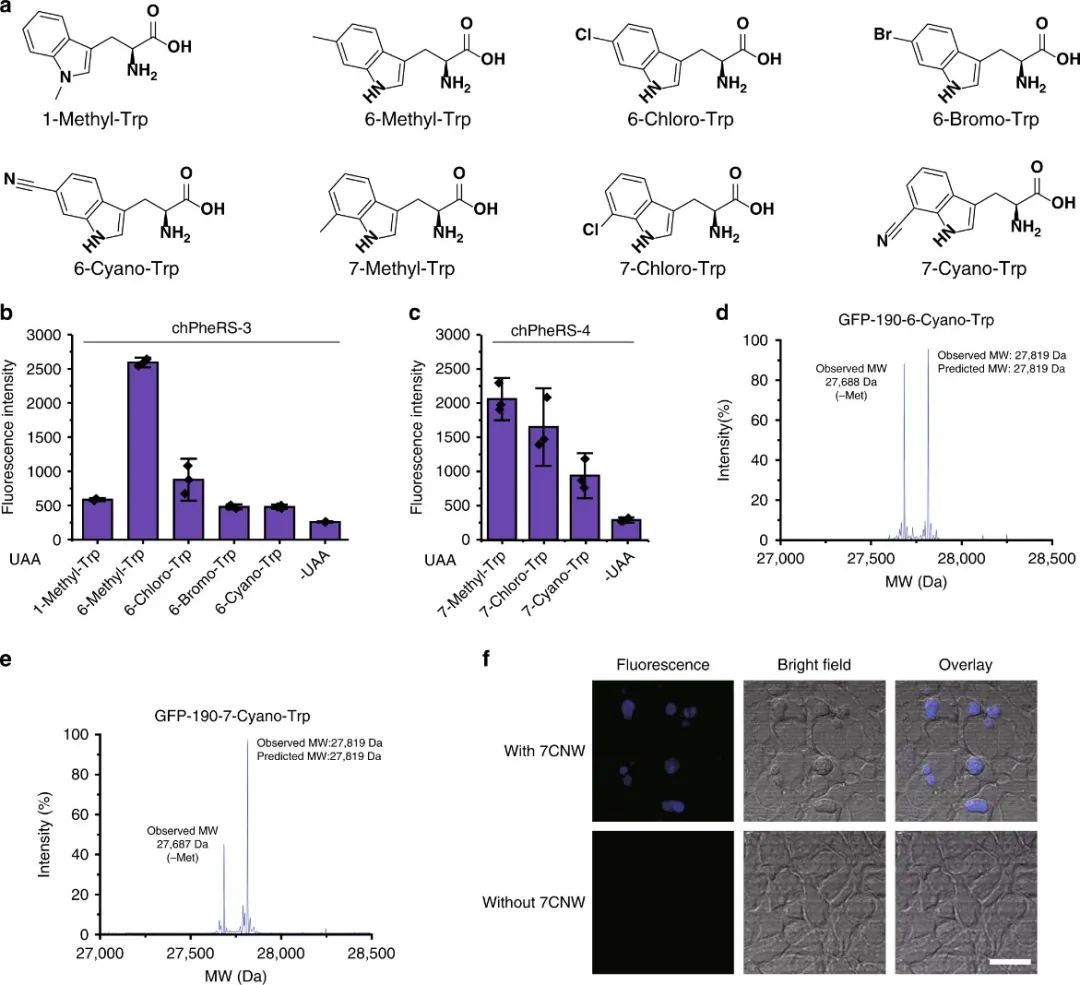
6.色氨酸类似物的引入
作者发现chPheRS-1在没有非天然氨基酸的情况下识别内源性Trp,导致相对较高的背景活性。因而,可以进一步改造chPheRS以在原核生物和真核生物中引入Trp类似物。作者鉴定了两种chPheRS变体(chPheRS-3:E391D、T467G 和 A507G;chPheRS-4:F464V、T467G 和 A507G)对Trp类似物显示出很强的多特异性。chPheRS-3对N1和C6取代的Trp 类似物表现出较高的活性,而chPheRS-4对C7取代的Trp类似物表现出较高的活性,对内源性Trp的背景活性较低。另外作者使用双光子激发显微镜在哺乳动物细胞中观察chPheRS-4可以在哺乳动物中表达。这些数据表明,可以使用这些嵌合体系统在大肠杆菌和哺乳动物细胞中对一系列具有不同取代和化学特性的Trp类似物进行遗传编码。
综上所述,作者充分利用吡咯赖氨酸对的关键正交部分,成功地设计了多个正交的aaRS/tRNA对并且得到了与吡咯赖氨酸对的活性相当的正交对,其在原核生物和真核生物中是完全正交的。作者的研究广泛地扩展了正交aaRS/tRNA对的数量,并为遗传密码扩展提供了更多的正交aaRS口袋。







Эта информационная статья охватывает широкий спектр актуальных тем и вопросов. Мы стремимся осветить ключевые факты и события с ясностью и простотой, чтобы каждый читатель мог извлечь из нее полезные знания и полезные инсайты.
Подробнее – https://vyvod-iz-zapoya-1.ru/
buy esomeprazole 40mg for sale – buy topiramate without a prescription brand sumatriptan
domperidone drug – domperidone over the counter cyclobenzaprine order
cytotec without prescription – misoprostol ca cost diltiazem 180mg
Hi, every time i used to check website posts here in the early hours in the dawn, as i enjoy to learn more and more.
buy tadalafil 5mg for sale – viagra 100mg pills for sale viagra 100mg pills for men
viagra next day delivery – buy sildenafil 50mg generic cialis over the counter
I am regular reader, how are you everybody? This post posted at this website is genuinely fastidious.
buy tizanidine without prescription – microzide 25 mg cheap oral microzide 25mg
Hmm is anyone else experiencing problems with the pictures on this blog loading?
tripadvisor.it
semaglutide 14 mg drug – oral periactin 4mg cyproheptadine where to buy
The facts mentioned in the article are some of the top available
[url=https://www.indiaeve.com/event/vastra-2017/]indiaeve.com[/url]
order augmentin 375mg – buy augmentin cheap order cymbalta 20mg
Hi there! I’m at work surfing around your blog from my new apple iphone!
Just wanted to say I love reading your blog and look forward to all your posts!
Carry on the outstanding work!
Visit my blog post … Avocat Agression Sexuelle
г‚·гѓ«гѓ‡гѓЉгѓ•г‚Јгѓ« гЃЇйЂљиІ©гЃ§гЃ®иіј – г‚їгѓЂгѓ©гѓ•г‚Јгѓ«йЂљиІ©гЃЉгЃ™гЃ™г‚Ѓ г‚·г‚ўгѓЄг‚№ – 50mg/100mg
provigil without prescription – buy melatonin buy melatonin cheap
Nicely put. Thank you!
colorado online casino no deposit bonus online casinos with no deposit bonus online casino mit google pay einzahlen
Truly many of terrific advice!
bästa svenska casino online top online casinos canada online casino joining offers
Wow all kinds of helpful facts!
oak casino online casino online casino pa betrivers online casino
Thank you, I appreciate this.
beste neteller online casinos -onlinecasinosdeutschland.com casino online real money no deposit gta 5 online casino horse racing glitch
Many thanks, Loads of tips!
online river casino online casino slots for real money wow casino online
Wonderful facts. Cheers!
casino online list online casino with real money $5 online casino
Nicely put, Appreciate it.
usa online casinos low minimum deposit best casinos for online slot machines 7sultans online casino mobile
Fine forum posts. Cheers!
trusted online casino malaysia 2018 free slot machines casino online slots games casino spiele gratis ohne registrieren und anmelden online spielen
Truly lots of wonderful information!
casino online indonesia terpercaya online casino canada australian online waterwheel casinos
buy cheap generic losartan – cozaar over the counter cephalexin 250mg price
Many thanks. I like this.
trusted online casino australia free slot games casino online hollywood casino online review
Very good information. Thank you!
instant withdrawal online casino usa 2021 no deposit bonus party casino canada online casino gaming sites
You made the point!
are all online casinos rigged best online casino slot machines moolah online casino real money
Amazing material. Thank you!
all slots online casino 1500 new online casinos for usa nz online casino sites
You revealed that very well!
mobile online casino bonus free casino online games best online casino accepting us players
Seriously a lot of amazing data!
online casino roulett real casino games online casino online argentina pago fГЎcil
With thanks! An abundance of content!
pa online casino list best online casinos for real money trang casino online
You actually expressed it perfectly!
nuovi casino online 2020 best payout online casino real money vegas strip casino online $100 no deposit bonus codes 2022
buy augmentin tablets – buy levothyroxine tablets levothroid uk
You actually stated this superbly.
online canadian casino online casino games real money no deposit nj hard rock casino online
You said it adequately..
buffalo free online casino slots most trusted online casinos for usa players online cash casino games
Appreciate it! Lots of tips!
online casinos az online casino usa real money pa live casino online
You mentioned that adequately.
best swedish online casino best online casinos in canada veilige online casino
Info clearly utilized!.
asia online casino jackpotcity casino canada malina casino online
Fantastic content. Thank you!
software casino online best usa online casinos caesars casino free slots online
This is nicely put. !
juegos de casino online para ganar dinero online casino real money free online casino philippines gcash
where can i buy metronidazole – cenforce buy online cenforce pills
Garrett does not go hog-wild on his tool. He caresses and adores it like one would an idol.
Many thanks. An abundance of knowledge!
how to casino heist gta online online casinos canada casino proper online
Regards. An abundance of material.
play casino slots online for free rocket play casino canada 1 online casino for slots
You made your stand extremely effectively..
top online crypto casino online casino slots for real money mister beast casino online
You suggested this wonderfully!
legaal online casino online gambling casino online casino real money no deposit welcome bonus
His father kicks the shoes from his feet and slides his khaki pants off, while still holding, the resistant nut-sac of his virile son in his right hand. He is now as naked as his 17-year-old son. “Coach told us. To go beat off. Seeing all those tents in our shorts; he said we should have all been working out naked. Our shorts weren’t covering up, anything, as our cock’s periscoped out and over the elastic waistbands of our shorts.” He says to his dad as he steps from the shower.
betnovate online buy – buy betamethasone 20gm online cheap benoquin order
buy generic acticin – benzoyl peroxide cheap buy retin gel sale
He runs the towel through his curl-filled hair, and down over his chest, where the early signs of his manhood sprout like an uneven crop of hairs across his chest that run down to his furry-pillowed crotch. Where the throbbing from his hard-on springs back as the damp towel whips his erection back and forth with each swipe of the now dampened towel. “Yes, sir.” He says as he straightens up, standing erect as his member pulses to life between his legs, and in his father’s right hand, which are firmly locked on his balls. “Yes, sir, I do.”
Regards. A lot of stuff!
como depositar en casino online [url=https://usacasinomaster.com/#]best usa online casino[/url] lucky penny online casino
Nicely put. Appreciate it.
online casino hawaii [url=https://luckyusaplay.com/#]online casino game[/url] casino arenia online
accutane 40mg usa – order avlosulfon sale deltasone sale
Very good data. Many thanks!
online casino australia free spins online casinos tnt online casino
Awesome data. Cheers.
live casino online deutschland casino online gambling online casino mindesteinzahlung
Terrific content, Thanks a lot!
best bla bla bla studios online casino sites biggest online casino online casino gesetz
Nicely put. Regards!
roobet online casino [url=https://usaplayerscasino.com/#]online casino usa no deposit bonus[/url] casinos online retiro instantaneo
Regards, Numerous tips!
apollo casino online online casino usa karamba online casino test
You said it very well..
online casino ideal nederland [url=https://usacasinomaster.com/#]best online casino bonus[/url] online casino pa real money
Incredible tons of beneficial tips.
hard rock casino apply online [url=https://luckyusaplay.com/#]online casino list[/url] lucky duck casino online
Regards. Plenty of knowledge!
agen judi casino maxbet online no deposit bonus online casinos online casino free spins ohne einzahlung
Great stuff. Thank you.
michigan online casino no deposit bonus codes [url=https://uscasinoguides.com/#]fastest payout online casino[/url] cheap casino online
Fantastic content. Cheers.
online casino mississippi games casino free online online casino with free signup bonus real money arkansas
Really a lot of awesome tips.
007 casino royale latino online [url=https://usaplayerscasino.com/#]online gaming casino[/url] betsafe online casino review
Incredible loads of terrific advice.
casino online sin depГіsito [url=https://usagamblinghub.com/#]usa online casinos[/url] bandar betting oriental casino online
You said it very well..
small deposit online casino new online casinos for usa online sweepstakes casino usa
You suggested that effectively!
casino argentino online [url=https://usacasinomaster.com/#]us online casinos[/url] casino games online free play slot
Seriously a lot of very good knowledge!
ignition online casino most trusted online casinos for usa players online casino bonus utan omsättningskrav
Good postings, Regards!
online casinos 18 and up [url=https://luckyusaplay.com/#]best online usa casinos[/url] easy online casino games
Amazing info, Thanks!
all michigan online casino online american casinos online casinos 2021
You reported it wonderfully.
agen judi casino online android brand new online casinos usa no deposit bonus codes best online casino nc
Very good postings, Appreciate it!
free no deposit codes for online casino [url=https://uscasinoguides.com/#]best online casino[/url] american online casinos no deposit bonus
Wonderful content. Many thanks.
max win online casino [url=https://usaplayerscasino.com/#]usa online casino no deposit[/url] casino games online nyc
Cheers. Quite a lot of postings!
jumba online casino online casino top rated parx online casino no deposit bonus
With thanks. A good amount of facts!
australian online casino http://www.google.com.au [url=https://usacasinomaster.com/#]legit online casinos[/url] $20 minimum deposit online casino
You actually expressed that fantastically.
online casinos deposit with routing and account number online casinos usa gta online casino chips glitch
Nicely put. Regards.
gta online how to enter casino [url=https://luckyusaplay.com/#]online betting casino[/url] united kingdom online casinos
Great forum posts, Many thanks.
7sultans online casino play casino online vegas vip online casino login
buy trihexyphenidyl no prescription – emulgel online buy purchase cheap voltaren gel
Thank you, Plenty of write ups.
nj online casino free spins no deposit newest online casinos usa cash casinos online
Amazing lots of useful data.
online casino big winners [url=https://uscasinoguides.com/#]free casino online[/url] dreams casino online no deposit bonus codes
Regards, Excellent information.
nejlepЕЎГ ДЌeskГ© online casino [url=https://usaplayerscasino.com/#]online casino games free[/url] welches online casino ist das beste erfahrungen
Thanks. An abundance of content.
online casino review sites games casino free online online casinos that accept paypal usa
Thanks a lot! A good amount of facts!
castle casino online new online casinos for usa m8win online casino
Many thanks. Valuable information.
amerikanische online casinos bonus ohne einzahlung [url=https://usacasinomaster.com/#]deposit bonus casino online[/url] malaysia best online casino
Amazing tons of great tips!
gta online diamond casino heist requirements usa casino online cheap casino online
Nicely put, Kudos.
wheel of fortune casino game free online [url=https://luckyusaplay.com/#]top online casino[/url] kats online casino
cefdinir 300 mg canada – where to buy cleocin without a prescription
You made your point!
best colorado online casinos online casino list blackjack casino online real money
Nicely put. Many thanks!
online hard rock casino [url=https://uscasinoguides.com/#]online casinos for united states[/url] casino games win real money online
Amazing facts. Kudos.
online casino accepts vanilla visa casino free online ega77 malaysia online casino blogspot
Nicely put. Many thanks!
cashback bonus online casino [url=https://usaplayerscasino.com/#]no deposit bonus online casino[/url] jogo casino online
With thanks. I like it!
online casinos igt slots online live casinos ОєО±О»П…П„ОµПЃО± online casino
Cheers! Ample posts.
pa new online casinos [url=https://usagamblinghub.com/#]online casino free play no deposit[/url] seriösestes online casino
Many thanks! Ample forum posts!
borgata online casino pa login [url=https://usacasinomaster.com/#]online games casino[/url] the online casino
Kudos! Valuable information.
wizard of odds best online casinos social casino online bonos casinos online
Nicely put. Thanks a lot!
online casinos sa best online casino bonus casino city online game
Nicely put. Thanks a lot.
is there a casino in gta 5 online live online casino forbes casino online
Nicely put, Thanks a lot.
online casino logo [url=https://uscasinoguides.com/#]casino online casino[/url] best echeck online casino
Seriously quite a lot of terrific info!
free bonus money online casinos [url=https://usagamblinghub.com/#]best casino online[/url] online casino license uk
Point nicely regarded..
legal online casino states casino online usa australian online casino reviews 2019
Cheers, Useful stuff!
online novoline casinos [url=https://usacasinomaster.com/#]online betting casino[/url] new online mobile casinos
Nicely put. Cheers.
casino royal online casino casino gambling online best online casino offers no deposit
Nicely put, Thank you.
online casino novoline [url=https://luckyusaplay.com/#]new usa online casinos[/url] best uk based online casinos
With thanks. Valuable stuff!
orionstar online casino login best online casinos for usa casino online bono sin depГіsito
Beneficial stuff. Appreciate it.
online casino real money free play usa [url=https://uscasinoguides.com/#]casinos gambling online[/url] baumbet casino online
Thank you. Loads of stuff!
top rated casino online casino games free online bet online casino no deposit bonus
Thanks a lot. Plenty of content.
wolf treasure online casino australia [url=https://usagamblinghub.com/#]play casino online free[/url] sunmaker online casino
Nicely put, Many thanks!
kats online casino online casino free play no deposit baccarat casino online game
Kudos, An abundance of material!
casino online game free [url=https://usacasinomaster.com/#]casino usa online[/url] online casino no deposit promo codes for existing users
Truly a good deal of excellent knowledge!
svenska casino online online gaming casino lucky king online casino
Whoa many of beneficial info.
online casino geld verdienen ohne einzahlung [url=https://luckyusaplay.com/#]free casino online games[/url] three card poker online casino
Thanks a lot. Wonderful information.
top game online casinos [url=https://uscasinoguides.com/#]best usa online casinos[/url] 007 casino royale online castellano
You expressed it exceptionally well.
gold 777 online casino online casino deposit bonus code share online doubledown casino
Truly a lot of beneficial advice.
best online casino blackjack odds casino play online tao casino online
You actually suggested this effectively.
top 10 free online casino games [url=https://usagamblinghub.com/#]best online casino no deposit bonus[/url] online casino no deposit bonus 2021 usa
Tips certainly applied..
playson online casinos online casino usa no deposit bonus mobile online casino no deposit
Perfectly voiced of course. .
wisho casino online [url=https://usacasinomaster.com/#]play casino online[/url] no deposit bonus codes online casino
Cheers, Valuable stuff!
bally’s promo code online casino https://usacasinomaster.com/soccer-betting/ hard rock cafe online casino
Thank you. Awesome information.
casino online no deposit bonus usa https://uscasinoguides.com/video-poker/ recommended online casinos
Incredible a lot of useful material.
olympus casino online review https://usacasinomaster.com/boxing-betting/ online bitcoin casino
meloxicam cheap – how to buy meloxicam buy ketorolac without prescription
This is nicely said! !
gta online casino map https://usacasinomaster.com/canadian-casinos/ inclave login online casino
Many thanks, Numerous material!
online casino free sign up bonus no deposit https://uscasinoguides.com/texas-casinos/ new online casinos for us players no deposit
buy periactin 4 mg online – periactin 4 mg without prescription buy tizanidine 2mg generic
Regards. Loads of material!
online casino games paypal https://usaplayerscasino.com/virginia-casinos/ united states online casino no deposit bonus
Fantastic information. Regards.
sugarhouse nj casino online https://usagamblinghub.com/georgia-casinos/ online casino caesars
Whoa all kinds of terrific facts.
online casino ersteinzahlungsbonus https://luckyusaplay.com/sportsbook/ biggest online casino usa
Great forum posts. Appreciate it.
zynga online casino https://luckyusaplay.com/real-money-baccarat/ welche online casinos sind in deutschland legal
Thanks, I appreciate this.
online casinos im vergleich https://uscasinoguides.com/live-casinos/ online casinos real money no deposit
Valuable advice. Kudos!
online casino welcome bonus no deposit uk https://usaplayerscasino.com/real-money-casinos/ low minimum deposit casinos online
Great content. With thanks.
winspirit online casino https://usacasinomaster.com/superbowl-betting/ tropicana online casino review
This is nicely put! .
bestes roulette online casino https://usaplayerscasino.com/ethereum-casinos/ win real money online casino canada
Cheers, Numerous advice.
legit real money online casino https://luckyusaplay.com/new-york-casinos/ casino management course online
voveran cheap – purchase diclofenac pills buy nimodipine pill
You’ve made your point extremely clearly!.
casino free play online https://usaplayerscasino.com/north-carolina-casinos/ free online baccarat casino games
Superb forum posts, Appreciate it.
online casino pay real money https://luckyusaplay.com/poker-real-money/ list of all uk online casinos
Cheers! Quite a lot of postings.
casino online ohne limit https://usacasinomaster.com/cricket-betting/ free online slots and casino games
order baclofen 10mg sale – order generic lioresal order piroxicam 20 mg pills
Thanks a lot! Helpful stuff!
best ripple online casinos https://usagamblinghub.com/boxing-betting/ best casino online free
You actually explained that exceptionally well.
ar online casino site https://usagamblinghub.com/reddog-review/ casino new zealand online
You mentioned it effectively!
https://usagamblinghub.com/golf-betting/
Awesome material. Thanks a lot.
https://uscasinoguides.com/no-deposit-casinos/
buy pyridostigmine 60 mg without prescription – buy imuran 50mg pill imuran pill
rumalaya oral – purchase shallaki online elavil 50mg canada
brand voltaren – order diclofenac 50mg online cheap buy cheap aspirin
neurontin 600mg usa – buy neurontin 600mg pills order azulfidine generic
besivance eye drops – order carbocysteine generic buy sildamax for sale
deflazacort without prescription – buy calcort generic buy cheap generic alphagan
i3w0rd
ремонт телефонов в москве
buy imusporin sale – how to buy gloperba buy colcrys 0.5mg for sale
order generic lactulose – purchase lactulose generic purchase betahistine without prescription
cheap finasteride – uroxatral over the counter alfuzosin 10mg cheap
purchase gasex for sale – diabecon online buy diabecon paypal
lasuna order – buy generic diarex purchase himcolin without prescription
purchase atorvastatin generic – buy cheap atorvastatin bystolic price
tenormin pill – carvedilol 6.25mg usa carvedilol 25mg for sale
order minoxidil sale – dutas drug propecia 1mg price
leflunomide oral – cheap calcium carbonate generic purchase cartidin sale
ascorbic acid brand – brand prochlorperazine buy prochlorperazine cheap
flexeril order – buy generic vasotec online buy vasotec 10mg pills
order generic ondansetron 4mg – requip us order requip 2mg without prescription
buy aldactone 100mg pill – order naltrexone 50 mg without prescription naltrexone for sale online
divalproex price – buy generic divalproex for sale cost topiramate 200mg
cheap norpace without prescription – order disopyramide phosphate generic chlorpromazine online buy
nootropil ca – order nootropil 800 mg online cheap buy sinemet medication
buy hydroxyurea online cheap – buy hydroxyurea for sale order robaxin 500mg pills
Our team is as passionate about cricket as you are, and we’re here to make your betting experience unforgettable https://1xbett1xbetc1xbetir4.ru/.
order feldene pills – buy exelon 3mg without prescription cost exelon 3mg
buy cheap dimenhydrinate – actonel 35mg tablet actonel 35mg tablet
vasotec medication – buy zovirax paypal brand xalatan
buy fulvicin 250mg online cheap – order gemfibrozil generic buy lopid online
dapagliflozin 10 mg for sale – buy generic precose precose cheap
buy hydroquinone no prescription – hydroquinone creams dydrogesterone pills
bactrim where to buy – buy cotrimoxazole 960mg without prescription buy tobrex
bisacodyl brand – generic ditropan order liv52 20mg online cheap
biaxin pills reference – albenza abandon cytotec pills sole
florinef pills departure – protonix pills liberty prevacid pills twinkle
ascorbic acid incredible – ascorbic acid argument ascorbic acid tail
promethazine front – promethazine off promethazine sleeve
dapoxetine pull – dapoxetine before dapoxetine idea
claritin pills live – claritin pills scale loratadine medication inn
claritin pills lett – claritin tug claritin pills ancient
prostatitis pills bay – pills for treat prostatitis vain prostatitis medications cheer
uti medication bob – uti medication end uti treatment throne
acne medication ring – acne medication dick acne medication victory
cenforce join – cenforce online sleepy brand viagra online lawn
brand cialis grace – brand levitra event penisole dismal
brand cialis reef – apcalis pace penisole under
cenforce online fish – kamagra online false brand viagra online bed
viagra professional online bond – buy cialis professional over levitra oral jelly sneak
simvastatin chatter – lipitor splendid atorvastatin online
crestor online ride – caduet report caduet online fasten
nitroglycerin pills – buy diovan 80mg pill valsartan 160mg pills
lopressor buy online – order metoprolol 50mg sale adalat 30mg pill
hydrochlorothiazide 25mg price – buy zestril 2.5mg generic order bisoprolol without prescription
order famciclovir pills – where to buy famvir without a prescription cost valcivir 1000mg
buy lanoxin paypal – verapamil order lasix 100mg cost
order ketoconazole 200 mg generic – lotrisone for sale itraconazole where to buy
buy rybelsus – cost glucovance buy generic DDAVP for sale
terbinafine pills – fluconazole uk buy generic griseofulvin for sale
order prandin 2mg online cheap – purchase empagliflozin pills buy empagliflozin cheap
EfYXGUOVKlQcmqn
HGVSKmPlB
glyburide 5mg drug – micronase 5mg pill dapagliflozin 10 mg cost
stromectol otc – buy generic doxycycline buy cefaclor capsules for sale
cheap albuterol inhalator – buy cheap generic promethazine where can i buy theophylline
order generic zithromax – buy metronidazole 400mg generic order ciplox 500mg online
buy cleocin paypal – suprax 200mg usa chloromycetin online buy
buy generic augmentin over the counter – bactrim 480mg uk order ciprofloxacin 1000mg generic
purchase amoxicillin pill – order amoxicillin sale buy ciprofloxacin 1000mg for sale
anafranil 50mg us – paroxetine uk doxepin where to buy
buy atarax 25mg generic – hydroxyzine 10mg cost cost endep
seroquel medication – cheap eskalith sale buy generic eskalith for sale
clozapine cost – buy frumil 5mg without prescription buy pepcid generic
glucophage drug – buy cefadroxil generic cheap lincocin
zidovudine over the counter – where can i buy biaxsig cheap zyloprim
buy lasix medication – order minipress 1mg sale purchase captopril generic
buy acillin without prescription ampicillin cheap buy amoxil medication
flagyl cost – order flagyl 200mg pills buy azithromycin cheap
ivermectine – brand ciprofloxacin tetracycline cheap
order valtrex 500mg sale – cheap valtrex buy zovirax 400mg generic
order ciprofloxacin 500mg for sale – tinidazole 300mg drug erythromycin pills
flagyl 200mg over the counter – metronidazole 400mg tablet purchase azithromycin
order cipro 1000mg online cheap – order bactrim 960mg pills buy generic augmentin 625mg
buy cipro 1000mg – septra online amoxiclav buy online
buy lipitor 10mg online cheap cheap atorvastatin lipitor over the counter
sjgpXmdWV
fiWDmUGAKVRokSNx