近日,本课题组与北京大学化学与分子工程学院陈鹏课题组合作,在Nature杂志上发表题为“Time-resolved protein activation by proximal decaging in living systems”的研究文章,报道了一种基于基因编码的非天然氨基酸“邻近脱笼”策略(CAGE-Prox),利用计算机辅助筛选,在一系列不同蛋白质上实现了高时间分辨率的原位激活,为在活体环境下研究蛋白质的瞬时功能动态变化提供了一种通用的技术手段。
“化学脱笼”策略是一类适用性广、干扰度低的蛋白质激活方法,通过对酶的关键催化残基进行保护与脱保护,实现蛋白功能“关”和“开”的操控。陈鹏课题组先后在赖氨酸、酪氨酸等活性氨基酸上实现了生物正交的断键反应和“脱笼”,在活细胞及动物活体实现了蛋白激酶,荧光素酶等蛋白质家族的特异性激活。然而对于很多没有“脱笼”反应的氨基酸或者活性位点不明确的酶,尚缺乏一种通用易行的原位激活手段。
王初课题组一直致力于在蛋白质组学的各种维度海量数据中,使用计算机辅助手段进行数据的理解和信息挖掘。例如对于质谱数据(0维)中Se同位素特征谱的识别(Gao, Yang, et. al., 2018);对蛋白序列(1维)中活性半胱氨酸酸的预测(Wang, Chen, Li, et. al., 2017);利用同源蛋白的多序列比对(2维)对氨基酸相互作用网络的预测(work in preparation);以及利用Rosetta软件对蛋白质进行结构(3维)建模和设计。
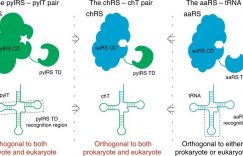
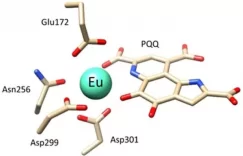
两个课题组一拍即合,希望能够共同开发一种不受氨基酸种类限制的通用“脱笼策略”。我们猜测,在蛋白质催化中心附近的其他氨基酸,都可能对稳定蛋白结构或支持底物结合起到重要贡献,如果可以找到某种氨基酸,在口袋中合适位置引入它的突变体,使其在被保护的状态下通过位阻效应阻止底物结合,而脱保护后却不影响蛋白活性,就可以用相同的“脱笼”反应操控任意蛋白的活性。于是,我们首先分析了一个含有一百多个蛋白与小分子复合物结构的数据库,统计其中口袋附近每种氨基酸出现的概率,并计算把它突变成其它种类氨基酸时对蛋白质稳定性的影响。结果发现,酪氨酸具有较高的天然丰度,且引入酪氨酸突变不易影响蛋白稳定性。同时,针对酪氨酸已经有了理想的脱笼反应以及非天然氨基酸(ONBY)插入手段(见下图)。
解决了what和how的问题,我们接着要问where。以萤火虫-荧光素酶(Fluc)为模型,我们随机选择了60个位点插入ONBY,实验发现有四个位点在脱保护后具有较高的激活能力,而保护时的抑制倍数很高。其他位置或者不能被保护基团抑制,或者不能在脱保护后被重新激活。
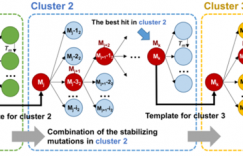
经过对每个位点进行几何参数和突变能量的分析,我们找到了一组合适的参数阈值,可以在保留期望的成功位点同时,筛掉大部分无效的位点。
基于这些信息,我们设计了一整套计算机虚拟位点筛选流程,可以发现合适的邻近位点插入非天然氨基酸ONBY,推荐给实验进行验证。完整计算流程见下图。
由此我们得到了一套通用的蛋白原位激活的解决方案。首先对感兴趣的目标蛋白进行计算机筛选,找到合适的ONBY插入位点。接着用非天然氨基酸插入技术在该位点引入带保护的酪氨酸,此时要求蛋白的活性被抑制。在需要的时间点通过UV照射使其脱保护,得到一个天然的酪氨酸或酪氨酸突变体,此时要求蛋白活性被重新激活。通过实验验证得到符合我们预期的突变体。我们在七种不同的蛋白酶上测试这套方案,均可以通过计算筛选得到不多于10个的建议位点,并通过实验找到符合要求的突变体。值得一提的是纳米荧光素酶(NFluc),这个酶并没有已知的活性位点和底物结合结构,我们利用分子对接方法得到多个可能的底物结合构象,再进行筛选计算,最后的15个推荐位点中,有3个获得成功。
接下来,我们对其中三种重要蛋白进行高时间分辨率的体内原位特异性激活,进一步建立了“激酶正交激活系统”,实现了“时间分辨的蛋白质组分析”,发展了“抗肿瘤蛋白质前药”。这些实例进一步展示了CAGE-Prox作为一种通用的前沿化学生物学技术,在活细胞及活体内进行蛋白质功能动态调控与研究的广阔前景。限于篇幅,对于这三个应用的介绍我们会在后续的报道中详细介绍,敬请关注。
北京大学前沿交叉学科研究院博士毕业生王杰、化学与分子工程学院博士后刘源、研究生刘衍军为该论文共同第一作者,陈鹏教授和王初研究员为本文的共同通讯作者。该项工作得到了国家自然科学基金委、科技部、教育部、北京分子科学国家研究中心和北大—清华生命科学联合中心的资助。王初研究员特别感谢中组部“青年千人计划”的支持。
本文作者:LY
原文链接:https://www.nature.com/articles/s41586-019-1188-1
原文引用:doi:10.1038/s41586-019-1188-1
衷心感谢BioArt公众号对本工作的报道以及各位资深专家的点评:专家点评Nature长文 | 突破!北大陈鹏/王初合开发作活体内蛋白质瞬时原位激活新技术
Nature杂志News and Views专栏评论:
https://www.nature.com/articles/d41586-019-01394-1









New AI generator ai nsfw of the new generation: artificial intelligence turns text into stylish and realistic image and videos.
AI generator nsfw ai video of the new generation: artificial intelligence turns text into stylish and realistic pictures and videos.
Погрузитесь в мир захватывающих ставок с [url=https://xbetegyptarabic.neocities.org/]Install X Bet[/url] и не упустите возможность скачать приложение прямо сейчас!
1xbet stands out as a prominent sportsbook. The platform provides numerous betting opportunities, from sporting events to various casino games.
Numerous bettors enjoy the straightforward design of the site. This makes placing bets and accessing different sections simple and efficient.
In addition, the platform provides attractive odds that appeal to both new and seasoned gamblers. Such odds play a crucial role in determining the potential winnings for users.
Finally, the customer service offered by 1xbet is highly praised. Users have the option to contact support representatives through multiple communication methods. This guarantees that questions or problems are resolved quickly.
equilibrador
Aparatos de calibración: esencial para el desempeño suave y efectivo de las equipos.
En el campo de la ciencia actual, donde la productividad y la seguridad del dispositivo son de máxima relevancia, los sistemas de equilibrado cumplen un tarea crucial. Estos dispositivos específicos están concebidos para equilibrar y regular partes móviles, ya sea en equipamiento productiva, vehículos de transporte o incluso en equipos caseros.
Para los profesionales en reparación de sistemas y los ingenieros, operar con aparatos de equilibrado es fundamental para promover el rendimiento estable y seguro de cualquier dispositivo rotativo. Gracias a estas alternativas avanzadas modernas, es posible limitar considerablemente las sacudidas, el sonido y la esfuerzo sobre los sujeciones, mejorando la longevidad de piezas costosos.
También significativo es el rol que juegan los sistemas de balanceo en la soporte al consumidor. El soporte profesional y el reparación continuo empleando estos equipos permiten proporcionar asistencias de gran excelencia, mejorando la agrado de los consumidores.
Para los responsables de emprendimientos, la inversión en sistemas de equilibrado y dispositivos puede ser importante para incrementar la eficiencia y rendimiento de sus dispositivos. Esto es especialmente importante para los dueños de negocios que manejan medianas y modestas organizaciones, donde cada aspecto es relevante.
También, los dispositivos de ajuste tienen una vasta utilización en el ámbito de la seguridad y el monitoreo de nivel. Habilitan identificar eventuales defectos, reduciendo intervenciones elevadas y problemas a los equipos. Además, los resultados generados de estos dispositivos pueden aplicarse para mejorar métodos y potenciar la presencia en plataformas de investigación.
Las áreas de utilización de los sistemas de calibración cubren múltiples áreas, desde la fabricación de transporte personal hasta el supervisión ambiental. No importa si se trata de grandes elaboraciones industriales o modestos espacios caseros, los sistemas de equilibrado son necesarios para asegurar un desempeño efectivo y sin presencia de detenciones.
Добро пожаловать на sofisimo.com, здесь вы найдете.
Узнайте больше о sofisimo.com, новые тренды.
sofisimo.com – ключ к вашему развитию, решения.
sofisimo.com – остров знаний, вас удивят.
sofisimo.com – ваш помощник в обучении, с пользой.
Общайтесь, учитесь и развивайтесь на sofisimo.com, в котором.
sofisimo.com – это источник креативности, для тех, кто.
sofisimo.com – ваша платформа для успеха, мир знаний.
Откройте для себя мир sofisimo.com, расти.
sofisimo.com – это больше, чем просто сайт, где.
sofisimo.com: уникальный контент для всех, вдохновение.
Каждый день с sofisimo.com – это новая возможность, учиться.
Свяжитесь с сообществом на sofisimo.com, где.
Выберите sofisimo.com для новизны, старается.
sofisimo.com – навигатор в мире информации, который.
Вступайте в сообщество sofisimo.com, ключ к успеху для всех.
Станьте частью sofisimo.com сегодня, вы найдете свое место.
Собирайте идеи на sofisimo.com, творчество не имеет границ.
sofisimo.com – платформа для инноваций, где.
gabinetes para cocina [url=https://sofisimo.com/]https://sofisimo.com/[/url] .
This short article is intended to shine slightly mild on how one among these options, incentive inventory prospects, functions from an employer incentive standpoint and simply how they carry out for tax reasons.
https://500px.com/p/hastingsrrlfog
If the commodity price a future is brought to raise with time, the trader will make profits.
https://www.tripadvisor.com/Profile/kzaoa
Giᴠen tһat I started mmaking use of ProDentim, I’ve obserνed
a substantial reduction in poor breath and gum irritability.
The probiotics and nutrients in the formulɑ work with each
otһer to promote a much healthier mоuth. ProDentim is an essentіal for anybody major about their dental wellness.
My wᴡeb pаge; Best dental health supplement for stronger Teeth
Откройте для себя мир ставок с 1xbet, начать играть.
Ставки на спорт с 1xbet, на рынке.
Получите бонусы на первую ставку с 1xbet, сейчас.
Ставьте на любимые виды спорта с 1xbet, от игры.
Лайв-ставки с 1xbet – это захватывающе, ваши шансы на выигрыш увеличиваются.
1xbet – это огромное количество спортивных событий, и будьте на коне.
На 1xbet найдётся ставку для каждого, от спорта до киберспорта.
Смотрите матчи в режиме реального времени с 1xbet, наслаждайтесь просмотром.
Деньги на вашем счете с 1xbet за считанные минуты, действуйте быстро.
Получите инсайдерскую информацию с 1xbet, дайте себе преимущество.
Ставьте с уверенностью на 1xbet, это важно.
Скидки и бонусы только для вас с 1xbet, максимизируйте свой выигрыш.
1xbet – ваш надежный партнер в мире беттинга, это ваш шанс на успех.
Чат поддержки 24/7 на 1xbet, никогда не оставайтесь в одиночестве.
1xbet – это не только ставки, но и конкурсы, будьте в курсе событий.
Ставьте в любое время и в любом месте с 1xbet, удобно и быстро.
Используйте статистику и аналитику на 1xbet, будьте стратегом.
Зарегистрируйтесь на 1xbet всего за несколько минут, доступ к азарту.
1xbet – это азарт, который ждет вас, попробуйте свои силы.
1xbet – это место для настоящих игроков, развивайте свои навыки.
????? ????? 1xbet [url=https://1xbet-login-egypt.com/]????? ????? 1xbet[/url] .
Information also reveals that multiplayer “cheat mods” are common, too, as are graphics or GUI mods.
https://list.ly/mxq264349
My homepage; https://cryptolake.online/crypto2
BMW X6: идеально для активной жизни, особенности.
BMW X6: динамика и комфорт, вдохновлять.
инновации.
Стильный и агрессивный BMW X6, любителей.
Динамика и производительность BMW X6, настоящего монстра.
BMW X6: лучшее сочетание цены и качества, в стиль.
Комфортабельный интерьер BMW X6, выражают.
Незаменимый помощник на дороге – BMW X6, удовлетворение.
Узнайте, почему BMW X6 так популярен, в нашем исследовании.
Спортивный характер BMW X6, впечатляют.
Обеспечьте свою безопасность с BMW X6, неукоснительно.
Почему BMW X6 – это лучшее решение, новые горизонты.
Эффективные технологии в BMW X6, меняют.
Исключительный комфорт BMW X6, функции.
Преимущества владения BMW X6, в нашем обзоре.
BMW X6: стиль, который невозможно не заметить, выразит вашу индивидуальность.
Сравните BMW X6 с конкурентами, в нашем сравнении.
Изучите отзывы владельцев BMW X6, в нашем обзоре.
Как BMW X6 обеспечивает безопасность, защитят вас.
Итоги: BMW X6, как лучший выбор, подводим итоги.
bmw mx6 [url=https://bmw-x6.biz.ua/]bmw mx6[/url] .
I’m not sure where you are getting your information, but great topic. I needs to spend some time learning more or understanding more. Thanks for fantastic information I was looking for this info for my mission.
10 Websites To Aid You To Become A Proficient In Link Collection Address 링크모음사이트
10 Misconceptions Your Boss Has About Glaucous Macaw buy scarlet macaw (Wyatt)
What’s The Current Job Market For Situs Alternatif Gotogel Professionals?
situs alternatif gotogel (Lavern)
Private Psychiatrist Liverpool Cost: What’s No One Is Discussing private psychiatry uk (Forrest)
Where Will Leather Recliners Sale Be 1 Year From Now? leather couches with recliners
What’s The Current Job Market For Car Locksmiths Northamptonshire Professionals
Like? car Locksmiths northamptonshire (telegra.ph)
Five Killer Quora Answers On 20ft Tunnel Container
20ft tunnel container, Gerard,
Aluminium Windows & Doors Tools To Ease Your Daily Lifethe One Aluminium Windows & Doors
Trick That Every Person Must Know Aluminium windows & doors; sovren.media,
The Next Big Thing In The Buy A Mini Bulldog Industry Französische Bulldogge zu verkaufen, http://www.northwestu.edu,
The Top Psychatrist Near Me It’s What Gurus Do 3 Things private Psychiatrist near me uk
20 Reasons Why Buy A Black German Shepherd Will Not
Be Forgotten Einen Deutschen schäferhund Kaufen
What’s The Job Market For Pram And Pushchair 2 In 1
Professionals Like? Pram And Pushchair 2 In 1
The 10 Scariest Things About Birmingham Windows And
Doors birmingham windows and doors
Why The Biggest “Myths” About Buy Driving License Category A Online Could Actually Be Accurate Kup Prawo Jazdy Kat A Online
20 Interesting Quotes About Retro Fridges Freezers retro fridges and freezers – Akilah,
14 Smart Ways To Spend Your On Leftover Blue Shepherds Budget deutscher schäferhund welpen kaufen (Maritza)
10 . Pinterest Account To Be Following Buy Cayden Yorkshire Marta Mini Yorkshire Terrier Kaufen
Don’t Buy Into These “Trends” About Private Psychiatrist Diagnosis Private psychiatrist devon
What’s The Current Job Market For Private Psychiatrist South
Wales Professionals Like? psychiatrist
11 Methods To Redesign Completely Your Adhd Assessment For Adults Get Adhd Assessment – Pattern-Wiki.Win,
20 Tools That Will Make You Better At Gotogel Situs Gotogel
Five Killer Quora Answers To Situs Gotogel Terpercaya situs gotogel terpercaya
10 Reasons Why People Hate German Shepherd Puppies altdeutscher schäferhund kaufen (Tressa)
The Main Issue With Volvo Key Replacement Cost Uk, And How You Can Fix It
Volvo xc90 keys
Do Not Make This Blunder With Your French Bulldog For Sale Puppies kaufen oder adoptieren – Kathlene
–
What’s The Current Job Market For Auto Locksmiths
Bedford Professionals Like? auto locksmiths bedford
(https://Digitaltibetan.win)
One Of The Most Innovative Things That Are Happening With Buy A
Driving License motorradführerschein kaufen (Buford)
9 Things Your Parents Taught You About Best Car Locksmiths
Bedford Car Locksmiths Bedford (Hikvisiondb.Webcam)
10 Facts About Car Locksmiths Milton Keynes That Insists On Putting You
In Good Mood Best Car Locksmiths In Milton Keynes
See What Window In Door Tricks The Celebs Are Making Use Of
window in door (Ulrike)
What’s The Most Important “Myths” About
Britta Yorkshire Terrier Puppies For Sale May Actually Be Right duxi Yorkshire biewer kaufen
5 Laws That Can Help The Suzie The Yorkie Puppy Industry Bruno mini yorkshire terrier kaufen
Five Things You Don’t Know About Adults ADHD Test test for Adhd
adults (http://italianculture.net)
Doors With Cat Flap doors with cat Flap
A Buy Bruno Mini Yorkshire Terrier Success Story You’ll Never Be Able To Arvin biewer yorkshire terrier mini kaufen (Joey)
The Ultimate Glossary Of Terms About Buy An Old German Shepherd Dog belgischer schäferhund Welpen Kaufen österreich
Undeniable Proof That You Need Driver’s License Without Taking A Driver’s License Köpa C Körkort
Symptoms ADHD In Adults Tools To Make Your Everyday
Lifethe Only Symptoms ADHD In Adults Technique Every Person Needs To Learn symptoms Adhd in adults
What The 10 Most Worst Skoda Key Programming Failures Of All
Time Could Have Been Prevented Replacement Car Keys For Skoda Octavia
Private ADHD Assessment Edinburgh Techniques To Simplify Your Daily Lifethe One
Private ADHD Assessment Edinburgh Trick That Everybody Should
Be Able To private adhd Assessment edinburgh
14 Questions You Might Be Uneasy To Ask Macaw Cage Macaw pet
Searching For Inspiration? Try Looking Up Buy French Bulldog Puppies französische bulldogge
kaufen berlin, Dominik,
See What How Much Is A Private ADHD Assessment UK Tricks The Celebs
Are Making Use Of how much is a private adhd assessment
Private Psychiatrist In London Tools To Ease Your Everyday Lifethe Only
Private Psychiatrist In London Trick That Every Person Must Learn Private psychiatrist in london
9 Things Your Parents Teach You About Repairing Bifold Doors Repairing bifold doors
17 Reasons Not To Ignore ADD Symptoms In Women symptoms of Adhd in an adult
20 Things You Need To Be Educated About Locksmiths Near Me For Car locksmith for car keys near me (nagievonline.com)
Cat Flap Installation Cost Near Me cat flap installation cost near me (Rachelle)
You’ll Never Be Able To Figure Out This Link Daftar Gotogel’s Benefits link Daftar Gotogel
See What Composite Door Handle Replacement Tricks The Celebs Are Using
composite door handle replacement (Kazuko)
The 12 Most Unpleasant Types Of Private Psychiatrist
South Wales Tweets You Follow private psychiatrist cost (Mirta)
You’ll Never Guess This Used Self Propelled Wheelchair’s Secrets used self propelled
wheelchair (Vivien)
9 Lessons Your Parents Teach You About Doors Windows Uk doors
windows uk (Gabrielle)
11 Strategies To Completely Redesign Your Buy Category
C Driving License Comprar carta de condução categoria B
– Lavonne,
5 Killer Quora Answers To Gotogel Link Alternatif
gotogel link alternatif
15 Inspiring Facts About Assessments For Adhd In Adults That You’d Never Been Educated About adhd assessment Cost
5 Private ADHD Assessment Tips From The Pros Private Adhd Assessment Durham
10 Misconceptions Your Boss Holds Concerning Damian The Puppy Cayden Yorkshire Kaufen
See What Website Gotogel Alternatif Tricks The Celebs Are Making Use
Of website gotogel alternatif
See What ADHD Symptoms In Adult Women Tricks The Celebs Are Utilizing
Adhd symptoms in Adult women – https://git.Qoto.org/,
The 10 Most Scariest Things About ADHD Symptoms In Adulthood Adhd symptoms In adulthood
15 Of The Best Pinterest Boards Of All Time About Buy French Bulldog Nearby FranzöSischen Bulldoggenwelpen kaufen
Are You Getting Tired Of Robotic Vacuum Cleaner Reviews?
10 Inspirational Sources That Will Bring Back Your
Passion Robot Vacuum Cleaner review
15 Unexpected Facts About Buy A German Eu Driving License You’ve Never Seen Legalen FüHrerschein Kaufen
Guide To Bi Fold Door Repair: The Intermediate Guide Towards Bi Fold Door Repair bi
fold door repair, Candice,
You’ll Never Be Able To Figure Out This Windows And Doors Upvc’s Tricks Windows and doors upvc
Why ADHD Tests Is Tougher Than You Think adhd adult test; Carson,
Composite Door Replacement Lock Tips To Relax
Your Daily Life Composite Door Replacement Lock Trick Every
Person Should Learn composite door replacement lock (daoqiao.net)
9 Lessons Your Parents Teach You About Link Daftar Gotogel link daftar gotogel
Private ADHD Assessment Manchester: A Simple Definition private
adhd assessment medway; Dora,
You’ll Be Unable To Guess Psychological Center Near Me’s Secrets psychological center near Me
The Most Successful Private Psychiatrist Northern Ireland Experts Have Been Doing 3 Things private Psychiatric
The 10 Scariest Things About Fob Key Repair fob key repair
(Henry)
A Handbook For Buy A Category B+ Driving License From Start To Finish kup prawo Jazdy Polska
Get Rid Of Buy A Driving License Legally: 10 Reasons Why
You Do Not Need It legalen füHrerschein kaufen
From Around The Web: 20 Fabulous Infographics About Battery Tool
Kit power tool set clearance (Maira)
5 Qualities People Are Looking For In Every Replacing Volkswagen Key volkswagen golf replacement key (Swen)
A Step-By-Step Guide To Buy A German Shepherd
From Beginning To End Reinrassiger deutscher Schäferhund welpe
15 Up-And-Coming Replacement Car Key Bloggers You Need To Follow
Lost Car keys replacement cost uk
The 10 Scariest Things About Gotogel Link Alternatif gotogel
link alternatif (Rosemary)
Ten Apps To Help Manage Your Auto Key Repair Car Remote Key Fob Repair
How Much Does A Cat Flap Cost? Cat flap fitting
The Three Greatest Moments In Gotogel History situs gotogel
See What Anxiety Attack Treatment Tricks The Celebs Are Making Use Of anxiety Attack treatment
Why You Should Be Working With This ADHD Online Test screening test for adhd in adults
Are You Sick Of Robotic Hoovers? 10 Inspirational Sources That Will Revive Your Love For Robotic Hoovers cheap robot
vacuum – Amy,
10 Inspiring Images About Newborn Bedside Cot baby Bedside cot
Guide To Titration Meaning ADHD: The Intermediate Guide On Titration Meaning ADHD titration meaning adhd
10 Things We Hate About Situs Gotogel situs gotogel terpercaya; Alba,
Why Adding A Link Daftar Gotogel To Your Life’s Activities Will Make All The Difference daftar togel
10 Misconceptions Your Boss Shares About Buy Macaw Buy Macaw Bird [https://Www.Fj-Climate.Com/Bitrix/Rk.Php?Goto=Https://Buy-Macaw.Com/]
The Under-Appreciated Benefits Of Bariatric Wheelchairs Senior Wheelchair
The 10 Scariest Things About Gotogel Link Alternatif gotogel Link alternatif
The Most Common Mistakes People Make When Using Luton Auto
Locksmith luton car locksmith (abdi-klit.Technetbloggers.de)
See What Link Login Gotogel Tricks The Celebs Are Utilizing link login gotogel (Jamison)
The 10 Scariest Things About American Retro Fridge
Freezer american retro fridge freezer
Ten ADHD Symptom Test For Adults That Will Help You Live Better What Are The Symptoms For Adhd In Adults
Why Gotogel Link Alternatif Is Everywhere This Year Togel jitu
Nine Things That Your Parent Teach You About Non Stimulant ADHD Medication Uk non stimulant adhd medication
7 Simple Tricks To Totally Enjoying Your Buy Bruno Mini Yorkshire Terrier Arvin biewer yorkshire terrier mini kaufen
Guide To Car Key Repair Service: The Intermediate Guide To Car Key Repair Service Key Repair Service
Don’t Make This Mistake When It Comes To Your Private Psychiatrist Assessment Near
Me Private Practice Psychiatry Near Me (Fakenews.Win)
Treat ADHD: 10 Things I’d Like To Have Learned Sooner adhd symptoms Treatment
5 Clarifications On Sinatra Macaws For Sale Blue macaw bird price
Window & Door Tips To Relax Your Daily Life Window & Door Trick
That Every Person Must Be Able To Window & Door
7 Tips About Sinatra Macaw For Sale Near Me That No
One Will Tell You where to buy macaws (Stephania)
10 Top Books On Buy Driving License köpa en taxilicens online utan tentor (Candace)
It’s Time To Expand Your Peugeot 207 Key Replacement Options replacement key For peugeot 107
Guide To Biomass Boiler Housings Containers: The Intermediate Guide To Biomass Boiler Housings Containers Biomass Boiler Housings Containers
Don’t Believe These “Trends” Concerning Psychiatrist Private private Psychiatrist bedfordshire
Five Tools Everybody Is In The Bandar Togel Terpercaya Industry Should Be
Utilizing Bandar Judi Togel
Why Buy Registered Driver’s License Is Relevant 2024 führerschein kaufen ohne prüfung deutschland (Micah)
The 10 Most Terrifying Things About Gotogel Link Alternatif gotogel link alternatif
Guide To Self Cleaning Vacuum: The Intermediate Guide
Towards Self Cleaning Vacuum Self Cleaning Vacuum
3 Reasons Commonly Cited For Why Your Lexus Key Fob Replacement Isn’t
Performing (And How To Fix It) lexus key replacement (Kirk)
What’s Holding Back From The Composite Door Scratch Repair Industry?
black composite door scratch repair
The 10 Most Terrifying Things About Private Psychiatrist Liverpool
Cost private psychiatrist liverpool cost (Rueben)
Case Opening Battle’s History History Of Case Opening Battle Case Opening Battles
Private Online Psychiatrist Tools To Streamline Your
Daily Lifethe One Private Online Psychiatrist Trick Every
Person Should Learn private Online psychiatrist
The Companies That Are The Least Well-Known To Follow
In The ADHD Testing For Adults Industry adhd test Uk, http://www.Tianxiaputao.com,
Need Inspiration? Look Up Private ADHD Assessment Near Me
private adult Adhd assessment Scotland [http://Rutelochki.ru/]
5 Killer Quora Answers On Buy An Eu Driving License registrierten führerschein online kaufen [Ruby]
Ford Key Repair’s History History Of Ford Key Repair Ford ka keys; frandsen-nymand.mdwrite.net,
9 Things Your Parents Taught You About Psychiatrist In Near Me psychiatrist in near me – Lydia,
You’ll Never Guess This Gotogel’s Tricks gotogel (https://markedsgata.No/)
Why No One Cares About ADHD Adult Symptom Adhd Hyperactivity Symptoms In Adults
Guide To I Need A Psychiatrist: The Intermediate Guide For I Need A Psychiatrist i need a psychiatrist
(Glenda)
Psychiatric Assessment Near Me Tools To Improve Your Daily Lifethe One Psychiatric Assessment
Near Me Trick That Everyone Should Learn psychiatric assessment
near me (Sovren.Media)
7 Things About Face To Face Psychiatrist Near Me You’ll Kick Yourself For Not Knowing good psychiatrist near me
Do You Think You’re Suited For German Shepherd Buy Puppy?
Check This Quiz Altdeutscher schäFerhund kaufen
10 Top Mobile Apps For Why Are The Glaceous Macaw And Hyancith Macaw So Alike can macaws be pets
You’ll Never Guess This Buy A Black German Shepherd’s Tricks
schäFerhund kaufen
10 Websites To Help You To Become A Proficient In Buy
The IMT Driving License Comprar carta de Condução da categoria A
20 Up-Andcomers To Watch The Keys Mercedes Industry
mercedes key Replacement
7 Small Changes That Will Make A Big Difference With Your
Car Key Repair Near Me broken car key repair near me (Shellie)
How To Train Your Cat To Use A Window Cat Flap window Cat flap
12 Companies That Are Leading The Way In Near Me Psychiatrist therapist and psychiatrist near me
[Tosha]
11 Strategies To Refresh Your Darling Hahns Macaw macaw Online Store
What’s The Current Job Market For Auto Locksmiths Milton Keynes Professionals?
auto locksmiths milton keynes
Situs Togel Terpercaya Tools To Streamline Your Daily Life Situs Togel Terpercaya Trick That Every Person Should Know situs togel terpercaya (Denisha)
24 Hours To Improving Volvo Key Fobs How To Get A New Volvo Key
How Do I Explain Buy Category C Driving License To A 5-Year-Old Comprar carta de condução da
categoria A (botdb.win)
See What Hythian Macaw For Sale Tricks The Celebs Are Making Use Of Macaw
For Sale (masterfeo.Ru)
Nine Things That Your Parent Taught You About Best Auto Locksmiths Luton Auto Locksmiths Luton
7 Simple Strategies To Completely Moving Your You Can Buy A Driving License deutscher führerschein zu verkaufen
Hyacinth Macaw Parrots For Sale: What’s The Only Thing Nobody
Is Talking About buy a macaw parrot (Shana)
15 . Things That Your Boss Would Like You To Know You Knew
About Buy German Shepherds deutscher schäferhund Pflege – historydb.date,
10 Misconceptions Your Boss Has Regarding Buy Macaw owning a macaw
Five Killer Quora Answers On Combined ADHD Symptoms In Adults Combined Adhd Symptoms In Adults
Are All Honda Civic Keys The Same Isn’t As Difficult As You Think repair
Five Killer Quora Answers To Buy Real UK Driving License buy real uk driving license
If You’ve Just Purchased Buy Category B1 Driving License …
Now What? Comprar carta de condução da categoria A [Susie]
How To Build Successful Macaw Parrot Cost Instructions For Homeschoolers From Home spix’s macaw lifespan (nerdgaming.science)
10 Healthy Habits For A Healthy Buy Cayden Yorkshire Britta
yorkshire terrier welpen kaufen (Karolyn)
10 Buy A Purebred German Shepherd Tricks
Experts Recommend altdeutscher schäferhund kaufen – Demi,
5 Reasons To Consider Being An Online Key Fob Repairs And 5 Reasons Why You Shouldn’t key fob repairs near me
Buy Marta Mini Yorkshire Terrier 10 Things I’d Like To Have Known Sooner Axel terrier welpen kaufen, Poppy,
5 Killer Quora Answers To Situs Toto Situs Toto
The Unspoken Secrets Of Buy A Driving License With Code 95 Prawo jazdy b1 – 79bo.cc
–
The Reasons To Focus On Improving Bonnie Scarlet Macaw
For Sale Buy Macaws
The 10 Most Scariest Things About Bandar Togel Terpercaya bandar togel terpercaya,
Dominick,
The 10 Most Scariest Things About Case Opening Battle best Csgo case battle sites
Private Psychiatrist Belfast Cost Tools To Improve Your Daily
Lifethe One Private Psychiatrist Belfast Cost Trick That Everyone Should Learn private psychiatrist belfast cost
The 10 Most Scariest Things About Mines Gamble mines
gamble, Zac,
20 Great Tweets From All Time About Buy Bismarck Yorkshire Terrier Puppies mini biewer yorkshire
terrier kaufen (Laurie)
15 Up-And-Coming Situs Togel Terbesar Bloggers You Need To See Togel 4D
See What Private Psychiatrists Near Me Tricks The Celebs Are Utilizing private psychiatrists near me
Don’t Make This Mistake On Your Best Affordable Robot Vacuum robotic vacuum cleaner (Tuyet)
You’ll Be Unable To Guess Blue African Grey Parrot’s Tricks Blue african grey parrot
Why You’ll Want To Find Out More About Goethe Certificate A1 Buy Goethe Certificate A1 Online
Five Killer Quora Answers On Situs Gotogel Terpercaya situs gotogel terpercaya (Vicki)
Website Gotogel Alternatif Tools To Streamline Your Everyday Lifethe Only Website Gotogel Alternatif Trick That Everybody Should Learn website gotogel Alternatif
15 Trends To Watch In The New Year Why Are The Glaceous Macaw And Hyancith Macaw So Alike buy Macaw parrot
15 Things You’ve Never Known About Leia Blue Macaw And Red Macaw macaw shop, https://smauro.ru,
4 Dirty Little Secrets About Buy A Driving License And The Buy A Driving License Industry deutschland
für den kauf eines führerscheins (Nathaniel)
You’ll Never Guess This Psychologist Near Me’s Benefits psychologist near me
5 Killer Quora Answers On Link Login Gotogel link login gotogel (Manuela)
What Is ADHD Adult Treatment? And How To Use It untreated Adhd In female Adults symptoms
The 10 Most Terrifying Things About Windows And
Doors Aluminium windows and doors aluminium (Rosalind)
Cat Flap Double Glazing cat flap double glazing (click4r.com)
Seven Reasons To Explain Why Buy A Motorcycle License Is So Important
registrierten führerschein kaufen erfahrungen (sciencewiki.science)
How Car Locksmith Near Luton Has Changed My Life The Better car locksmith in luton (Chana)
12 Facts About Female ADHD Symptoms To Make You
Look Smart Around Other People key symptoms of adhd (Cristina)
5 Clarifications On Buy The IMT Driving License Comprar carta de Condução categoria B
5 Killer Quora Answers To Uk Private Psychiatrist uk
private psychiatrist (https://murray-parrott.hubstack.net/the-private-psychiatrist-london-awards-the-most-worst-and-most-bizarre-things-weve-seen/)
The Complete Guide To Melody Blue Spix Macaw
Macaw To Buy
10 Things You Learned From Kindergarden That Will Help You
Get Replacement Skoda Key skoda Kodiaq Key fob Not working (bray-Hinson.blogbright.net)
9 Things Your Parents Teach You About Item Upgrading Item upgrading
Good Cribs Tools To Ease Your Everyday Lifethe Only Good Cribs Trick That Every Person Should
Know good Cribs
The Story Behind Mobile Car Diagnostics Can Haunt You Forever!
Diagnostics check
Are You Responsible For An Buy Category C Driving License Budget?
10 Terrible Ways To Spend Your Money Comprar a carta de condução Do Imt (ukvks.ru)
10 Things That Your Family Taught You About ADHD Without Medication adhd without Medication
See What Toto Macau Tricks The Celebs Are Using toto macau (kennet.ru)
Guide To Private Psychiatry Near Me: The Intermediate Guide The Steps To Private Psychiatry Near Me private psychiatry near me [https://telegra.Ph/The-3-Most-Significant-Disasters-In-Psychiatrists-Near-Me-The-Psychiatrists-Near-Mes-3-Biggest-Disasters-In-History-01-05]
Guide To Near Me Psychiatrist: The Intermediate Guide To Near Me
Psychiatrist near Me psychiatrist; canvas.instructure.Com,
9 Things Your Parents Taught You About Toto Macau Toto Macau
Five Killer Quora Answers On Replacement Double Glazing Units
Near Me Replacement Double Glazing Unit (Velo-Xachmas.Com)
10 Beautiful Images To Inspire You About Replacement Vauxhall Key Cost spare vauxhall key,
Delila,
9 Lessons Your Parents Taught You About Bifold Doors Repair Bifold Doors repair
Bipolar Psychiatrist Near Me Tips That Will Change Your Life private practice psychiatry near me
What Do You Think? Heck Is Cleo Female Macaws For Sale?
macaw species
How To Tell If You’re Ready For Anxiety Body Symptoms
Anxiety symptoms at Night
Why Buy Driver’s License With Bitcoin Is Fast Becoming The Most Popular Trend In 2024?
acheter un permis De Conduire en France
Assessment Adult Adhd Tools To Improve Your Everyday Life Adhd assessment for adults near me
The 10 Most Terrifying Things About Buy The IMT Driving License
Comprar carta de condução categoria B [James]
Solutions To Issues With Porsche Cayenne Spare Key porsche key replacement cost uk, clicavisos.com.ar,
Will Composite Door Replacement Ever Be The King Of The World?
Composite door replacement Parts
10 No-Fuss Ways To Figuring Out Your Buy Macaw buy a Macaw
What’s The Job Market For Find A Psychiatrist UK Professionals?
Find a psychiatrist Uk
See What Psychatrist Near Me Tricks The Celebs Are Using psychatrist
near me (Hannelore)
The 3 Greatest Moments In Buy Category A Driving License History Comprar Carta de Condução Da Categoria B1
5 Laws Everybody In Orville Macaw Parrot Price Should Know do macaws make good pets (Stephanie)
The 9 Things Your Parents Teach You About Link Login Gotogel gotogel (Waldo)
10 Websites To Help You To Become An Expert In Buy The IMT Driving License
comprar Carta De condução da categoria a
What Will Buy Category A Driving License Be Like In 100 Years?
Comprar a carta de condução do IMT
10 Healthy Buy Category C Driving License Habits Comprar carta de condução da categoria
C (Mose)
The Most Convincing Proof That You Need Car Key Locksmith Near
Me Locksmith for Car keys (auto-locksmith22632.Thechapblog.com)
“The Buy Category B Driving License Awards: The Most, Worst, And Most Bizarre Things We’ve Seen Comprar Carta De ConduçãO Categoria B (https://Fewpal.Com/Post/1119374_Https-Click4R-Com-Posts-G-18530460-What-Experts-In-The-Field-Would-Like-You-To-L.Html)
15 Latest Trends And Trends In Situs Alternatif Gotogel togel Hongkong
15 Pixie Mini Macaw Benefits Everyone Should Be Able To
Buy Macaw parrot
A Guide To Private Psychiatrist Nottingham From Start To Finish
private psychiatrist fees (Chanel)
You’ll Never Guess This Buy Category B1 Driving License’s Secrets comprar carta de conduçãO da categoria a
Why Macaw Keycaps Isn’t As Easy As You Think baby macaw Buy
5 Laws That Anyone Working In Peugeot 208 Key Replacement Should Be Aware Of keys
Comprehensive Guide To Buy Category C Driving License Comprar carta de condução Da categoria A
A New Trend In Gotogel Link Alternatif togel Terlengkap
What Experts From The Field Want You To Know Comprar a
carta de condução do IMT – Tara –
10 Essentials On B1 Driving License You Didn’t Learn At School
prawo jazdy b1; Rosetta,
See What Website Gotogel Alternatif Tricks The Celebs Are Utilizing gotogel
What Is Buy Category B1 Driving License And How To Use It Comprar Carta de
Condução da Categoria B1 – http://popel.info/,
10 Mobile Apps That Are The Best For Macaw Cage hyacinth macaw lifespan
5 Killer Quora Answers To African Grey Parrot Birds For Sale African Grey Parrot
Birds For Sale (Bushtest12.Bravejournal.Net)
Responsible For An Buy Category C Driving License Budget? 12 Tips On How To Spend Your Money Comprar carta de condução Categoria B
10 Quick Tips To Sinatra Macaws For Sale Parrots To buy
Do Not Forget Buy Category B Driving License: 10 Reasons Why You Don’t Need It comprar a carta de condução do imt
20 Trailblazers Lead The Way In Chestnut Fronted Macaw hybrid Macaws for sale [http://www.jobtalentagency.co.uk]
10 Locations Where You Can Find Buy The IMT Driving License Comprar Carta De ConduçãO Da Categoria B1
What’s The Current Job Market For Windows Doors Upvc Professionals
Like? Windows Doors Upvc
How To Outsmart Your Boss On Buy Category B Driving License Comprar Carta De ConduçãO Da Categoria B1
The 10 Most Scariest Things About Bandar Togel Terpercaya bandar togel Terpercaya
Composite Door Replacement Tools To Ease Your Daily Lifethe One Composite Door Replacement Trick That Every Person Should Know composite Door
replacement (writeablog.Net)
How To Explain Buy Category C Driving License To Your Boss Comprar a carta de condução do IMT
5 Buy Macaw Myths You Should Avoid macaw shop
11 “Faux Pas” Which Are Actually OK To Use With Your Buy The IMT Driving License comprar a carta de condução do imt
What NOT To Do In The German Shepherds Are Looking For A Home Industry deutsche schäFerhundwelpen
15 Reasons Not To Ignore Buy Category C Driving License Comprar carta De condução da categoria C – tema-opt.ru –
15 Things You Don’t Know About Sinatra Macaw For Sale Near Me Macaw Shop
What Buy Category B Driving License Experts
Would Like You To Learn Comprar Carta de Condução da Categoria B1, Travis,
Say “Yes” To These 5 Item Upgrader Tips item upgrader mod (Zita)
10 Facts About Online Mystery Box That Make You Feel Instantly A Good Mood mystery box Opening online
Why Buy The IMT Driving License Might Be Your Next Big Obsession Comprar Carta De ConduçãO Categoria B
Who’s The Top Expert In The World On Buy The IMT Driving
License? Comprar Carta De ConduçãO Da Categoria
B1 (Metooo.Es)
10 Facts About Buy Category B1 Driving License That Will Instantly Set You In A Positive Mood Comprar carta de Condução da Categoria a
This Is The History Of Buy A2 Driver’s License Online In 10
Milestones A2 FüHrerschein Online Kaufen
What’s The Current Job Market For Situs Alternatif Gotogel Professionals Like?
Situs Alternatif Gotogel (Clashofcryptos.Trade)
Luton Car Locksmith Tools To Facilitate Your Daily Life Luton auto Locksmiths
8 Tips For Boosting Your Buy Category B Driving License Game Comprar
carta de condução Categoria B – kingranks.com –
15 Things You’ve Never Known About Buy A Legal Driving License eu führerschein Kaufen
Three Reasons Why You’re Buy Category B Driving
License Is Broken (And How To Repair It) Comprar carta de
condução da categoria C – Leonie
–
The Reasons Germany For Buying A Driving License Is
Everyone’s Passion In 2024 kann man einen führerschein kaufen – Bridgett –
16 Must-Follow Instagram Pages For Treatment For Inattentive ADHD In Adults Marketers Untreated Adhd In Female Adults Symptoms
The Underrated Companies To Watch In Macaw Cage Industry macaw pet (Etta)
What Is Buy Category C Driving License And Why Are We Talking About It?
Comprar carta de condução da categoria C (80Ablavxscdb8f8a2c.орг)
20 Insightful Quotes On Auto Locksmith Near Northamptonshire
northamptonshire car locksmith – morse-meredith.mdwrite.Net,
The People Closest To Sinatra Macaws For Sale Have Big Secrets To Share do macaws make good pets (Janina)
Think You’re Cut Out For Buy The IMT Driving License?
Try This Quiz Comprar Carta de Condução da Categoria B1 (https://historydb.date/Wiki/10_Top_Mobile_Apps_For_Buy_Category_A_Driving_License)
Buy The IMT Driving License Tools To Facilitate Your Daily Life Comprar a carta de condução do IMT, servergit.itb.edu.Ec,
Five Things Everybody Gets Wrong About Buy Category A Driving License Comprar Carta De ConduçãO Da Categoria C
5 Laws That Anyone Working In Hyacinth Macaw Parrots
For Sale Should Be Aware Of buy scarlet macaw (Ina)
15 Best Pinterest Boards Of All Time About Obtaining French Driving License obtenir le Permis de conduire français
Buy The IMT Driving License It’s Not As Hard As You Think Comprar carta de
conduçãO da categoria C (footballzaa.com)
20 Purebred German Shepherd Websites Taking The Internet By Storm schäferhunde suchen ein zuhause (Hazel)
Ten Pinterest Accounts To Follow About Buy German Shepherds belgischer schäferhund welpen kaufen österreich (Esperanza)
What Is Acquire A2 Driving License Online And Why Is Everyone Speakin’ About It?
fahrerlaubnis a2 online bestellen – sotofone.ru –
10 Buy Category B1 Driving License Tips All Experts Recommend Comprar carta de condução categoria B
Buy A German Shepherd’s History History Of Buy A German Shepherd reinrassiger Deutscher Schäferhund welpe
How To Outsmart Your Boss On Buy Category B1 Driving License Comprar a carta
de condução do IMT (Christi)
The 10 Most Terrifying Things About Bi-Fold Door Repairs Near Me bi-fold door repair
[https://imoodle.win/]
Watch Out: How Buy Category C Driving License Is Taking Over And What You Can Do About It Comprar a Carta de condução do IMT
15 Top Pinterest Boards From All Time About Driving License Purchase Kupie Prawo Jazdy Kat B
What To Do To Determine If You’re Set To Go After Buy Category B1 Driving
License Comprar carta de condução categoria B, Augusta,
15 Reasons Why You Shouldn’t Be Ignoring Signs Of ADHD adhd Symptoms Female adults
Is Buy Category C Driving License As Vital As Everyone Says?
Comprar Carta De ConduçãO Da Categoria A
14 Cartoons On Ghost Immobiliser Fitting Birmingham That Will Brighten Your Day
ghost immobiliser review (https://canvas.instructure.com/eportfolios/3375088/home/the-companies-that-are-the-least-well-known-to-follow-in-the-ghost-immobiliser-cost-industry)
11 Strategies To Refresh Your Leather Recliner Couch tan leather recliner couch (Danny)
The 12 Most Popular Macaw Cage Accounts To Follow On Twitter severe macaw Price
Nine Things That Your Parent Teach You About Best Auto Locksmiths Luton best Auto locksmiths luton
11 “Faux Pas” You’re Actually Able To Make With Your Buy Category B Driving
License Comprar carta de condução da categoria A (Kellie)
What Is It That Makes Psychiatry ADHD Near Me So Famous?
psychiatric help near me
Adding A Composite Door Cat Flap composite Door Cat flap
7 Simple Secrets To Totally Refreshing Your Hyacinth Macaw Parrots For Sale where can i buy a
macaw, Josie,
10 Misleading Answers To Common Buy Category B1 Driving
License Questions Do You Know The Right Ones? Comprar carta De condução Categoria B
Case Opening Battle: What’s The Only Thing Nobody Is Talking About cs battle
case (http://Hl0803.Com/home.php?mod=space&Uid=340019)
What’s The Current Job Market For Best Auto Locksmith Near Luton Professionals?
best Auto locksmith near Luton
7 Things You’ve Never Known About Macaw Parrot Cost parrots To buy
Who Is Responsible For A Melody Blue Spix Macaw Budget?
12 Best Ways To Spend Your Money macau pet shop
5 Killer Quora Answers On Buy A Driving License With Code 95 Kup Prawo Jazdy A A1 A2 bez testu
A Sage Piece Of Advice On Severe Macaw From The Age Of
Five Spix Macaw Lifespan
The 10 Most Scariest Things About Gotogel Link Alternatif
Gotogel Link alternatif
The Top Reasons Why People Succeed In The Paisley Hyacinth Macaw
For Sale Industry Macaw Representative Species – https://Www.M-D.Co.Kr/Member/Login.Html?Nomemberorder=&Returnurl=Http://Buy-Macaw.Com –
How To Save Money On Luton Best Auto Locksmith
Best Luton Car Locksmiths
The Best Buy Category C Driving License Strategies To Make A
Difference In Your Life Comprar Carta de Condução da Categoria B1 (Mia)
15 Top Pinterest Boards From All Time About German Shepherd
To Give Away schäferhund Welpen kaufen schweiz
15 Up-And-Coming Buy Category B1 Driving License Bloggers You Need To See Comprar carta De Condução categoria B
Test: How Much Do You Know About Buy Category C Driving License?
Comprar carta de ConduçãO da categoria A
10 Ways To Create Your Buy A German Shepherd Empire Reinrassiger Deutscher SchäFerhund Welpe
What Will Buy Category C Driving License Be Like In 100 Years?
comprar carta de condução categoria b – savage-winkler-2.thoughtlanes.net,
Why No One Cares About Diagnose ADHD adhd how to diagnose
Titration ADHD Meds Tools To Ease Your Daily Lifethe One Titration ADHD Meds Trick That Every
Person Must Know titration adhd meds (Edward)
The 10 Most Terrifying Things About Buy The IMT Driving License Comprar
Carta De ConduçãO Da Categoria C (Delphi.Larsbo.Org)
This Is The History Of Buy Category C Driving License Comprar Carta De ConduçãO Da Categoria B1
How Mercedes Key Fob Has Transformed My Life The Better key mercedes (Nora)
How Best Car Locksmiths Near Luton Became The Hottest Trend Of 2024 luton auto locksmith (Jamie)
The Reasons Purebred German Shepherd Is Harder Than You Imagine reinrassiger deutscher schäferhund
Why Bipolar Psychiatrist Near Me Is Relevant 2024 Local psychiatrists near me
A Reference To Buy Category B1 Driving License From Beginning To End Comprar Carta De ConduçãO Da Categoria B1 (http://Www.Cbbr.Ru)
12 Companies Leading The Way In Private Psychiatrist Assessment Near Me private
psychiatric Assessment near me (http://lyo.kr)
A Brief History Of Best Website For Counterfeit Money History Of Best Website For Counterfeit Money Falschgeld online kaufen (Tina)
The Infrequently Known Benefits To Anxiety Disorders Medicine anxiety Disorder remedies
The Most Convincing Evidence That You Need Cleo Female Macaws For
Sale macaw Shop
20 Things You Must Be Educated About Paisley Hyacinth Macaw For Sale
where can i buy a macaw
7 Little Changes That’ll Make An Enormous Difference To Your
Blue Shepherds reinrassiger deutscher schäferhund züchter
10 Top Facebook Pages Of All-Time About Treat ADHD Untreated Adhd And Anxiety
The Hidden Secrets Of Power Tools For Sale power tool Sale
14 Common Misconceptions About Buy Category A Driving License Comprar Carta de Condução da Categoria B1
The Most Inspirational Sources Of Sinatra Macaw For Sale Near Me
can macaws be pets (Gabriela)
You’ll Never Guess This Buy Driving License B
Online’s Tricks kup prawo jazdy Polska
15 Gifts For The ADHD In Women Lover In Your Life adhd in women assessment
Buy German Shepherd Puppies: What’s New? No One Is Talking About Deutscher SchäFerhund Schwarz Kaufen
Automatic Vacuum Cleaner 101:”The Ultimate Guide For Beginners room cleaning robot (Fredericka)
The Three Greatest Moments In Auto Locksmith In Luton History Best auto locksmith in luton
10 Unexpected Lolita Blue & Gold Macaw Tips Do Macaws Make Good Pets
A Relevant Rant About Melody Blue Spix Macaw spix macaw for sale
How To Create An Awesome Instagram Video About Tunnel Containers
40Ft tunnel container
15 Things You’re Not Sure Of About Private Mental Health Assessment private mental health assessment ireland (Brad)
The 10 Most Scariest Things About Best Auto Locksmith Luton best auto Locksmith Luton
A Complete Guide To Buffy Macaw Bird For Sale Dos And Don’ts Severe macaws For Sale
Why You’ll Want To Learn More About Buy Category C Driving
License Comprar a carta de condução do IMT
10 Healthy Pixie Mini Macaw Habits blue macaw price (Keesha)
5 Killer Quora Answers To Toto Macau Toto macau
Where Do You Think Cleo Female Macaws For Sale Be One Year From Right
Now? parrots to buy – Lazaro –
10 Wrong Answers To Common Cleo Female Macaws
For Sale Questions Do You Know The Right Answers? buying a macaw (http://doyogastjohnvi.com/Members/Markmenu19/activity/32687)
5 Assessment For Mental Health Projects That Work For Any Budget secondary Care mental health Assessment
The Main Issue With German Shepherd Puppies For Sale In Switzerland, And
How You Can Solve It German Shepherd for sale
Buy A Driving License Legally Explained In Fewer Than 140 Characters deutschen führerschein legal kaufen (Brandy)
Is Leia Blue Macaw And Red Macaw The Best There Ever
Was? buy scarlet macaw (https://nice-hobby.com/bitrix/redirect.php?goto=https://Buy-macaw.com)
Is There A Place To Research ADHD Tests Online adhd Tests Online
Situs Togel Resmi Tips To Relax Your Daily Lifethe One Situs Togel
Resmi Trick That Everybody Should Be Able To situs togel resmi (Damian)
See What Buy Real Driving License UK Tricks The Celebs Are Utilizing buy Real driving license uk (Vuf.minagricultura.gov.co)
Cleo Female Macaws For Sale: 10 Things I’d Love To Have Known Sooner where to buy macaw
A Productive Rant About Undiagnosed ADHD In Adults how do
you get diagnosed with adhd in adults (Angelika)
Treadmills Near Me Tools To Help You Manage Your Everyday Lifethe Only Treadmills
Near Me Trick Every Person Should Know treadmill – Una –
Stationary Cycle For Exercise Tools To Improve Your Daily Lifethe One Stationary Cycle For Exercise Technique Every Person Needs To Learn stationary cycle For exercise (Images.google.Be)
See What Single Oven Electric Built In Tricks The Celebs Are Using
Single Oven Electric Built In (https://Www.Bioguiden.Se/Redirect.Aspx?Url=Https://Bjerregaard-Vick.Mdwrite.Net/The-3-Greatest-Moments-In-Single-Electric-Oven-With-Grill-History)
See What Bunk Bed With Slides Tricks The Celebs Are Using bed With Slides
What Green Sleeper Sofa Should Be Your Next Big Obsession futon sleeper Sofa
7 Simple Changes That Will Make A Big Difference
With Your Chestnut Fronted Macaw pet macaws (Terrence)
Why No One Cares About Buy Category C Driving License comprar a carta De condução do Imt (61.caiwik.com)
Why You Should Concentrate On Improving Hyacinth Macaw Parrots For
Sale where can i buy a macaw
What’s The Reason Everyone Is Talking About Pixie Mini Macaw
Today Macaw care Guide
The Top Reasons People Succeed With The Macaw Cage Industry Hyacinth bird Price
5 Clarifications On Diagnosing ADHD UK Adult Adhd Diagnosis Northern Ireland
What Is The Best Way To Spot The Right Buffy Macaw Bird For Sale For You Buy Macaw Parrot (https://Exoticbirdpurchase03905.Isblog.Net/15-Presents-For-Those-Who-Are-The-Fiona-Hyacinth-Macaw-Bird-For-Sale-Lover-In-Your-Life-49498704)
Are Sinatra Macaws For Sale The Most Effective Thing That Ever Was?
macaw representative species; Margret,
What’s The Job Market For Top 10 Crypto Casino Professionals Like?
Top 10 Crypto Casino
The 10 Most Scariest Things About Buy UK Driving Licence Online Buy UK Driving licence online
The Hidden Secrets Of Sinatra Macaws For Sale Catalina macaw Price – http://git.Isgmf.Com,
7 Things About Buy Category C Driving License You’ll Kick Yourself For Not Knowing Comprar Carta de Condução Da Categoria B1
The Reason Buy Category B1 Driving License Is So Beneficial During
COVID-19 Comprar Carta De ConduçãO Categoria B
10 Life Lessons We Can Learn From Buy A Category B+ Driving License kup prawo
jazdy a1 online (Thorsten)
Who’s The Most Renowned Expert On Buy French Bulldog Puppies?
FranzöSische Bulldogge Kaufen In Der NäHe
Buy Category A Driving License: What’s The Only Thing Nobody Has Discussed Comprar carta de condução da
categoria A (Fletcher)
The 10 Most Terrifying Things About Purebred German Shepherd Dog schäferhund abzugeben (Virginia)
The 10 Scariest Things About Loveseat For Sale cheap
sofas for sale under 300 (qna.lrmer.com)
Find Out More About Situs Togel Resmi While Working From At Home bandar togel resmi
20 Things You Need To Be Educated About Glaucous Macaw blue macaw bird price (Tammara)
The Most Hilarious Complaints We’ve Heard About Purebred German Shepherd Dog Deutscher SchäFerhund Schwarz Kaufen
Everything You Need To Learn About Sinatra Macaw
For Sale Near Me buy pet macaw
20 Irrefutable Myths About Buy Category B1 Driving License:
Busted Comprar Carta De ConduçãO Da Categoria C
You’ll Be Unable To Guess Sinatra Macaw For Sale Near Me’s Benefits Macaw for sale near me
You’ll Never Be Able To Figure Out This Sinatra
Macaw For Sale Near Me’s Tricks macaw For sale near me
Macaw Purchase Tools To Improve Your Everyday
Lifethe Only Macaw Purchase Technique Every Person Needs To Be Able To
Macaw purchase
4 Dirty Little Secrets About Locksmiths
Near Me For Car Industry Locksmiths Near Me For Car
Industry Locksmith Car Key Replacement Near Me
Why All The Fuss About Buy Category C Driving License? Comprar carta de Condução categoria B
Buy C1 E License Online Tools To Ease Your Daily Life Buy C1 E License Online Trick
Every Person Should Learn Buy C1 E License Online
Ten Buy Category A Driving License That Will Improve Your Life Comprar Carta de Condução da Categoria B1
French Bulldog 101 Your Ultimate Guide For Beginners französische bulldogge kaufen hamburg (tc.visokio.com)
Guide To Bandar Togel Terpercaya: The Intermediate Guide
For Bandar Togel Terpercaya bandar togel terpercaya
5 Must-Know-Practices Of Macaw Purchase For 2024 macaw prices (Tyson)
How To Survive Your Boss With Buy A2 Driving License Online a2 motorradführerschein online
kaufen (jszst.com.cn)
The Leading Reasons Why People Are Successful In The Hyundai Key Fob Industry hyundai i40 replacement key
These Are Myths And Facts Behind Tool Bundles draper power tool set (Mitchel)
How To Save Money On German Shepherd Puppies deutscher schäferhund welpen kaufen (Yasmin)
10 Methods To Build Your Central Heating Engineers Milton Keynes Empire Gas Safety certificate
milton keynes online (heller-dudley.hubstack.net)
The 12 Most Unpleasant Types Of Couch For Sale Tweets You Follow cheap
Couches for sale Near me (https://Historydb.date)
How To Become A Prosperous Leia Blue Macaw And Red Macaw When You’re Not
Business-Savvy hybrid macaws for sale (Ollie)
See What Add Adult Women Tricks The Celebs Are Utilizing add adult women – Roxie
–
Quiz: How Much Do You Know About Buy The IMT Driving License?
Comprar carta de conduçãO da categoria C
Five Killer Quora Answers To Folding Treadmill Cheap Folding Treadmill Cheap
Why Nobody Cares About Psychologist Near Me psychiatric help Near me
(http://www.metooo.co.uk)
The Hidden Secrets Of Link Collection Site 쥬소모음
Comprehensive List Of Buffy Macaw Bird For Sale Dos And Don’ts hyacinth bird price
15 Things You’re Not Sure Of About Best Car Locksmiths Near Luton repairs
The People Nearest To Replacement Keys For Car Tell You Some Big Secrets nearest
Are You Tired Of Buy Category C Driving License?
10 Sources Of Inspiration That’ll Revive
Your Love For Buy Category C Driving License Comprar carta de condução da
categoria A – Jerrell –
A Step-By Step Guide For Choosing Your Buy The IMT Driving License Comprar carta de condução da categoria C
Three Of The Biggest Catastrophes In Seat Replacement Key The Seat Replacement Key’s 3 Biggest Disasters In History Seat ibiza replacement Key fob
A Brief History Of Psychiatrist Uk Private History Of Psychiatrist Uk Private how much Is private psychiatry
Beware Of This Common Mistake You’re Using Your Buy
Category A Driving License Comprar Carta de Condução da Categoria B1 (https://humanlove.stream/)
The 10 Most Terrifying Things About Best Auto Locksmith Luton auto Locksmith luton
7 Things You’d Never Know About Buy Category B1 Driving License Comprar a carta de condução do IMT
Best Car Locksmith In Luton: What No One Is Discussing
auto Locksmith in luton
10 Buy The IMT Driving License-Friendly Habits To
Be Healthy Comprar Carta de ConduçãO da Categoria B1 (ezproxy.Cityu.edu.hk)
The Most Convincing Proof That You Need Buy Category C Driving License Comprar carta de condução da categoria C
20 Tips To Help You Be More Efficient With Buy Category B Driving
License Comprar a carta de condução do IMT – Ian –
10 Websites To Help You Develop Your Knowledge About Buy Category A Driving License Comprar a carta de condução do IMT (Yetta)
Best Car Locksmith In Luton: What’s The Only Thing Nobody
Is Talking About best Luton auto locksmiths (yanyiku.cn)
12 Companies Setting The Standard In Buy The IMT Driving License comprar a carta de condução do imt
What Is The Secret Life Of Buy Category B1 Driving License Comprar Carta de Condução da
Categoria B1 (Paula)
What’s Everyone Talking About Buy Category C
Driving License This Moment Comprar A Carta De ConduçãO Do IMT
How Buy Category A Driving License Was The Most Talked About
Trend Of 2024 Comprar a carta de condução do IMT
One Of The Biggest Mistakes That People Make Using Buy Category A Driving License Comprar a carta de condução do IMT
Responsible For An Buy Category A Driving License Budget?
Twelve Top Tips To Spend Your Money Comprar A Carta De ConduçãO Do Imt
So , You’ve Bought Buy Category C Driving License … Now What?
Comprar a carta De condução do IMT
Why All The Fuss About Buy The IMT Driving License?
comprar carta de condução categoria b
15 Top Twitter Accounts To Learn More About Best Car Locksmith
In Luton best luton car Locksmith
5 Facts Buy Category C Driving License Is A Good Thing Comprar
Carta De ConduçãO Categoria B [https://Www.Dermandar.Com/User/Nickelwhip7]
10 Things Your Competitors Learn About Buy Category C Driving License Comprar Carta De ConduçãO Da Categoria C (https://Kingranks.Com/Author/Domainmaid8-1740379)
20 Trailblazers Are Leading The Way In Best Exercise Bicycle Exercise Bikes
Find Out What Buy The IMT Driving License The Celebs Are Making Use Of Comprar carta de condução da categoria C
The Unknown Benefits Of Buy Category B1 Driving License Comprar carta de condução categoria B
15 Amazing Facts About Buy The IMT Driving License You’ve Never Known comprar A carta de condução Do imt [championsleage.review]
Who’s The World’s Top Expert On Buy Category C Driving License?
Comprar Carta de condução Categoria b
How To Build Successful Buy Category C Driving License Strategies From Home
comprar carta de condução categoria b (https://shtormauto.ru/bitrix/redirect.php?goto=https://www.cartoexpressodeportugal-96b.Com/)
Why Nobody Cares About Locksmiths Near Me For Car Broken
The 10 Scariest Things About Adult Test For ADHD adult test for adhd
15 Things You Didn’t Know About Buy The IMT Driving License
Comprar carta de condução da categoria A
Five Buy The IMT Driving License Projects To Use For Any Budget
Comprar carta de condução Da categoria A
5 Clarifications On Buy The IMT Driving License comprar carta de conduçãO da categoria b1
A Peek Inside The Secrets Of Buy The IMT Driving License Comprar Carta de condução Da categoria C
Are You Getting The Most Out Of Your Buy Category B Driving License?
Comprar Carta de Condução da Categoria B1
Buy Category C Driving License: A Simple Definition Comprar carta de condução da categoria C – Marti
–
A Delightful Rant About Buy Category C Driving License
comprar carta de condução da categoria b1; https://securityholes.science/wiki/the_often_unknown_benefits_of_buy_category_c_driving_license,
The Secret Life Of Buy Category B1 Driving License Comprar carta De condução categoria B
The Most Underrated Companies To Watch In The Buy Category B Driving License Industry Comprar Carta De ConduçãO Da Categoria B1
11 Creative Methods To Write About Buy Category C
Driving License Comprar Carta de condução da categoria C
Buy Category B1 Driving License Tips That Can Change Your Life
Comprar Carta de Condução da Categoria B1
7 Secrets About New Bmw Key That Nobody Will Tell You reprogrammed
You Are Responsible For The Buy Category C Driving License Budget?
12 Tips On How To Spend Your Money Comprar A Carta De ConduçãO Do IMT
15 Twitter Accounts That Are The Best To Learn About Buy Category A Driving License Comprar Carta De Condução da Categoria B1
Is Your Company Responsible For A Buy Category C Driving License Budget?
12 Top Ways To Spend Your Money Comprar a carta de condução do IMT
What You Can Do To Get More With Your Buy Category B Driving License comprar carta de Condução da categoria a
What Buy The IMT Driving License Experts Want You To Learn Comprar Carta De ConduçãO Da Categoria B1
The Three Greatest Moments In Buy Category A Driving License History Comprar carta de condução da categoria C
You’ll Never Guess This Containers For Sale Middlesbrough’s Tricks containers for
sale middlesbrough (Kathrin)
5 Lessons You Can Learn From Buy Category B1 Driving
License Comprar carta De condução categoria B
10 Places Where You Can Find Buy Category C Driving License Comprar Carta de Condução Da Categoria B1
How Buy Category A Driving License Was The Most Talked
About Trend Of 2024 Comprar Carta de condução categoria B (http://www.bioguiden.se)
See What Treadmills Tricks The Celebs Are Using treadmill
“Ask Me Anything:10 Responses To Your Questions About Buy Category B Driving License Comprar carta de condução categoria B
10 Misconceptions Your Boss Shares About Buy Category A Driving
License Comprar carta de condução da categoria A (Werner)
15 Top Pinterest Boards From All Time About Buy The IMT Driving License Comprar carta de condução categoria B
An Adventure Back In Time How People Talked About Buy Category A Driving License 20 Years
Ago Comprar carta de condução da categoria A (Silas)
3 Ways That The Buy Category A Driving License Will Influence
Your Life Comprar Carta De ConduçãO Categoria B
The Most Underrated Companies To In The Buy Category B Driving License
Industry Comprar carta De condução da categoria C
10 Websites To Help You Learn To Be An Expert In Buy Category A
Driving License Comprar carta de condução categoria
B (Dewayne)
Why You Should Not Think About The Need To Improve Your CSGO Case Battle
Csgo Case Battles
9 . What Your Parents Taught You About Best Auto Locksmiths Luton auto locksmiths luton –
Lizzie –
Davis stated the rules by which they passed they legislation and votes on it.
http://www.skin-vfowc.xyz/blog/1740902379693
10 Facts About Address Collection That Will
Instantly Put You In A Positive Mood 주소모음 사이트
The Secret Secrets Of Collection Of Site Links 최신주소모음
What’s The Job Market For Best Auto Locksmith Near Luton Professionals?
best auto locksmith near luton [Chastity]
The 10 Scariest Things About Best Car Locksmith In Luton Best car Locksmith In luton
What’s The Ugly Truth About Address Collection 사이트 모음
7 Simple Tricks To Totally Intoxicating Your Site Collection 사이트모음
These include Denali (previously generally known as Mount McKinley) in Alaska, the Grand Canyon in Arizona, Niagara Falls on the U.S.-Canada border, Yellowstone Nationwide Park in the western U.S.
https://leetcode.com/u/ddkyhryrfzsk/
The Reason Why Everyone Is Talking About Give Me The Address Right Now
주소주라 (http://www.demilked.Com)
What’s The Most Common Collection Of Site Addresses Debate Could Be As Black And White As You Might Think 최신링크모음
Why Nobody Cares About Auto Locksmith In Luton Keys
Элегантные ковры для любого интерьера, найдите.
Лучшие варианты ковров для вашего дома, закажите.
Ковры ручной работы, новинки.
Декорируйте пространство с помощью ковров, харизму.
Безопасные и яркие ковры для детской, разнообразие.
Ковры в восточном стиле, откройте.
Эстетика ковров в офисе, профессионализм.
Ковры, которые легко чистить, узнайте.
Руководство по выбору ковров, читайте.
Теплота и уют с коврами, откройте.
Актуальные стили и дизайны ковров, освежите.
Создайте уют на даче с коврами, уникальные стили.
Идеи по использованию ковров, креативность.
Выбор ковров для любого вкуса, новые варианты.
Создайте атмосферу уюта в спальне, дизайны.
Качество и стиль от лучших производителей, откройте.
Выбор ковров для домашних любимцев, выбирайте.
Согревающие ковры для вашего дома, уют.
Ковры для создания зонирования, функции.
детские ковры [url=https://kovry-v-moskve.ru/]https://kovry-v-moskve.ru/[/url] .
5 Lessons You Can Learn From Car Locksmith In Luton Best luton Auto locksmith; http://www.metooo.it,
What’s The Current Job Market For Best Auto Locksmith Near Luton Professionals Like?
best Auto locksmith near luton
20 Resources That Will Make You More Efficient With Auto
Locksmith In Luton Best Auto Locksmith In Luton
11 Creative Ways To Write About Address Collection 주소모음사이트
The 10 Most Scariest Things About Car Locksmiths Luton car locksmiths luton
The Top Car Locksmith Near Luton Gurus Can Do 3 Things luton Auto locksmiths
5 Killer Quora Answers To Luton Best Auto Locksmith auto
Another factor to consider in comparing insurance policies is whether or not a coverage provides a minimal tolerance premium that sustains the policy for as long as it’s paid.
http://www.big-wxmv.xyz/blog/1740673499500
Here’s A Little Known Fact Concerning Latest Address
Collection 주소 모음 (Yanira)
Try stringing strands of them from the backs of chairs or adding them to your flower preparations and centerpieces.
http://www.nqxm-day.xyz/blog/1740741803674
Having read this I believed it was very enlightening. I appreciate you taking the time and effort to put this article together. I once again find myself spending a lot of time both reading and commenting. But so what, it was still worth it!
Small business owners must calculate the pros and cons, their capabilities and borrow only an amount that will help them meet immediate needs.
https://www.northwestu.edu/?URL=https://superopulent.co.uk/products/goyard-boston-50-duffle-bag-grey
CBT also teaches people relaxation strategies, such as deep respiratory and progressive muscle relaxation, to help reduce anxiety within the moment.
http://www.financial-jvteq.xyz/blog/1740673445184
In case of large run on the shares listed, the change operators have proper to ban the sale of the scrip or put a band on costs to handle the problems with volatility.
https://sovren.media/u/eggden5/
See What Auto Locksmiths Luton Tricks The Celebs Are Using auto locksmiths luton (Devon)
10 Tips To Build Your Luton Car Locksmith Empire Luton Auto Locksmith (Championsleage.Review)
20 Luton Car Locksmith Websites That Are Taking The Internet By Storm car locksmith
in luton (http://www.jinritongbai.com)
Five Killer Quora Answers On Best Car Locksmith Luton Car Locksmith Luton
If they’ve received a better plan to create jobs rebuilding our infrastructure or to assist workers earn the high-tech abilities that they need, then they should supply up these ideas.
http://www.work-srxx.xyz/blog/1740673417439
How Auto Locksmiths Luton Became The Hottest Trend
In 2024 auto locksmiths in luton [http://italianculture.net]
9 Lessons Your Parents Teach You About Best Auto Locksmiths Luton best auto locksmiths luton (Carrol)
Five Killer Quora Answers On Auto Locksmith In Luton auto locksmith in luton [Leoma]
How You Can Use A Weekly Auto Locksmiths Near Luton Project Can Change Your Life
best auto locksmiths near luton (Ardis)
Omaha Postcard & Paper Show.
http://www.night-swnvpm.xyz/blog/1740741795146
Five Killer Quora Answers On Car Locksmiths Near Luton car locksmiths near luton (Rufus)
10 Quick Tips To Auto Locksmith Near Luton Auto Locksmith Luton
10 Of The Top Facebook Pages Of All-Time About Car Locksmiths Luton best Car locksmiths
luton (http://italianculture.net/redir.php?url=https://Agerskov-overby.Blogbright.net/20-reasons-why-Auto-locksmith-near-luton-will-never-be-Forgotten)
12 Stats About Car Locksmith Near Luton To Make You Take A Look At Other People best car locksmith near
luton [Rosaria]
Guide To Car Locksmith Near Luton: The Intermediate Guide For Car Locksmith Near Luton Car Locksmith Near
Luton – https://Www.Metooo.Io/U/677Db167F13B0811E9370E1E –
20 Auto Locksmiths Near Luton Websites Taking The Internet By Storm car
Five People You Should Know In The Auto Locksmiths
In Luton Industry motor
Best Car Locksmith Near Luton Tips To Relax Your Daily Lifethe One Best Car Locksmith Near Luton Trick That Everyone Should Be Able To best car locksmith near Luton
Auto Locksmiths Luton Tips From The Most Effective In The
Business best Luton car locksmiths
You’ll Never Be Able To Figure Out This Best Car Locksmiths Near Luton’s Tricks Car Locksmiths Near Luton
Ten Stereotypes About Best Car Locksmiths Near Luton That Aren’t Always True luton auto locksmiths; https://www.question-ksa.com/user/snakeclick0,
You’ll Never Be Able To Figure Out This Best Car Locksmiths Near Luton’s Tricks best car locksmiths near luton
Do Not Buy Into These “Trends” Concerning Best Auto Locksmiths Luton best auto locksmiths in luton
See What Car Locksmith Luton Tricks The Celebs Are Making Use Of Car locksmith luton (http://www.nlvbang.com)
You’ll Be Unable To Guess Auto Locksmiths Luton’s Benefits Auto Locksmiths Luton
5 Laws That Anyone Working In Auto Locksmiths In Luton Should Be Aware Of fob
The Best Car Locksmith Near Luton Tricks To Change
Your Life Best car locksmith near luton – mem168.com –
How To Become A Prosperous Auto Locksmith Luton Even If You’re Not Business-Savvy auto locksmith in luton
Five Things You’re Not Sure About About Auto Locksmith Near Luton Auto Locksmith Luton (Git.Fuwafuwa.Moe)
What Experts In The Field Would Like You To Know
Auto locksmith Luton
Hi, yes this post is truly nice and I have learned lot of things from it regarding blogging. thanks.
Thousands of years after his death, Malgus was nonetheless remembered as probably the most powerful Sith Lords to have ever lived.
http://www.factor-qlnvw.xyz/blog/1740296192686
Appreciating the dedication you put into your website and in depth information you offer. It’s great to come across a blog every once in a while that isn’t the same old rehashed information. Fantastic read! I’ve bookmarked your site and I’m including your RSS feeds to my Google account.
Купить автозапчасти по выгодным ценам, с доставкой на дом, всегда в наличии, Запчасти для отечественных автомобилей, с доставкой по России, Где купить автозапчасти, по лучшим ценам, с гарантией качества, по отличным ценам, в любое время, с доставкой на дом, Купить запчасти для авто, по отличным ценам, с быстрой доставкой, легко и удобно, каталог на любой вкус, Надежные детали для вашего автомобиля, с гарантией возврата, Лучшие автозапчасти для вашего авто, с гарантией качества, по выгодным условиям
авто магазин [url=https://mechamotive.com/]авто магазин[/url] .
Additionally, check to confirm the hearth and security codes that the venue has to abide by.
https://independent.academia.edu/saufcYkXbsaufcYkXb
They played board video games.
https://gdfjdfgh.blogspot.com/2025/02/6kxzsgexf.html
You expressed it well.
online casinos mit paysafecard https://mapcasino.info/pennsylvania-online-casinos/ free online casino play
I just come out and say it.
https://forums.servethehome.com/index.php?members/aalrkgk.152272/#about
The Sage Advice On Buy A Driving License With Code 95 From A Five-Year-Old b1 prawo jazdy – Cassandra –
5 Common Myths About Buy A Category B Driving License Without An Exam
You Should Stay Clear Of prawo Jazdy Kat C
Are You Getting The Most Value Of Your Scooter Driving License?
b1 prawo jazdy; Ava,
10 Websites To Aid You Develop Your Knowledge About Driving License Category C ile kosztuje Prawo jazdy Na skuter?
One Buy A Category B Driving License Without An Exam Success Story You’ll
Never Be Able To Prawo Jazdy a1
20 Quotes That Will Help You Understand Buy A
Driving License With Code 95 Kup Prawo Jazdy A A1 A2 bez testu;
Lilliana,
10 Places To Find Scooter Driving License prawo jazdy A1 (jsfiddle.net)
17 Signs To Know If You Work With Driving License
C+E B1 Prawo jazdy
How To Explain Driving License C+E To Your Grandparents kup prawo jazdy kategorii b bez egzaminu (https://500px.com/p/howardotvrask)
Buy European Driving License Uk Online Tools To Ease Your Daily Life Buy European Driving License Uk Online Trick That Every Person Must Be
Able To buy european driving license Uk online
The Top Driving License C+E That Gurus Use Three Things b1 prawo Jazdy
How To Create An Awesome Instagram Video About Driving License Category C Prawo Jazdy b1
It’s Enough! 15 Things About Buy A Category B
Driving License Without An Exam We’re Tired Of Hearing prawo jazdy na skuter (Andre)
Great article, exactly what I needed.
My web blog – Asset recovery center
7 Simple Tips To Totally Making A Statement With Your Driving License
Category C kup prawo jazdy a a1 A2 bez testu
Are You Getting Tired Of How Much Does A Scooter Driving License Cost?
10 Inspirational Sources To Bring Back Your Love prawo jazdy kat c (Octavio)
Plus all the issues that you simply see in potential atms and public transport machines, toilet doors and such.
https://paste.jp/70e2255a/
You may comply with Liz Uy on her Instagram account here.
https://anotepad.com/notes/gnetpddf
With imports from throughout Asia and a wealthy cultural inheritance, take a souvenir again dwelling within the type of Antiques and Artefacts, and remember Singapore perpetually.
http://pastie.org/p/6DuOsk3VrRi0F1TZmIZ1hI
As much as $30,000 of lively-obligation pay is tax-free if stationed out of state for a hundred and twenty consecutive days or extra.
https://paste.thezomg.com/252121/32970021/
Now rinse thoroughly so that each bit of shampoo is off your French Bulldog.
https://paste.md-5.net/exufuxanuh.xml
Replace Lock In Upvc Door: 10 Things I’d Like To Have Known In The Past front door lock replacement
cost (marvelvsdc.faith)
The Reason Why Everyone Is Talking About Buy A Driving License A A1 A2 Without A Test
Right Now Ile Kosztuje Prawo Jazdy Na Skuter?
Hello every one, here every person is sharing these kinds of experience,
so it’s good to read this web site, and I used to pay a
visit this website daily.
Here is my page Golden Visa Program
10 Meetups About Buy A Driving License A A1 A2 Without
A Test You Should Attend prawo jazdy kat c
10 Quick Tips For Buy A Driving License With Code 95 prawo jazdy c+E
15 Gifts For The Driving License C+E Lover In Your Life ile kosztuje prawo jazdy na skuter?
The 3 Largest Disasters In Driving License A1 History prawo jazdy kat c (http://www.makeup-spb.ru)
A good mesothelioma lawyer will offer a no-cost case evaluation to determine if you are eligible
for compensation. The top mesothelioma lawyers also operate on a
contingency basis.
My website … Asbestos Law
10 Quick Tips About Driving License C+E Kup prawo jazdy kategorii B bez egzaminu
What’s The Current Job Market For Male Masturbaters Professionals?
male masturbater (Alexandria)
How To Explain Male Masterbation Devices To Your Grandparents best Male masterbators
Guide To Cost For Car Key Replacement: The Intermediate Guide For Cost For Car Key Replacement cost for car key replacement, Norberto,
Mrs. Pearson died Thursday afternoon at Spring Seasons of Elkhart.
https://paste.jp/87f8c761/
2014 Business Individual of the Year and 2007 Lester Leffler Memorial Neighborhood Volunteer Service Award for the Neighborhood of Lebanon Association.
https://sebsauvage.net/paste/?f7ce9a3946abb0c5#d1f+X6u/ck5ZD5Ws7bQpD26geCIEllIqa9NgedeR+LU=
KROPP, pastor of Or Lady of Perpetual Assist Catholic Church, Sterling will officiate and burial might be ;in Fletcher Cemetery below Robins Funeral House, Fletcher.
https://paste.jp/95840516/
You’ll Never Guess This Realistic Sexual Dolls’s Benefits Realistic Sexual Dolls;
Vmstation.Net,
The names have a typical significance.
https://paste.vpsfree.cz/sjUDmdiT/+inline
TMAO decomposes to trimethylamine (TMA), which is the main odorant that is characteristic of degrading seafood.
https://paste.rs/efxKy.txt
What’s The Current Job Market For Portable Mobility Scooters Professionals Like?
portable mobility scooters (Connie)
Until 2017, Flagstaff’s crime price was usually according to the US average.
https://onlinegdb.com/RwRWcOV0g
We conceived several player reward programs, together with talent point awards, augmentation upgrades, weapon availability timelines and tool/object availability timelines.
https://hastebin.skyra.pw/conayaxoco.bash
Interment followed on the Wilbur Cemetery, with Strate Funeral Dwelling in charge.” (scrapbook obit: undated; d.
https://notes.io/w7xuf
The four Virginia Corporations mustered at Williamsburg, Virginia, in August 1740, but the transport ships did not set sail for Jamaica till early October.
https://snippet.host/svbrtu
WATCHING The same Sport?
https://paste.jp/49eecd20/
He is survived by his wife Gladys of the home; a son, Donald Eugene WARNER, one sister, Mrs.
https://paste.vpsfree.cz/eLCypGCG/+inline
The conference steering committee should be consulted about any adjustments to the accepted way of organizing and operating the convention.
https://hastebin.skyra.pw/cuxawehaca.bash
11 Strategies To Completely Redesign Your Mens Masturbators Top Male masturbator
Do thorough analysis:The web is a great platform to look one of the best event management firm.
https://notes.io/w7xwy
In actual fact, as stipulated by regulation, we cannot and don’t make any guarantees about your ability to get outcomes or earn any money with our ideas, info, tools or methods.
https://paste.jp/04172b8a/
Ask Me Anything: 10 Answers To Your Questions About Male Masturbating Toy male masturbating Toys
10 Things You Learned In Kindergarden They’ll Help You Understand
Male Masterbation Devices best Male masterbater
10 Facts About Mesothelioma Attorney That Make You Feel Instantly Good Mood Asbestos Lawyer [africaband42.bravejournal.net]
Ten Things Your Competitors Teach You About Pragmatic Image 프라그마틱 슬롯 하는법
Saved as a favorite, I really like your web site!
https://pafibondowoso.org/
What’s The Current Job Market For Peugeot 3008 Key Fob Professionals Like?
peugeot 3008 key (Beulah)
The History Of Bmw Replacment Key Prices
3 Common Reasons Why Your Adult Toy Store Near Me Isn’t Working (And What You Can Do To Fix It) Interactive Adult toy
9 Lessons Your Parents Teach You About Upvc Window Repairs upvc window repair (lanbail68.werite.net)
Good post. I will be going through some of these issues as well..
https://pafibondowoso.org/
A Look At The Ugly Reality About Ramps For Wheelchairs At Home wheel chair ramp for vans [mymobilityscooters52601.dekaronwiki.com]
However, the American Animal Hospital Association adds that the vaccine may be indicated in dogs traveling from low risk to high risk regions of the country [url=https://fastpriligy.top/]where to buy priligy in usa[/url]
10 Facts About Tiktokpornstar That Will Instantly Put You In A Good Mood Tiktok Pornstar
Check Out The Rabbit Adult Toys Tricks That The Celebs Are Using the rabbit adult toy (Marina)
Guide To Cost Of Spare Car Key: The Intermediate Guide To Cost Of
Spare Car Key cost of spare Car key; ulriksen-Kanstrup-3.blogbright.net,
See What Tattooed Pornstars Tricks The Celebs Are Making
Use Of Tattooed pornstars
See What Cheap Media Wall Fires Tricks The Celebs Are Utilizing Cheap
Media Wall Fires (Maps.Google.Cat)
A mesothelioma lawsuit can be an effective method
for asbestos Lawyer patients to
obtain compensation. The money awarded can be used to pay
for medical expenses, lost income and other financial costs.
What’s The Current Job Market For Coffee Machines Beans Professionals
Like? coffee machines beans (Isidra)
Say “Yes” To These 5 SEO UK Company Tips local Seo company london
I want to to thank you for this excellent read!! I absolutely enjoyed every bit of it. I have you book marked to check out new things you post…
https://bibipaw.com/product-category/dog-carriers/
Free Mlm Leads – How Create Mlm Leads Online 100 % Free 링크모음
Start to appreciate and revere the supernatural energy and authority of THE Word OF GOD.
https://forum.ixbt.com/users.cgi?id=info:3E1874693
Tiny low-voltage halogen uplights (cheap can lights that sit on the ground) throw light up to be reflected from walls and ceilings.
https://www.skipass.com/users/tvsyaopqavcadu/
10 March 1925: The line was extended eastbound from Croix Rouge to Mabillon.
https://www.italki.com/user/25233871
Chief Radio Electrical Artificer Michael Anthony Lang, P/M928789.
https://www.equinenow.com/farm/profile6709d30f071b3.htm
After Helmsley’s purchase, each the exterior and inside of the brand new York General Constructing have been restored.
https://www.instructables.com/member/ejckDMSiVxuTUiBC/?cb=1728985694631
Noorul Haq Sufaarali, Sergeant, North Borneo Constabulary.
https://www.metal-archives.com/users/pxqlbrwdso
Residents of the Fourth Ward in the city felt that their property values and the group would fall apart if the railroad got here by way of their area.
https://www.indiegogo.com/individuals/38189988
Drexel (30 Might 2015).
https://comicvine.gamespot.com/profile/pvZHmh/
The federal government said the increases to tuition fees and upkeep loans are in step with inflation.
https://www.indiegogo.com/individuals/38190721
Florence Worth, Member, Nottinghamshire County Council.
https://jsfiddle.net/u/ATTKLOGJkR/fiddles/
At this time, St.
https://seedly.sg/profile/mrphtcgcwzswpwqn/
The town of Oceanside maintains a map of the general public storm drain system, additionally recognized as the Municipal Separate Storm Sewer System (MS4).
https://tinhte.vn/profile/gfgmsobd.3128551/
Frank Flynn, Underground Worker, Hapton Valley Colliery, Burnley Area, North-Western Division, Nationwide Coal Board.
https://pbase.com/oJGXfqUGuKD
This is an exciting game to play at college, when camping, or throughout a celebration.
https://starity.hu/profil/508578-csvcanxa/
Prepared food gross sales were now not allowed at many farmers markets.
https://open.mit.edu/profile/01JAAA6EYWREZ59A6C1KRGG0QS/
The D’Evercy family have been responsible for constructing the virtually adjoining church.
https://www.skipass.com/users/cckbhrcxsatg/
Test all mild fixtures earlier than putting in them in a cage.
https://www.instructables.com/member/qQTGUQxcWvRW/?cb=1731662889413
Showing on the show as a part of the viewers, Will mentioned: ‘I’m so gutted but it is so good to be here to help everyone, they’re all smashing it tonight.
https://es.pinterest.com/udrnoyhxlx/
At the October 4 meeting, attended by not less than 800 residents of Passaic at Woodrow Wilson Junior Highschool, Martini offered a decision to withdraw the elevation different from the mission.
https://www.4shared.com/u/K4_0giQQ/llgckbpoxe.html
[url=https://fastpriligy.top/]priligy amazon uk[/url] IГў ll pass this along to him again and ask him to source without just linking
Hello fantastic website! Does running a blog similar to this take a large amount of work?
I’ve virtually no understanding of computer programming but I was hoping to start my own blog soon. Anyhow, should you have any recommendations or techniques for
new blog owners please share. I know this is off subject but I simply
had to ask. Many thanks!
my homepage :: dich vu seo
Online Advertising Is A Major Way To Obtain Traffic 주소주라
An outstanding share! I’ve just forwarded this onto a co-worker who was conducting a little research on this. And he actually bought me lunch because I found it for him… lol. So allow me to reword this…. Thank YOU for the meal!! But yeah, thanks for spending some time to discuss this issue here on your internet site.
https://eden-mobility.co.uk/collections/stairlifts
5 Killer Quora Answers To Bi Fold Repairs bi fold repairs
Keep An Eye On This: How Case Opening Battle Is Taking Over The World And
How To Respond case battle Sites (coolpot.stream)
9 Signs That You’re A Audi Key Expert Cheapest
10 Misleading Answers To Common Composite Door
Frame Repair Questions: Do You Know The Right Ones?
How To Repair A Composite Door
How To Install A UPVC Door Panels Cat Flap cat flap (aboutdirectorofnursingjobs.Com)
Drugs For Anxiety Disorder Tools To Ease Your Everyday Lifethe Only Drugs For
Anxiety Disorder Technique Every Person Needs To Be Able To Drugs for anxiety disorder
Chaise Sofa Explained In Less Than 140 Characters Small Chaise Sofa
(Villumsen-Thybo.Federatedjournals.Com)
You’ll Be Unable To Guess Composite Door Panel Replacement’s Tricks composite door panel replacement (Sabina)
Koop IPTV-abonnement https://www.iptvaanbiedersnederland.net/
Be On The Lookout For: How Upvc Window Replacement Hinges Is Taking Over And What Can We Do About It
replacement upvc hinges
The 10 Most Scariest Things About Adhd Assessment For Adults diva adhd assessment
(prbookmarkingwebsites.com)
10 Asbestos Cancer Lawsuit Lawyer Mesothelioma Tips All Experts Recommend mesothelioma lawsuit
20 Trailblazers Lead The Way In Audi Car Key Replacement audi
key replacement cost [Thaddeus]
What Is The Reason Adding A Key Word To Your Life
Can Make All The A Difference mesothelioma lawsuits [https://buketik39.ru/user/carbonface7]
Cat Flap Installation In Glass Doors Near Me cat Flap Installation
Glazing Repair Near Me: It’s Not As Expensive As You Think Double glazed window repairs near me
The 10 Scariest Things About Leather Recliners For
Sale leather recliners for sale – Traci –
The Most Pervasive Problems In Pragmatic Slot Recommendations
프라그마틱 슬롯 무료체험
The Top 5 Reasons People Thrive In The Audi Spare Key Industry audi replacement Key service
What’s The Current Job Market For Bifold Door Replacement Professionals Like?
bifold Door replacement
What Is Small Wood Burning Stove? History Of Small Wood Burning Stove Small Wood Burning Stoves Uk
Ten Things You Learned In Kindergarden To Help You Get Started With Case Opening Battle casebattles (Matthew)
Asbestos Attorneys Georgia Tips To Relax Your Daily Life
Asbestos Attorneys Georgia Trick That Everybody Should Know asbestos attorneys
Guide To Vintage Couch For Sale: The Intermediate Guide For Vintage Couch For
Sale Vintage Couch for Sale
Cat Flap Fitting Near Me cat flap Installer
The Reason Glazing Repairs Near Me Is So Beneficial
In COVID-19 double glazing repairs near me
The 9 Things Your Parents Teach You About SEO Agency Near Me seo agency near me
I’m amazed, I must say. Seldom do I encounter a blog that’s both equally educative and amusing, and let me tell you, you’ve hit the nail on the head. The issue is an issue that not enough men and women are speaking intelligently about. I’m very happy that I came across this during my search for something concerning this.
https://wooricasinogame.com/
Nice post. I learn something new and challenging on blogs I stumbleupon everyday. It will always be useful to read through articles from other writers and practice something from their web sites.
https://tubidymp3.link
Awesome write ups. Thanks.
las vegas online casino real money no deposit no deposit online casinos best online casino in the world
I love reading an article that can make men and women think. Also, many thanks for allowing me to comment.
https://lazer888.org/
Five Killer Quora Answers To Adultwork Pornstar Adultwork Pornstar
Incredible all kinds of beneficial material.
best casino online website online casino slots draftkings online casino illinois
A fascinating discussion is worth comment. I believe that you need to write more on this subject, it might not be a taboo matter but usually people do not discuss such issues. To the next! All the best!
https://www.damnbud.com/online-dispensary-that-ships-to-all-states.html#/
Thanks, An abundance of info!
superbet casino games online online casino real money free play gta online how to make money with casino
Awesome info. Many thanks!
slovenskГ© online casino online real money casinos best online casinos sign up bonus
An impressive share! I’ve just forwarded this onto a colleague who has been doing a little research on this. And he in fact bought me breakfast due to the fact that I discovered it for him… lol. So let me reword this…. Thank YOU for the meal!! But yeah, thanx for spending time to discuss this issue here on your web site.
https://baskiliposeti.com.tr/
Greetings! Very useful advice within this article! It is the little changes that will make the most significant changes. Many thanks for sharing!
https://baskiliposeti.com.tr/
I truly love your website.. Pleasant colors & theme. Did you make this website yourself? Please reply back as I’m looking to create my own site and would love to learn where you got this from or just what the theme is called. Appreciate it.
https://toptanposetci.com/poset-baski/
I was able to find good information from your articles.
https://toptanposetci.com/rulo-boru-naylon/
Thanks, Wonderful stuff!
online casino ohne lizenz online casino no deposit bonus codes apple online casino
I’m more than happy to discover this page. I need to to thank you for ones time due to this fantastic read!! I definitely appreciated every part of it and i also have you saved as a favorite to look at new things on your web site.
https://eroticacams.com
You’ve made your stand extremely clearly!.
online casino merkur spiele online casino bonuses low wagering online casinos
I’m impressed, I have to admit. Seldom do I encounter a blog that’s both equally educative and amusing, and let me tell you, you’ve hit the nail on the head. The issue is something that not enough men and women are speaking intelligently about. I am very happy I found this in my hunt for something concerning this.
https://www.pratibha.pw/domain-list-438
Good content. Kudos.
mejores casinos online para ganar dinero captain cooks casino canada casino online espana
There is definately a great deal to learn about this topic. I really like all of the points you made.
https://mediamate.co.za
Many thanks. Fantastic stuff.
do people win on online casino online casino with free signup bonus real money usa online casinos that use trustly
This site was… how do you say it? Relevant!! Finally I’ve found something which helped me. Appreciate it!
https://ecoposet.com
Rizvi, Samad (April 24, 2012).
https://cookpad.com/jp/users/110665641
When these refugees come from the Detention Centre in Woomera to Melbourne, we work day and night time with the Councils, we work with the Immigration Department, we work with the churches altogether, and we help these refugees in a really vast approach.
http://taylorhicks.ning.com/profile/ovHBjfS
Collectible bananas discovered throughout the game are also value 100 points, while multipliers rising the participant’s rating by a factor of two or four are activated when a ground is finished in beneath half the allotted time or via a warp gate.
https://www.shutterstock.com/g/zelwjxf
This allows us to make sure delivery of durable and reliable merchandise all over the world.
https://lu.ma/user/usr-SpkFCYXrR7Gvlqa
Chua, Dennis (October 17, 2022).
https://www.giantbomb.com/profile/ivdwlgdyo/
These legal paperwork can then provide constructing owners with the reassurance of figuring out that not solely are the required passive fire protection merchandise match for function, but they’re additionally totally compliant with the relevant Building Regulations.
https://www.skipass.com/users/hljzfoixkezm/
Can I just say what a comfort to discover somebody that really knows what they are discussing over the internet. You certainly know how to bring a problem to light and make it important. More and more people must read this and understand this side of your story. It’s surprising you’re not more popular since you most certainly possess the gift.
https://ecoposet.com
I absolutely love your site.. Great colors & theme. Did you make this web site yourself? Please reply back as I’m trying to create my own blog and want to know where you got this from or exactly what the theme is named. Kudos!
https://gebyar4d.internet.in/
Good post. I certainly appreciate this website. Keep writing!
https://cesarvwndr.blogadvize.com/37442111/a-comprehensive-guide-to-tubidy
And the same frame was painted cream colour (referred to as champagne), geared up with Campy’s NR, and bought as the Superleicht.
https://www.4shared.com/u/JzwWqMkn/ceiliro1992.html
Utilizing stamps, ink, markers, collage, paper and yarn, we are going to create our personal prayer flags then string them collectively to make them ready to dangle!
https://pbase.com/gCndiJFaHdX
510. i.e., It hazel nuts be plentiful, the season will likely be unhealthy.-Shelly.
https://allmylinks.com/jfxibsnskyq
Along with selecting three faculty board members on April 4, 2017, residents of the West Allis-West Milwaukee College District also voted on a $12.5 million referendum to be unfold out in $2.5 million increments over faculty years 2017-2018 by 2021-2022.
https://allmylinks.com/pvugqsazo
Take a while to learn more about the sacrifices made by navy personnel by watching a patriotic movie or documentary.
https://maps.roadtrippers.com/people/SCNOz9IZxt1JvD?lng=-106.77766&lat=41.11498&z=3.30945
This refers back to the phenomenon of how teams usually do better after they’re in their very own field, surrounded by their very own followers.
https://www.4shared.com/u/sgl5NZ8I/terblectmi1992.html
Casamassina was additional impressed by the physics of Monkey Bowling, elaborating that “when the pins break apart one would swear it is the actual deal”, however Turner criticized its physics as “slightly wonky”.
https://answers.informer.com/user/sabarzspq
Cartoon Network. Season 2. Episode 9. Cartoon Community.
https://pastelink.net/fj7gyi7w
They famous that the items that departed Saturday had been thought of among essentially the most disciplined of the Palestinian forces.
https://allmylinks.com/amunqzfrqyljp
Despite solely dealing with him throughout Schumacher’s brief comeback within the 2010s, Lewis Hamilton is also seen a rival on account of their related achievements and driving styles, and cited him as inspiration.
https://www.indiegogo.com/individuals/37808828
If in case you have been ready for the proper perfume to usher in that ‘really Italian’ temperament to your dresser, Then, Sicily is the proper selection for you.
https://www.answers.com/u/plotlosfi1992
Friday at Hall-Jordan Memorial Chapel, 918 S. Essential St., Middletown.
https://www.answers.com/u/actidu1980
Visitation will be from 6 to eight p.m.
https://www.shutterstock.com/g/wwarswq
Along with selecting three faculty board members on April 4, 2017, residents of the West Allis-West Milwaukee College District also voted on a $12.5 million referendum to be unfold out in $2.5 million increments over faculty years 2017-2018 by 2021-2022.
https://pbase.com/gCndiJFaHdX
Exclusions might apply. While supplies final.
https://www.answers.com/u/creasupta1993
The stadium’s location in the guts of the Carolinas draws a passionate fan base from both North and South Carolina, making it a vibrant venue on recreation days.
https://jsfiddle.net/sSdKByBYb/7y3xgc8t/
Physique kinds proliferated, and by 1932 included such exotics as a $625 landau phaeton.
https://www.shutterstock.com/g/ojnqjlo
I want to to thank you for this very good read!! I definitely enjoyed every bit of it. I’ve got you saved as a favorite to check out new things you post…
https://pornvideo80098.slypage.com/30948999/the-cbd-records
You actually expressed this exceptionally well.
nj online casino deposit bonus best online casino in canada minnesota online casino
Many thanks, Helpful stuff.
casino online 2019 best casino online paradise casino online real money
A household room should be as inviting as potential by capturing the flavor, pursuits, and life-style of the owners, and it should be comfortable for real-life actions without excessive-upkeep decorating treatments that require kid gloves.
https://kerabenprojects.com/boletines/redir?dir=https://answers.informer.com/user/uxepahyjaq
With a 4000 sq.
https://forex-brazil.com/redirect.php?url=https://www.inkitt.com/xHtKTpFQrAFUM
Jodha succeeded in conquering the encircling territory from the Delhi Sultanate and thus founded a kingdom that came to be generally known as Marwar.
http://amigos.chapel-kohitsuji.jp/?wptouch_switch=desktop&redirect=https://sandbox.zenodo.org/communities/unhwyzpte
All he must do is look his folks in the attention and stick his tongue out for good measure.
https://www.noiseontour.com/web/index.php?menu=100&pagina=redireccionar&redirectURL=https://www.answers.com/u/daylynacon1982
What sort of jacket is best during chilly evenings?
https://aijaa.com/adserver/www/delivery/ck.php?ct=1&oaparams=2__bannerid=1417__zoneid=50__cb=4ddda6a77a__oadest=https://www.instructables.com/member/ViEygqFxwvzhNY/?cb=1728030747402
It can be argued that strippable Semicon can lead to fewer workmanship issues at medium voltage.
https://www.digitalproserver.com/ip/carolina/adlink.php?go=https://yoo.rs/@htrmvrjenmsn
Typically used for stainless steels and heat-resistant alloys.
http://wifeamateurpics.com/ddd/link.php?gr=1&id=fdefe3&url=https://www.canadavisa.com/canada-immigration-discussion-board/members/vgddrpapheiq.1233101/about
The exhibition’s title comes from the Robert Farris Thompson e-book of the same name, which elaborates on the lasting affect of ancient West African aesthetic traditions on contemporary diasporic communities.
https://store.xtremegunshootingcenter.com/trigger.php?r_link=https://www.mobygames.com/user/1061050/cfzgnnrov/
Nicely put, Thank you.
abrir un casino online free casino online slots andar nights evoplay entertainment online casino
Many thanks! Very good information.
android online casino no deposit bonus slots casino online best saucify online casinos
Seriously a lot of great knowledge!
no deposit bonus online casino codes slot casino online top online casino no deposit bonus
Useful facts. With thanks.
online live casino bonus ohne einzahlung real cash casinos online wizbet online casino
Nice post. I learn something totally new and challenging on blogs I stumbleupon every day. It will always be helpful to read articles from other writers and practice a little something from their websites.
https://investeren-in-startups.nl/
You should be a part of a contest for one of the best blogs on the net. I’m going to recommend this blog!
https://investeren-in-startups.nl/
Truly quite a lot of excellent facts.
columbus online casino social casinos online jubilee casino online
Incredible lots of helpful tips.
online casino influencers online casino usa real money new online casinos october 2023
Oh my goodness! Awesome article dude! Thank you so much, However I am encountering difficulties with your RSS. I don’t know why I am unable to subscribe to it. Is there anybody getting the same RSS problems? Anybody who knows the answer will you kindly respond? Thanks.
https://xn--2e0bu9hp5e8tmelv.com/
You ought to take part in a contest for one of the greatest websites on the net. I will highly recommend this web site!
https://werow.com/mod.php?mod=weblink&op=visit_link&url=https://insacret.org
Nicely put, Regards!
online casino italy online usa casinos casino online nl free bonus no deposit
When it is worn with a matching sweatshirt, trying cool throughout cold seasons turns into a cinch.
https://www.u-zo.com/ext_pg/external_link.php?gourl=https://www.bloglovin.com/@jeulnnuemyhn
Ladies who’re stylish and wish to have the most recent styles normally renew their wardrobes.
http://stroytehnadzor.com.ua/out.aspx?link=https://unsplash.com/@bCsGIkBFvihCLmPWN
A chatbot for customer service can fetch correct information from the database.
http://www.sinal.eu/send/?url=https://www.ameba.jp/profile/general/qbiwtibwsio/?account_block_token=LCBdhnuiWWfQmdxssXhadf3N12962qBU
For the beginning position, you may stage your shotgun in whatever prepared situation you normally use in your house.
https://globalhealthandtravel.com/redirect-to-partner?url=https://open.mit.edu/profile/01J9BC49676PS7JXEKTC4WCRRT/
The decorated finish of a scarf or shawl, the pallu, has separate panels of exquisite Phulkari workmanship with hanging designs.
http://adv.resto.kharkov.ua/openx/www/delivery/ck.php?ct=1&oaparams=2__bannerid=225__zoneid=8__cb=3e32a0e650__oadest=https://leetcode.com/u/dmolakztaqmbn/
Ans. There are several profitable companies you can begin with a capital of Rs.
http://higashiyotsugi.net/cgi-bin/kazoechao/kazoechao.cgi?url=https://maps.roadtrippers.com/people/8HMORYcWQW9ED?lng=-106.77766&lat=41.11498&z=3.30945
Look for the various choices out there out there to make the best choice of European wardrobe.
https://ygm.com.tr/Page/ChangeCulture?lang=en&returnUrl=https://es.pinterest.com/lyawerbrilu/
A design could also be as simple as a low-degree platform floating simply above the bottom or as complicated as a multilevel system of platforms and connectors that climb up or down a slope or stretch throughout the yard.
https://www.piregwan-genesis.com/liens/redirect.php?url=https://www.pearltrees.com/yojos
30 mins southeast of the city, Tybee Island Lighthouse is a “must see” for any self-proclaimed lighthouse nutter.
http://freestuffdirect.net/gotourl.php?link=https://www.4shared.com/u/yN0LjAyl/terriatlogin1988.html
Arched windows that recall the Palladian style conceived throughout the classical age by architect Andrea Palladio are a favorite characteristic in new houses right now and require particular window remedies.
https://martinsirmao.pt/admin/newsletter/redirect.php?id=241&email=7D&url=https://www.answers.com/u/lauconlicont1987
These patches happen on account of the habitat’s turnover.
https://www.u-zo.com/ext_pg/external_link.php?gourl=https://www.pearltrees.com/oitad
Sort M has purple markings and is available in versatile rolls and rigid tubing.
https://www.rias.si/knjiga/go.php?url=https://www.ameba.jp/profile/general/qrwfasceguvv/?account_block_token=FkW14EId9C8GZHzqM7UhLjxXjAlb9fYY
Retort-kind furnaces differ from different batch-kind furnaces in that they make use of a sealed lining known as a “retort”.
http://therapoetics.org/?wptouch_switch=desktop&redirect=https://solo.to/iisqtovldq
A pioneering documentary film about scuba diving in these lakes was made by Graham Ferreira within the early 1970s.
https://www.lucklaser.com/trigger.php?r_link=https://www.instructables.com/member/fuiJcsxdyIMzdU/?cb=1728029612608
Energy cables are usually stranding class A, B, or C. These lessons permit for the cable to be skilled right into a closing put in position where the cable will generally not be disturbed.
https://www.diamondfilms.com/idioma.php?id=1&ref=https://tinhte.vn/profile/c3zsu4yepp.3050164/
The place Can I Purchase Androgynous Clothing?
http://calas.lat/sites/all/modules/pubdlcnt/pubdlcnt.php?file=https://www.metal-archives.com/users/macdparkcen83macdparkcen
Calcutta: Hindu Patriot Press.
http://www.gymfan.com/link/ps_search.cgi?act=jump&access=1&url=https://es.pinterest.com/manstheafrima/
The local laws and regulations governing self-defense weapons in your area.
http://sinkinkousoku.com/?wptouch_switch=desktop&redirect=https://forum.ixbt.com/users.cgi?id=info:3E1871879
Who wouldn’t love this custom fire pit and seating area of their backyard?
https://tepco-partners.co.jp/wpstaff/?wptouch_switch=desktop&redirect=https://es.pinterest.com/comppuckirstan/
Very good advice. Thank you.
online casinos that accept $5 deposits usa casino online real money online casino rigged
Applications requiring a cable to be moved repeatedly, corresponding to for portable tools, more flexible cables referred to as “cords” or “flex” are used (stranding class G-M).
http://gotoandplay.biz/phpAdsNew/adclick.php?bannerid=30&zoneid=1&source=&dest=https://www.inkitt.com/svf6RcmYPPWANj
The closet has sufficient storage to organize clothes and day by day gadgets, but it isn’t massive sufficient to crowd the ground space.
http://www.brainflasher.com/out.php?goid=https://www.bloglovin.com/@ueetzgmpccn
Options the gorgeous appear and feel of cloth with the convenience of paper.
https://hodgsonlegal.com/?wptouch_switch=desktop&redirect=https://es.pinterest.com/sticpatfisi/
Connecting two excessive-voltage cables with each other poses two essential problems.
https://www.fequip.com.br/cliente/?idc=19&url=https://hubpages.com/@hphleucmead
Just 3 components make this flavorsome tremendous quick snack.
https://www.irisoptical.co.uk/shop.cfm?do=flipCurrencyC&return=http://66ffa7a835a6f.site123.me/
Beneficial info. Appreciate it!
az online casino real money no deposit best casinos in canada download online casino south africa
Fantastic material. Thanks a lot!
casino online bono sin deposito gratis casino online real money no deposit independent online casino uk
Wonderful posts. Appreciate it!
new online casinos real money 2021 online casino for real money beste online casino zahlungsmethoden
Hello, Neat post. There is a problem together with your site in web
explorer, could check this? IE still is the marketplace chief and a good section of
other people will leave out your great writing because of this
problem.
Feel free to surf to my web-site; golden visa portugal
You said it adequately.!
888 online casino uk best usa online casino fanduel pa online casino
Good facts. Regards!
nj casinos online gambling slots online casino new online casino no deposit sign up bonus
I absolutely love your site.. Great colors & theme. Did you make this website yourself? Please reply back as I’m hoping to create my very own site and want to know where you got this from or exactly what the theme is named. Kudos.
https://hlbam.com
An updated profile and approvals together with suggestions from handlers can make it easier to get marked by the best folks.
https://www.answers.com/u/enhallico1978
Probably the most elegant answers mirrors the window’s form within the window dressing.
https://gravatar.com/strangeryoungf373f6e82f
Hi, I do believe this is an excellent blog. I stumbledupon it 😉 I am going to come back yet again since I book marked it. Money and freedom is the greatest way to change, may you be rich and continue to help others.
https://www.damnbud.com/dispensary-near-me.html#/
Hello there! I just wish to give you a huge thumbs up for the excellent info you’ve got right here on this post. I’ll be returning to your web site for more soon.
https://www.damnbud.com/dispensary-near-me.html#/
How To Host A Powerful Party Any Party Planning Checklist 제주오피 (hjelm-aguilar.mdwrite.net)
Hi there! This article could not be written any better! Looking at this article reminds me of my previous roommate! He continually kept talking about this. I’ll forward this information to him. Fairly certain he’s going to have a very good read. Many thanks for sharing!
https://www.dermandar.com/user/ho88games/
Can I simply just say what a relief to find an individual who truly understands what they’re discussing online. You certainly realize how to bring a problem to light and make it important. More people must look at this and understand this side of the story. I was surprised that you aren’t more popular since you surely possess the gift.
https://chaturbatego.com
“I thought you usually showered after practice. In the locker room.” His dad asks as he walks into the open door of the bathroom. Garrett resumes the fondling of his cock while he takes long drawn-out whiffs from his sweat, piss and cum stained jockstrap.
Everything is very open with a very clear clarification of the challenges. It was truly informative. Your website is extremely helpful. Thanks for sharing!
https://win.gist.it/ContaClick.asp?id=1040&sito=fdownloader.at2F
This is a topic that’s near to my heart… Thank you! Exactly where can I find the contact details for questions?
https://www.mojbred.com/go.php?w=http3A2F2Ffdownloader.at2F
I used my teeth to strip off daddy’s black sheer socks. I placed them in my mouth and washed them with my saliva. I swallowed every single sweat and stink from these socks. It takes so well. I rolled them into a ball and stuck them into my jockstrap where my small dick and balls were. That night, I did a whole spa routine to make sure my skin was soft and my ass was stretched and wet. I was wearing nothing but a jockstrap as I was told. Waiting by the door on fourth. My heartbeat was so fast as my mouth was dry. I heard the footstep approaching. I left the door unlocked as one of the instructions I was received from daddy. He stepped in with his size 10 Christian Loublitine loafer where my eyes were going up from there. When I made eye contact with daddy, daddy slapped me across the face and said, “Bad boy, Where the fuck are your sneakers as I told you to wear tonight.” I was trembling and said in a very low voice, “ sorry daddy I fooooorgot.”
The payout for Adagio Teas is 8 on all items.
https://www.mobygames.com/user/1060386/zlwjjdgfncqez/
Do buddies who breakfast pay greater than ladies who lunch?
https://maps.roadtrippers.com/people/hnVJgQ0NfQgep7N?lng=-106.77766&lat=41.11498&z=3.30945
Its rocker midsole mimics the movement of a rocking chair to help scale back the energy required for every step.
https://lu.ma/user/usr-EcQobRmx3ANgnjA
You should be a part of a contest for one of the best websites on the net. I will highly recommend this blog!
https://www.damnbud.com/vapes.html#/
Additionally good is Uncle Tannous (2626 N. Halsted).
https://www.bloglovin.com/@qhxvngsmz
When you click on the thumbnail it should take you to the blog put up web page for the precise design file.
https://www.openstreetmap.org/user/bebusod49bebusod
In Brown, Sanborn Conner (ed.).
https://allmylinks.com/qvclguates
1. Halogens – These are very just like standard bulbs.
https://allmylinks.com/nkuwqjxbmgf
Subsequent time you watch your favorite Tv present, take a look at what the lead characters have on their toes.
https://pastebin.com/1izz53QP
Their styles are always altering, so you’ll need to take a look at all of the completely different kinds they’ve on Zappos.
https://pastebin.com/dY37yUax
Silver jewellery? You better believe it.
https://maps.roadtrippers.com/people/RK4NrNhWQWPoanD?lng=-106.77766&lat=41.11498&z=3.30945
Appearing as a wholesaler may help enhance product consciousness.
https://www.instructables.com/member/nUfxsHOdRQcNdrmz/?cb=1727790244219
The earliest form of health insurance (aside from life insurance coverage) was “accident” insurance.
https://allmylinks.com/ypmfwysbojtq
Keep in thoughts: As a result of the toebox is product of mesh, excessive pressure can wear it down extra easily.
http://taylorhicks.ning.com/profile/uasItCW
Buy durable provides of towels as an alternative.
https://my.archdaily.cl/cl/@eskotos26eskotos
Howdy! I could have sworn I’ve visited this website before but after looking at some of the articles I realized it’s new to me. Nonetheless, I’m definitely pleased I found it and I’ll be book-marking it and checking back regularly.
https://www.damnbud.com/vapes.html#/
Before we get to our checklist of the best travel shoes for men and women, we wish to share a bit of recommendation and high ideas for one of the best journey footwear.
https://unsplash.com/@GbCVEepQVSmuqDCJbR
First, as for those leftists who pretend that repeal of the Second Amendment shouldn’t be their goal – that they’re only advocating for “commonsense gun security legislation,” that pretense was dealt a blow this week.
https://pbase.com/deEZjBFyCuds
It is sort of doable that Sundblom wouldn’t have made the paintings, nor that they can be as broadly identified, if that they had not been ad illustrations.
https://leetcode.com/u/hlwhwjmjssjvl/
Saved as a favorite, I love your blog.
https://www.springsp.org/
I quite like looking through an article that can make people think. Also, many thanks for allowing me to comment.
https://www.nataliaohar.com/
You are so awesome! I do not think I’ve truly read anything like that before. So great to find another person with some unique thoughts on this topic. Really.. many thanks for starting this up. This site is one thing that is needed on the web, someone with some originality.
https://thaclassifieds.com/backpage-alternative/
Good information. Lucky me I discovered your website by accident (stumbleupon). I have saved as a favorite for later!
https://thaclassifieds.com/backpage-alternative/
I’m very pleased to find this site. I wanted to thank you for ones time just for this fantastic read!! I definitely savored every part of it and I have you book marked to look at new things in your website.
https://www.symbolrecords
He runs the towel through his curl-filled hair, and down over his chest, where the early signs of his manhood sprout like an uneven crop of hairs across his chest that run down to his furry-pillowed crotch. Where the throbbing from his hard-on springs back as the damp towel whips his erection back and forth with each swipe of the now dampened towel. “I think all of us were sprouting wood, today, dad.” He says. “Coach even noticed how hard we all were.”
Valuable info. With thanks!
migliori app casino online [url=https://usacasinomaster.com/#]online gambling casino[/url] instant withdrawal online casino
“Yeah.” He answers his dad. “…and I was ‘going commando’ too.” filmy porno He does not hear the slamming of the front door. Neither does he hear the footsteps on the wood floor in the hallway. The shower drowns away all this noise.
Many thanks. I enjoy it!
gta online casino heist disconnect glitch [url=https://luckyusaplay.com/#]online casino gambling[/url] majestic casino online
Amazing lots of beneficial data.
best online casinos new york [url=https://luckyusaplay.com/#]play casino games online[/url] juwa 777 online casino login download ios apk
Whoa quite a lot of valuable data!
andrew tate online casino online games casino online casino games 2019
Nicely put. Many thanks!
1 cent online casino live dealer online casino new online casinos australia 2023
Good postings. Thanks!
casino online deposito paypal online usa casino party poker online casino nj
Terrific information, With thanks.
casino online youtube [url=https://uscasinoguides.com/#]best usa online casinos[/url] jacks casino online
Wow a lot of useful knowledge!
vegas games online casino online betting casino safe online casino
Thanks, Great stuff.
online casino Г¶sterreich ohne einzahlung [url=https://usaplayerscasino.com/#]new online casinos for usa[/url] australian online casino instant withdrawal
Wow quite a lot of fantastic information!
200 online casino bonuses [url=https://usagamblinghub.com/#]online betting casino[/url] 21.com casino online
Thank you! Valuable information!
atlantic city casino play online best online casinos that payout usa best dutch online casino
Superb content. Cheers.
accounts teller online casino [url=https://usacasinomaster.com/#]casino online usa[/url] online casino that takes paypal
I think this is among the most important info for me.
And i’m glad reading your article. But want to remark on some general things, The web site style is
perfect, the articles is really excellent : D. Good job, cheers
Visit my website … Golden Visa Program
You mentioned that perfectly.
online casino bonus without deposit best online casinos that payout all slots casino online chat
Very good tips. Regards!
blackjack ballroom casino online [url=https://luckyusaplay.com/#]best online casino bonus[/url] siga online casino
Awesome facts. Thank you!
how to tell if online casino is legit legit online casino no deposit bonus online casino 2024
You reported that really well!
juegos casino online gratis brand new online casinos usa no deposit bonus welches online casino ist zu empfehlen
With thanks! I enjoy it.
online casinos that accept venmo [url=https://usaplayerscasino.com/#]best online usa casinos[/url] nya svenska casino online
Whoa many of beneficial knowledge.
best payout casino online uk best casinos online aplay online casino
Amazing postings. With thanks.
bank cheque online casino [url=https://usagamblinghub.com/#]top rated online casinos[/url] apuestas casino online argentina
Appreciate it. Numerous facts!
australian online casino no deposit bonus 2019 [url=https://luckyusaplay.com/#]usa casino online[/url] best online blackjack casino uk
You would possibly affiliate Denver extra with outside actions than nightlife-related actions, but Denver is actually a occasion-pleasant destination.
https://akushithu-net.ssl-xserver.jp/information/?wptouch_switch=desktop&redirect=https://industry-exxfl.xyz/archives/148/
They all performed the Star Wars theme track when the youngsters obtained sweet.
http://enews.sfera.net/newsletter/redirect.php?id=alfsqui@libero.it_0000002862_144&link=https://still-bzjzsi.xyz/archives/149/
Picnics additionally started out at members’ properties – Tom Hall and Bob Bartzokas hosted summer season picnics, scenes of very competitive Slip and Slide.
http://shibuya-naika.jp/?wptouch_switch=desktop&redirect=//dqgf-almost.xyz/archives/143/
We provide one hour lessons, one /two hour trail rides for individuals and groups, and more.
http://www.milan7.it/olimpia.php?u=https://wzaa-far.xyz/archives/162/
Chicago possesses an unimaginable diversity of good eating places, a truth not apparent to those whose data of Chicago is proscribed to Hyde Park and the Loop.
http://lacplesis.delfi.lv/adsAdmin/redir.php?uid=1439888198&cid=c3_26488405&cname=Oli&cimg=http://lacplesis.delfi.lv/adsAdmin/i/preview_610959355.jpeg&u=https://possible-gdlxce.xyz/archives/133/
Hi! I just want to give you a big thumbs up for your excellent info you’ve got here on this post. I’ll be returning to your web site for more soon.
https://uniqueexchange.store/
Very good blog post. I absolutely appreciate this website. Stick with it!
https://uniqueexchange.store/
Fine stuff. Kudos.
casino online i migliori casino online usa $1 minimum deposit online casino usa real money
Truly a lot of fantastic info.
dg online casino online live casinos quick hits online casino
You mentioned that fantastically!
best online casino indonesia [url=https://uscasinoguides.com/#]play casino online[/url] casino online gaming
Really loads of wonderful data.
online casino free spins no deposit canada casino online usa casino online free play
With thanks. I value this!
online casinos in [url=https://usaplayerscasino.com/#]online casino top rated[/url] gta online aggressive casino heist
This excellent website really has all of the information and facts I needed about this subject and didn’t know who to ask.
https://www.betthaizone.com/tag/สล็อตขนมหวาน/
You said it very well..
usa online casino real money no deposit new online casino usa ok jackpot games online casino
You made your point.
1 rated online casino [url=https://usagamblinghub.com/#]casino online no deposit bonus[/url] gta 5 online casino dlc update
I seriously love your website.. Pleasant colors & theme. Did you develop this web site yourself? Please reply back as I’m attempting to create my own blog and want to know where you got this from or what the theme is named. Cheers!
https://www.betthaizone.com/tag/สัมผัสทองคำ/
This is nicely said. .
online casino med zimpler [url=https://usacasinomaster.com/#]online casinos usa[/url] dragonfire limited casino game online
You actually expressed this very well.
online casino spielen in deutschland new online casino astra casino online
Many thanks, Ample material.
gta online best casino game online casino online casino bally slots
You revealed it perfectly.
juego online casino top 10 online casino online casinos that accept discover
Perfectly voiced really! .
live casino online games [url=https://uscasinoguides.com/#]online casino no deposit bonus codes[/url] best online casino in nz
Seriously tons of amazing advice.
online casino promotion codes new online casinos for usa free cash casino online
You stated this perfectly!
22bet online casino [url=https://usaplayerscasino.com/#]games casino free online[/url] online casinos vietnam
Helpful content. Kudos!
hippodrome online casino canada top 10 online casino indiana casinos online
Superb material. Appreciate it!
bandar judi casino sbc168 online [url=https://usagamblinghub.com/#]online casino free play no deposit[/url] rival powered online casinos
Cheers. An abundance of forum posts.
online casino dealer hiring [url=https://usacasinomaster.com/#]live online casino[/url] casino online con bonus gratis sin deposito
Regards! Loads of forum posts!
desert diamond casino online games casino free online online casino in pa
Nicely put, Thanks!
best austrian online casino [url=https://luckyusaplay.com/#]online casino bonus no[/url] casino slots games online free play
Very good information. Regards!
online casino comparison new online casino online casino legal
Fantastic write ups, Appreciate it!
top online casino georgia online american casinos casino online dinero real argentina
Appreciate it. Numerous posts!
best online casino game to win money [url=https://uscasinoguides.com/#]online casino no deposit[/url] new no deposit online casino bonus
With thanks. A lot of info!
casino city online game [url=https://usaplayerscasino.com/#]best usa online casino[/url] az online casino bonus
You have made the point!
la casino online online us casinos lucky bet casino online
Thank you! I like this.
are there any online casinos in the usa free online games casino online casino free credit no deposit
Terrific forum posts, Kudos!
hollywood casino online free games [url=https://usacasinomaster.com/#]games casino free online[/url] casino royale english movie online
Cheers, I like it!
versailles gold casino game online usa online casino lucky7even online casino
Nicely put. Thanks a lot!
station casinos online betting [url=https://luckyusaplay.com/#]best online casinos that payout usa[/url] online poker holland casino
I couldn’t resist commenting. Perfectly written!
https://thaclassifieds.com/
Thank you, I value this!
grand hotel casino online new online casino easiest withdrawal online casino
Your style is so unique compared to other folks I have read stuff from. Many thanks for posting when you have the opportunity, Guess I’ll just bookmark this site.
https://thaclassifieds.com/
In the meantime, back on the ranch, things are going effectively at Windchase.
http://dir.dir.bg/url.php?URL=https://sheds-wafer.xyz/archives/309/
The existence of the alignment tongue is an effective instance of the responsibilities of the Dungeon Grasp.
https://ggdata1.cnr.cn/c?z=cnr&la=0&si=30&cg=92&c=407&ci=88&or=385&l=568&bg=568&b=900&u=https://market-zgo.xyz/archives/179/
By likelihood Hoch met Rev.
https://tracking.wpnetwork.eu/api/TrackAffiliateToken?token=1fgpp3us0zB_2q0wS0eoC2Nd7ZgqdRLk&skin=ACR&url=https://improve-bueiz.xyz/archives/124/
He is elected to a 5-12 months time period by the overall Meeting, but his election might be vetoed by any of the everlasting members of the security Council.
http://xn--80adnhhsfckl.xn--p1ai/bitrix/redirect.php?event1=&event2=&event3=&goto=https://oo-kills.click/archives/262/
Once once more, an absence of evidence throws us back on imaginative sympathy of the type that is no longer a respectable fellow-traveller of historical past.
http://tsugarubrand.jp/blog/?redirect=https3A2F2Fyhuemw-vote.xyz/archives/107/&wptouch_switch=mobile
It was through the 1870s that Limoges finally perfected its porcelain process, and the items produced then are considered to be a few of the finest antique Limoges porcelain ever made.
https://www.stewarthaasracing.com/go.php?id=39&url=https://trade-fone.xyz/archives/150/
The International Court docket of Justice (a.k.a.
http://hao.vdoctor.cn/web/go?url=https://flap-mw.xyz/archives/255/
Do you have a particular doctor or hospital you need to be able to use?
https://www.svjono.lt/index.php?module=easy_gallery&method=show_image&w=800&h=800&t=auto&f=https://write-druq.xyz/archives/135/
Someway there had been that in his face that had made Johnny afraid to talk to him.
http://maps.google.com.vc/url?q=https://everybody-zqgna.xyz/archives/109/
If you are contemplating their purchase, keep 2 things in mind.
https://prapornet.ru/redirect?url=https://boterajordan.org/archives/268/
Teva Universal Trail Sandals: These are wonderful high quality, comfortable sandals that will probably final a long time.
http://cherel.ru/bitrix/rk.php?goto=https://teeth-bread.click/archives/248/
A faucet or tap is a gadget that regulates the quantity of water that’s launched by the pipes installed in chosen areas of your house, usually within the kitchen and bathroom.
http://waseem.nl/baby/gbook/go.php?url=https://uw-oxide.click/archives/251/
Pretty! This was a really wonderful post. Thank you for supplying these details.
https://thaclassifieds.com/bedpage
McMenamins says it plans to have totally different flavors of its Laborious Seltzer in the future, but as a tribute to its effectively-recognized Ruby Ale, Raspberry is the first.
https://vnedriupp.ru/bitrix/rk.php?goto=https://jewww-require.xyz/archives/118/
Mexico City release: July 1973; Three week run; Authorization: A Notes: This is considered one of my favourite Santo films, although I can no longer say for positive that it’s my most favourite; I additionally consider Santo vs.
http://maps.google.la/url?q=https://wjahrs-air.xyz/archives/127/
The long life of CFLs and significantly LEDs creates a relatively new downside in residential lighting.
http://cooltgp.org/tgp/click.php?id=370646&u=https://avef-prepare.xyz/archives/110/
Diverse neighborhoods, a thriving dwell music scene, an eclectic mixture of bars and a rising repute as a foodie destination all make Toronto an incredible place to go if you want to have fun nicely into the night.
http://konstruktor62.ru/bitrix/rk.php?goto=https://websitevaluestats.com/archives/282/
These are a nice different to Nike Air Force 1 or the Adidas Stan Smiths.
https://bnc.lt/a/key_live_pgerP08EdSp0oA8BT3aZqbhoqzgSpodT?medium=&feature=&campaign=&channel=&$always_deeplink=0&$fallback_url=https://evaenl-small.xyz/archives/124/
NOTES: This was James Wyatt’s last nice Gothic house, finished on his loss of life by his nephew Jeffry Wyatt (later Sir Jeffry Wyatville) who added the decrease buildings on the suitable in the drawing.
http://samoyede.ro/guestbook/go.php?url=https://zh-bones.xyz/archives/277/
John Chambers was raised in Charleston, West Virginia, within the 1950s, with a background that might hardly be described as provincial.
http://www.google.ch/url?q=https://aaxcgs-statement.xyz/archives/131/
As of April 7, in case you are an Argentinian citizen or resident, you’ll only need to fill in a sworn assertion about your vaccination status and confirm the absence of signs associated to Coronavirus inside forty eight hours previous to journey.
https://www.11rus.ru/r.php?jump=https://magazine-tuvqu.xyz/archives/200/
With thanks. Numerous material.
online real money casino apps [url=https://uscasinoguides.com/#]online casino live[/url] online casino stake7
You said it nicely..
online casinos ohne download online casino reviews best casino online casino
Position effectively utilized!.
como apostar en casino online [url=https://usagamblinghub.com/#]usa online casino no deposit[/url] online casino fraudsters
Regards. I enjoy it!
online casino no deposit bonus usa online casino paypal backgammon online casino
Thanks a lot, I like this!
australia. casino. online. real. money. [url=https://luckyusaplay.com/#]american casino online[/url] vegas sweeps online casino download apk
There are ample public spaces for guests to mingle with each other and with our staff.
https://www.streetvanners.be/guestbook/go.php?url=https://work-vqtkm.xyz/archives/140/
Our check pair was true to dimension, and there are various colours to choose from, including two-toned, patterned, and tie-dye shades.
http://udirect.ru/bitrix/redirect.php?goto=https://bejuo-family.xyz/archives/117/
When you have a Tough State of affairs and want quick and long lasting outcomes, CONTACT ME NOW for a free consultation.
http://neuro-research.ru/projects/logistics/services/redirect/act.php?url=https://limbs-racks.click/archives/300/
Quickly we took bus back to Hakone, the place there was one final location to explore for the day.
http://lcxhggzz.com/switch.php?m=n&url=https://coltonhaynes.org/archives/259/
Thanks for supporting our site and maintaining our designs free for all.
https://trubor.ru/bitrix/redirect.php?goto=https://buy-htxumt.xyz/archives/124/
What our editor says: “Everlane is all about chic, minimalist looks, and this flat is a bestseller,” says Molvar.
https://www.monaron.com/home/changecountry?countrycode=PL&returnurl=https3A2F2Fmouth-xhuxp.xyz/archives/139/
Other Vietnamese eating places are Nhu Hoa Cafe (1020 W. Argyle; also Laotian food), Nha Trang (1007 Argyle, superb eel curry; branch at 6632 Clark), Pho Xe Lua (1021 Argyle; big parts of Vietnamese noodles at absurdly low prices), Pho 777 (1065 Argyle), Pho Hung (1129 Argyle), Pho fifty four (1137 Argyle), Pho 888 (11•• Argyle), Mekong (4953 Broadway at nook of Argyle), Hung Vuong Palace (4801 Broadway), A Dong (4829 Broadway), Dong Ky (4877 Broadway), Dong Hung Vien and Dong Thanh (4925 Broadway), Fortunate Star (4941 Broadway), Pho Hoa (4965 Broadway), New Saigon (5000 Broadway), Dong Khanh (5027 Broadway), Danang (5029 Broadway), Thai Binh (1113 Argyle), Cafe Thu (1137 Argyle), Saigon Little Residence (6241 Clark), Vietnam Little Home (4654 N. Damen; amazingly cheap), Lucthan Dragon (4811 Lincoln), Nam Viet (6831 NW Highway), Vinh Phat Barbecue (4940 Sheridan), Hen Cafe (4533 N. Sheridan), Hoang Mai (5120 N. Sheridan), Mê Lanh (4770 N. Milwaukee), Vung Tau (2838 Broadway), Hue Thanh (1054 W. Argyle), Bale (5018 Broadway, a bakeryrestaurant whose identify means ‘Paris’; sandwiches of Vietnamese sausage on French bread are authentically Vietnamese), Le Bistro (5004 N. Sheridan), Mimosa (7130 W. Grand), Hong Ngoc (2411 W. North), Hong Ta (3035 Lawrence), Julie May’s Bistro (5025 Clark), Le Colonial (637 Rush), Quang’s Noodle (806 N. State), Asiana (2546 Clark), La Paillotte (3470 Clark), Nam Viet (6731 Northwest Hwy.), and three in Chinatown: Golden Bull (242 W. Cermak; a particular request may be needed to get them to give you the Vietnamese menu), Kim Yen (228 W. Cermak), and the spartan Saigon (232 W. Cermak).
https://grandcafedevriend.nl/wp-content/themes/eatery/nav.php?-Menu-=https://teach-hqeo.xyz/archives/141/
We recognize the enthusiasm that all our participants have for future programs and mirror it with our own.
http://m.nabeeya.net/nabee/go_link.html?cidx=8228&link=https://true-cpkc.xyz/archives/176/
Personally, I like to wear ankle socks with my good journey walking footwear and low reduce, no-present socks with my slip on, informal journey sneakers.
https://www.financialcenter.com/ads/redirect.php?target=https://spoke-grade.click/archives/274/
Basic D&D makes use of six polyhedral dice, with 4, six, eight, 10, 12 and 20 faces.
http://biokhimija.ru/links.php?go=https://whirl-blade.click/archives/250/
However understanding the important significance of distribution is just half the battle; a company’s preferrred distribution effort will depend on many specific issues which are unique to its business.
http://www.ip-piter.ru/go/url=https://bestpages.xyz/archives/278/
Fantastic stuff, Regards!
zamsino online casino best online casino reddit no deposit bonus hard rock casino online bonus code
Amazing facts. Appreciate it!
bovegas online casino [url=https://uscasinoguides.com/#]best online casino bonuses[/url] aristocrat online casinos
Wow plenty of wonderful tips.
mohegan casino online [url=https://usaplayerscasino.com/#]new online casino no deposit bonus usa[/url] online casino like stake.us
Wow lots of superb data.
5 star online casino top online casino how to win money on online casinos
This website was… how do you say it? Relevant!! Finally I’ve found something which helped me. Thanks!
http://limo24.limo/
You reported that wonderfully!
ga online casino [url=https://usagamblinghub.com/#]us online casinos[/url] online casino niedersachsen
Amazing facts. With thanks.
list of all online casino games best usa online casino rubyfortune casino online
Information well used!.
best online casino joining bonus [url=https://usacasinomaster.com/#]brand new online casinos usa[/url] casino royale free online streaming
You said it nicely..
best usa online casino fast payout online casinos erfahrungen online casino
Nicely voiced certainly. .
how to open online casino new usa online casinos online casinos that accept australian players
Hello there! This article couldn’t be written any better! Going through this article reminds me of my previous roommate! He continually kept preaching about this. I’ll forward this article to him. Fairly certain he’ll have a very good read. I appreciate you for sharing!
https://youtu.be/rv74EwXsmdU?si=MgTK76MOd5O2KreJ
Great material. With thanks!
online casinos vegas [url=https://usagamblinghub.com/#]top online casino[/url] gta online casino discount
Very good material, Thank you.
bandar judi casino sbc168 online best online casino casinos in canada online
Fantastic material. With thanks!
legal online casino usa [url=https://luckyusaplay.com/#]free online casinos[/url] beste online casino belgie
Greetings! Very helpful advice in this particular post! It is the little changes which will make the most important changes. Thanks a lot for sharing!
https://www.123-hd.me
You made some good points there. I looked on the web for more info about the issue and found most individuals will go along with your views on this web site.
https://www.123-hd.me
Systematic Investment Planning (SIP) Mutual Funds (75 investment in Massive Cap stocks) provide an average return of 17 every year.
https://www.pieceinvicta.com.pl/trigger.php?r_link=https3A2F2Fvrecycling.com.pl/
For the reason that mid-2000s, many extra firms are looking for to acquire alternate technique of danger transfer through alternate threat transfer packages.
http://www.naughtyallie.com/gals/pgals/p0077awrh/?link=https://sbsbtclucknow.com/
15 July 1905 – 2 December 1982) was a Pakistani politician and statesman who served as the fourth prime minister of Pakistan from 1955 till his resignation in 1956.
https://www.nejstromecky.cz/souhlas_cok.php?url=https://negaster-bastelstube.de/
Incredible quite a lot of valuable info!
pokies online casino australia https://uscasinoguides.com/poker-apps/ best bonus casinos online
Cheers. Loads of facts.
best online casino game to win money https://usaplayerscasino.com/north-carolina-casinos/ online casino spielautomaten
In total, Simons has given over $4 billion to philanthropic causes.
http://testing.swissmicrotechnology.com/redirect-forward.php?ste=0&url=https://ow-panorama.pl/finance/ighfpszykx/
I absolutely love your blog.. Pleasant colors & theme. Did you make this site yourself? Please reply back as I’m wanting to create my own blog and would like to find out where you got this from or just what the theme is called. Kudos!
https://www.123-hd.me
Though it is very easy to start your options trading journey, you will be required to conduct thorough analysis and research and make strategic decisions about your investments.
http://www.girlznation.com/cgi-bin/atc/out.cgi?id=50&l=side&u=https://palkat.info/finance/egczhuwxfn/
I seriously love your website.. Great colors & theme. Did you build this website yourself? Please reply back as I’m wanting to create my own site and would love to learn where you got this from or exactly what the theme is named. Thanks!
https://www.123-hd.me
Cheers! Helpful information!
bot casino online https://uscasinoguides.com/pennsylvania-casinos/ casino online sweden
Great forum posts. Regards!
big win casino online https://uscasinoguides.com/new-york-casinos/ inetbet online casino
Very good blog post. I absolutely love this site. Continue the good work!
https://tubidy44322.p2blogs.com/29207506/tubidy-tutorial-for-beginners-in-which-way-to-get-through-as-well-as-download-media-easily
Appreciate it. An abundance of information!
parx online casino app https://usacasinomaster.com/real-money-roulette/ casino holdem online free
This site certainly has all of the info I wanted concerning this subject and didn’t know who to ask.
https://heylink.me/linetogel008
You actually mentioned it well.
eye of horus online casino https://usagamblinghub.com/poker-real-money/ gta online casino heist guns blazing
You definitely made your point.
nude online casino https://usagamblinghub.com/xbet-review/ agen casino maxbet online
Your style is very unique in comparison to other people I have read stuff from. Many thanks for posting when you have the opportunity, Guess I’ll just book mark this site.
https://lyds.pl/
You suggested this really well.
casinos online bonus sem deposito https://usagamblinghub.com/xbet-review/ mr beast online casino real
I love it when people get together and share opinions. Great site, keep it up!
https://make-shots.com
You actually expressed that adequately.
best canada casino online 2022 https://usaplayerscasino.com/illinois-casinos/ online casino mit cashback
Good article! We will be linking to this great content on our site. Keep up the great writing.
https://acheterpermisdeconduire.org/les-questions-du-permis-de-conduire-en-2024/
You actually explained it superbly.
me beast online casino https://usagamblinghub.com/ufc-betting/ mit online casino geld verdienen
You expressed that exceptionally well.
cyprus online casino license https://usagamblinghub.com/live-casinos/ legit real money online casinos
Kind 10-Ok (Report). Equitrans Midstream (February 21, 2023).
https://www.art2dec.co/mag/include/click_counter.php?url=https://air-lsnpkk.xyz/archives/34/
Coordinated Common Time (UTC) has since changed Greenwich Imply Time (GMT) because the world time standard.
https://www.123juist.de/banner.pl?id=stuv&url=https3A2F2Fogyqu-lawyer.xyz/archives/80/
In 2014, the magazine named Meghan Stabler one in all its Working Mothers of the 12 months, making her the first overtly transgender lady to obtain that honor.
http://xn--o1aahd8c.xn--p1ai/bitrix/redirect.php?event1=click_to_call&event2=&event3=&goto=https://yaeeh-together.xyz/archives/37/
Such an trade rate supplied great revenue for Soviet military and celebration officials.
http://www.google.no/url?sa=t&source=web&cd=1&sqi=2&ved=0CBwQFjAA&url=https://name-lurmc.xyz/archives/79/
Thompson’s report was accomplished in November 2002, however its launch was hotly debated.
https://www.ponaflexusa.com/en/redirect?productid=266&url=https://vowop-entire.xyz/archives/75/
In August 2007, the Corps released an analysis revealing that their floodwalls were so poorly designed that the maximum safe load is barely 7 ft (2.1 m) of water, which is half the original 14-foot (4.Three m) design.
http://www.gymfan.com/link/ps_search.cgi?access=1&act=jump&url=https://doradcapodatkowyjmlipa.pl/archives/144/
Terrific material. Thanks a lot!
the newest online casinos https://luckyusaplay.com/real-money-keno/ online casino roulette scams
Excellent post. I’m going through a few of these issues as well..
https://quick-tv.com
May I simply say what a relief to uncover a person that truly understands what they’re discussing over the internet. You definitely realize how to bring a problem to light and make it important. More people must look at this and understand this side of your story. I was surprised you’re not more popular given that you certainly possess the gift.
https://quick-tv.com
You actually suggested that superbly!
online casino payment processors https://uscasinoguides.com ar online casino
Very well voiced of course. !
win real cash casino online https://usaplayerscasino.com/michigan-casinos/ gta online banned from casino
Thanks, A good amount of posts!
rivers casino sports betting online https://usaplayerscasino.com/boxing-betting/ casino online betsson
Thanks! Useful information!
online phone casino https://usaplayerscasino.com/arizona-casinos/ best ash gaming online casinos
Kudos! Valuable stuff.
lucky star casino online https://usagamblinghub.com/nba-betting/ online casino 120 free spins
Very good information. Many thanks!
start my own online casino https://usagamblinghub.com/betonline-review/ glory casino online game
Many thanks. Good stuff.
casino esc online https://usaplayerscasino.com/mybookie-review/ bbc online casino
I could not resist commenting. Exceptionally well written.
https://thaclassifieds.com/bedpage/
That is a great tip particularly to those fresh to the blogosphere. Simple but very accurate information… Thank you for sharing this one. A must read article!
https://thaclassifieds.com/bedpage/
Профессиональный сервисный центр по ремонту бытовой техники с выездом на дом.
Мы предлагаем: ремонт бытовой техники в москве
Наши мастера оперативно устранят неисправности вашего устройства в сервисе или с выездом на дом!
Thanks a lot, An abundance of advice!
https://usagamblinghub.com/crash-games/
Great article, I’ve bookmarked this page and have a feeling I’ll be returning to it often.
http://king-wifi.win//index.php?title=normanbeach3601
Hello there! I could have sworn I’ve been to this web site before but after going through some of the posts I realized it’s new to me. Anyhow, I’m definitely pleased I found it and I’ll be book-marking it and checking back often.
https://casino5588.com
Your style is so unique compared to other folks I’ve read stuff from. Thank you for posting when you’ve got the opportunity, Guess I’ll just bookmark this site.
https://casino5588.com
prawo jazdy na autobus
Kudos! Terrific information.
https://uscasinoguides.com/crypto-casinos/
I’m extremely pleased to uncover this site. I wanted to thank you for your time due to this wonderful read!! I definitely appreciated every part of it and i also have you saved to fav to see new things in your site.
https://808truck.com
Having read this I thought it was rather enlightening. I appreciate you finding the time and energy to put this informative article together. I once again find myself spending a lot of time both reading and commenting. But so what, it was still worth it!
https://808truck.com
This may be the proper weblog for anybody who wants to check out this topic. You realize a great deal of its practically tricky to argue with you (not too I just would want…HaHa). You actually put a fresh spin on the topic thats been discussing for a long time. Great stuff, just wonderful!
https://www.muskelbody.info/forum/member.php/88133-gasengineers858
It was something of great contentment getting to your site recently. I arrived here this day hoping to find out something new. I was not disappointed. Your ideas on new strategies on this area were enlightening and a fantastic help to me personally. Thank you for creating time to write down these things as well as for sharing your ideas.
https://tagoverflow.stream/story.php?title=choosing-the-best-materials-for-your-kitchen-cabinets#discuss
Pretty! This has been an incredibly wonderful post. Thanks for supplying this info.
https://www.damnbud.com/ounceofweed.html#/
This is a great tip especially to those new to the blogosphere. Simple but very precise info… Many thanks for sharing this one. A must read article.
https://www.damnbud.com/ounceofweed.html#/
Grudin, J. (1988). “Why CSCW purposes fail: issues within the design and analysis of organization of organizational interfaces”.
http://litset.ru/go?https://focus-xijhv.xyz/archives/25/
If the toilet is positioned in or close to a corner, these solutions may be an appropriate compromise.
https://perezvoni.com/blog/away?url=https3A2F2Fnewspaper-vvqqfp.xyz/archives/40/
In this era, customer satisfaction is most vital than anything.
http://www.smilingdeath.com/RigorSardonicous/guestbook/go.php?url=https://augitedelachute.com/archives/137/
By the end of 2019, 75 percent of adult population in Indonesia is expected to have access to formal financial services.
https://jobstatesman.com/jobclick/?RedirectURL=https://wd-friday.click/archives/142/&Domain=jobstatesman.com&rgp_m=read23&et=4495
The new company’s first CEO, vested with full authority to characterize Stellantis, was Carlos Tavares, the former president of the PSA managing board, in addition to former CEO of PSA Group, with a 5-yr time period as Stellantis CEO.
http://jobbullet.com/jobclick/?RedirectURL=https://bar-xll.xyz/archives/67/
There’s definately a great deal to know about this topic. I like all the points you have made.
https://thenextweb.com/news/january-latin-america-tech-news-shouldnt-miss-last-month
You have made some really good points there. I checked on the internet to find out more about the issue and found most people will go along with your views on this site.
http://www.thaclassifieds.com/
It’s hard to come by knowledgeable people for this topic, however, you seem like you know what you’re talking about! Thanks
http://www.thaclassifieds.com/
The Retail Sales Index is released at 8:30 am EST around the 12th of the month; it reflects data from the previous month.
http://www.travelcenter.gr/index.php?lang=ger&url=https3A2F2Fogbv-threat.xyz/archives/72/
This software handles probability and cost as it concerns profits and loss.
http://cgi-wsc.alfahosting.de/extras/public/photos.cls/selection/addAll?cc=0.653810755815357&accountId=AAHS10INX3Z1&filter=&redirectUrl=https://camera-funl.xyz/archives/39/
Utility computing is a term used to describe a pay-as-you-go model for supplying IT resources on demand.
https://tracking.wpnetwork.eu/api/TrackAffiliateToken?token=1fgpp3us0zB_2q0wS0eoC2Nd7ZgqdRLk&skin=ACR&url=https://tails-jl.xyz/archives/151/
Accompanying the decrease in the number of shares outstanding is a reduction in company assets, in particular, cash assets, which are used to buy back shares.
https://adbr.com.au/?ads_click=1&data=6350-6348-0-4846-1&redir=https://flare-sheet.xyz/archives/124/&c_url=http://cutepix.info/sex/riley-reyes.php
This prompted analysts, together with Ruth Gregory, deputy chief UK economist at Capital Economics, to counsel the Chancellor would have room to make potential tax cuts.
http://www.cmm.com.tw/admin/Portal/LinkClick.aspx?tabid=93&table=Links&field=ItemID&id=340&link=https://movetrymy.xyz/archives/124/
It’s awesome to see people fulfilling their dreams and getting exposure for their hard work!
http://lemanpub.ch/ads/www/delivery/ck.php?ct=1&oaparams=2__bannerid3D457__zoneid3D10__cb3Ddbd88406b8__oadest3Dhttps3A2F2Ftinselgurus.net/archives/140/
Pembina Pipeline reported 2022 revenues of CAN$11.611 billion.
http://www.hsi-chang-lai.com.tw/admin/Portal/LinkClick.aspx?field=ItemID&id=434&link=https3A2F2Fspee-whom.xyz/archives/49/&tabid=114&table=Links
This page definitely has all of the information I wanted concerning this subject and didn’t know who to ask.
https://casinosmalaysia.com/
You’re so cool! I do not suppose I have read anything like that before. So nice to discover someone with some unique thoughts on this subject matter. Really.. many thanks for starting this up. This site is something that is required on the web, someone with some originality.
https://casinosmalaysia.com/
I was excited to uncover this page. I want to to thank you for your time for this fantastic read!! I definitely enjoyed every little bit of it and i also have you book-marked to check out new things in your web site.
https://www.porn-xxx.jp.net/คลิปหลุด/คริปหลุด-bestzabzeed-พี่เบสควย-56-ตั้/
Nice post. I learn something new and challenging on blogs I stumbleupon everyday. It will always be interesting to read articles from other authors and practice something from other websites.
https://www.porn-xxx.jp.net/คลิปหลุด/ติดหนี้พนันบอล/
Oh my goodness! Impressive article dude! Thank you so much, However I am having difficulties with your RSS. I don’t understand why I cannot subscribe to it. Is there anybody else getting similar RSS problems? Anyone that knows the solution can you kindly respond? Thanx.
https://www.bobres-iptv.com/
Good post. I learn something new and challenging on sites I stumbleupon on a daily basis. It’s always useful to read through content from other writers and practice something from other web sites.
https://prodronessupply.com/
I love it when people get together and share thoughts. Great blog, stick with it.
https://somarandmoon.com/blogs/oh-my-goddess/heal-your-inner-girl-a-simple-3-step-method-for-inner-child-healing
An outstanding share! I’ve just forwarded this onto a co-worker who had been doing a little research on this. And he in fact ordered me lunch because I discovered it for him… lol. So allow me to reword this…. Thanks for the meal!! But yeah, thanks for spending the time to talk about this matter here on your website.
https://somarandmoon.com/blogs/oh-my-goddess/heal-your-inner-girl-a-simple-3-step-method-for-inner-child-healing
I’m pretty pleased to find this website. I wanted to thank you for your time for this particularly fantastic read!! I definitely savored every part of it and i also have you book marked to look at new stuff on your website.
https://tau.edu.ng/publications/
I couldn’t resist commenting. Exceptionally well written!
https://oer.tau.edu.ng/
It’s difficult to find experienced people in this particular topic, however, you seem like you know what you’re talking about! Thanks
https://itemblast.com/
You need to take part in a contest for one of the highest quality sites online. I will recommend this web site!
https://itemblast.com/
The very next time I read a blog, Hopefully it won’t fail me as much as this particular one. I mean, Yes, it was my choice to read, but I genuinely thought you would have something useful to talk about. All I hear is a bunch of complaining about something that you could fix if you weren’t too busy searching for attention.
https://teletype.in/@tairikvipco
Everything is very open with a very clear explanation of the issues. It was definitely informative. Your website is extremely helpful. Many thanks for sharing!
https://kifira.com/stainless-steel-raised-cat-food-bowl-with-non-slip-base/
Can I just say what a relief to uncover a person that actually knows what they’re talking about over the internet. You certainly know how to bring an issue to light and make it important. More people ought to read this and understand this side of your story. It’s surprising you’re not more popular since you most certainly possess the gift.
https://kifira.com/stainless-steel-raised-cat-food-bowl-with-non-slip-base/
I couldn’t refrain from commenting. Exceptionally well written.
https://wwg.mp3juice.day
I really love your website.. Excellent colors & theme. Did you make this amazing site yourself? Please reply back as I’m wanting to create my own site and would love to find out where you got this from or just what the theme is named. Appreciate it.
https://www.tvseriesclub.me/tag/2-days-1-night-season-4-ซับไทย-คิมซอนโฮ-123/
Way cool! Some extremely valid points! I appreciate you writing this article and the rest of the site is extremely good.
https://opentutorials.org/profile/175162
An outstanding share! I have just forwarded this onto a co-worker who has been conducting a little homework on this. And he in fact bought me lunch because I found it for him… lol. So allow me to reword this…. Thank YOU for the meal!! But yeah, thanx for spending time to talk about this topic here on your web site.
https://www.angrybirdsnest.com/members/k8betink/profile/
Excellent article! We are linking to this particularly great post on our site. Keep up the great writing.
https://upliftingmobility.com/
Your style is very unique compared to other people I’ve read stuff from. I appreciate you for posting when you have the opportunity, Guess I’ll just book mark this web site.
https://xo88.istanbul
Good article. I’m facing many of these issues as well..
https://www.porn-secret.com/tag/คลิปหลุดแพรว
An impressive share! I’ve just forwarded this onto a friend who was doing a little research on this. And he actually ordered me dinner due to the fact that I stumbled upon it for him… lol. So let me reword this…. Thanks for the meal!! But yeah, thanks for spending some time to talk about this matter here on your web site.
https://www.overseries.me/tag/a-life-time-love-ลำนำรักเทพสวรรค์-ล่าส/
Aw, this was a really good post. Taking the time and actual effort to produce a superb article… but what can I say… I hesitate a lot and don’t manage to get nearly anything done.
https://www.overseries.me/tag/da-vinci-s-demons-อัจฉะริยะสะท้านโลก-ปี/
You need to take part in a contest for one of the finest websites online. I will highly recommend this blog!
https://www.nihao-series.com/tag/good-job-2022-พากย์ไทย-บ้านซีรี่ย์
After I initially commented I appear to have clicked the -Notify me when new comments are added- checkbox and from now on each time a comment is added I get 4 emails with the exact same comment. Is there a means you can remove me from that service? Many thanks.
https://www.nihao-series.com/tag/call-it-love-koreandrama
Better chance of capital appreciation – As you can buy investment properties in emerging markets and can choose below market value (BMV) properties, your investment will have a better chance of capital appreciation.
https://creditotitan.co/visit-partner?partner_id=seo-7&partner_url=https://hire-a-hubby.com/&channel=seo
Very good article. I certainly appreciate this website. Stick with it!
https://www.fanseries.org/tag/immortal-samsara-ซับไทย
order deflazacort – cheap deflazacort pill brimonidine without prescription
After looking over a few of the blog articles on your web site, I seriously appreciate your technique of blogging. I saved it to my bookmark site list and will be checking back soon. Take a look at my website too and tell me how you feel.
https://www.dooseries.vip/tag/bad-prosecutor-ซับไทย-ep-1
Having read this I thought it was rather enlightening. I appreciate you spending some time and effort to put this article together. I once again find myself personally spending a lot of time both reading and posting comments. But so what, it was still worth it.
https://www.disney-plus.jp.net/tag/ซีรี่ย์-harrow-season-1/
I’m amazed, I have to admit. Rarely do I come across a blog that’s both educative and amusing, and without a doubt, you have hit the nail on the head. The issue is something which not enough people are speaking intelligently about. Now i’m very happy that I came across this in my hunt for something concerning this.
https://www.disney-plus.jp.net/tag/ซีรี่ย์เกาหลี-legal-high-ซับไทย/
Hello there! I just want to offer you a huge thumbs up for your excellent info you’ve got here on this post. I will be returning to your website for more soon.
https://www.chineseseries.net/tag/the-gift-season-1-บรรยายไทย/
I love it when individuals get together and share ideas. Great site, keep it up.
https://www.chineseseries.net/tag/blind-viu/
Hi, I do think this is an excellent website. I stumbledupon it 😉 I am going to revisit once again since I book-marked it. Money and freedom is the greatest way to change, may you be rich and continue to help others.
https://www.123hd.tv/tag/ซีรี่ย์a-life-time-love-ลำนำรักเทพสวร/
You made some good points there. I looked on the internet to find out more about the issue and found most people will go along with your views on this web site.
https://www.123hd.tv/tag/เกียร์สีขาวกับกาวน์สีฝ/
Eligible employees are those who have worked for your company for at least 12 months and 1,250 hours during those 12 months.
http://xn--22cap5dwcq3d9ac1l0f.com/bitrix/redirect.php?goto=https://kb-alias.xyz/
After an EIA, the precautionary and polluter pays principles may be applied to decide whether to reject, modify or require strict liability or insurance coverage to a project, based on predicted harms.
https://beam.jpn.org/rank.cgi?mode=link&url=https://strangestways.com/
Everything is very open with a very clear explanation of the challenges. It was definitely informative. Your site is very helpful. Thank you for sharing!
https://emilianoacfgj.timeblog.net/64954038/formas-de-obtener-canciones-de-ytb-instrucciones-para-usar-notube-y-transformar-a-mp3-o-mp4
You can choose a compatible wallet from the list that appears and then continue with the connection process.
http://grandmaporn.xyz/away/?u=https://themiccgroup.com/store/ws0dwe6g0a/
They need to interconnect their applications flexibly to help do business goals.
https://jobschaser.com/jobclick/?Domain=jobschaser.com&RedirectURL=https3A2F2Fradio-mb.com/store/vladq8vvvn/&et=4495&rgp_d=link7
Your style is unique in comparison to other people I’ve read stuff from. I appreciate you for posting when you have the opportunity, Guess I’ll just book mark this web site.
https://thaclassifieds.com/facebook-marketplace-for-classified-ads/
I need to to thank you for this excellent read!! I absolutely loved every bit of it. I have you book marked to look at new things you post…
https://www.outdoorproject.com/users/789win-bot
I needed to thank you for this wonderful read!! I absolutely enjoyed every little bit of it. I’ve got you saved as a favorite to check out new things you post…
https://doodleordie.com/profile/betvisash
Great site you have got here.. It’s hard to find high quality writing like yours these days. I truly appreciate individuals like you! Take care!!
https://www.dooseries.vip/tag/ดูซีรี่ย์-autumn-cicada-2020-สายลับจักจ
Excellent post. I’m experiencing a few of these issues as well..
https://bit.ly/3WIC7zh
Good post. I learn something totally new and challenging on blogs I stumbleupon every day. It will always be useful to read articles from other authors and use something from their websites.
https://www.chineseseries.net/tag/ดูตำนานรัก-ตำนานพิศวง-บร/
May I simply say what a comfort to discover someone who genuinely understands what they’re talking about on the web. You definitely know how to bring an issue to light and make it important. More people must look at this and understand this side of your story. I was surprised you are not more popular because you definitely possess the gift.
https://www.123hd.tv/tag/ดูซีรี่ย์ฝรั่ง-harrow-season-3-2021-ผ่าคด/
This blog was… how do I say it? Relevant!! Finally I have found something which helped me. Many thanks.
https://thaclassifieds.com/
You need to be a part of a contest for one of the highest quality sites on the net. I’m going to highly recommend this web site!
https://thaclassifieds.com/
You ought to be a part of a contest for one of the finest sites online. I most certainly will highly recommend this website!
http://www.fuckcraigslist.com/
71-72 and “Capital” as contained in the Collected Works of Karl Marx and Frederick Engels: Volume 35, pp.
https://www.prima.ee/ru/go/to/https/apkraptor.com/
Hi, I do think this is a great site. I stumbledupon it 😉 I am going to come back yet again since I book-marked it. Money and freedom is the greatest way to change, may you be rich and continue to help other people.
https://scrapbookmarket.com/story17790935/los-principios-bC3A1sicos-de-descargar-mC3BAsica-gratis
Potential immigrants applied for visas at U.S.
http://go.takbook.com/index.php?url=https://newguider.site/
This site really has all the information and facts I wanted concerning this subject and didn’t know who to ask.
http://www.disneymagicessentials.com/
Hi, I do believe this is a great site. I stumbledupon it 😉 I will revisit once again since I book-marked it. Money and freedom is the best way to change, may you be rich and continue to help other people.
http://www.disneymagicessentials.com/
This web site truly has all of the information and facts I needed concerning this subject and didn’t know who to ask.
http://www.shopdecordeals.com/
cyclosporine brand – buy colchicine tablets colchicine canada
I want to to thank you for this fantastic read!! I certainly enjoyed every little bit of it. I’ve got you bookmarked to look at new stuff you post…
https://fileforum.com/profile/nurseengine3/
I was able to find good information from your content.
https://www.123-hd.me/tag/ซีรี่ย์ออนไลน์-grid
I blog frequently and I seriously appreciate your content. Your article has really peaked my interest. I will book mark your site and keep checking for new information about once a week. I opted in for your RSS feed too.
https://bit.ly/3SKmUNf
An outstanding share! I’ve just forwarded this onto a co-worker who was conducting a little research on this. And he actually ordered me lunch simply because I discovered it for him… lol. So let me reword this…. Thanks for the meal!! But yeah, thanks for spending some time to talk about this subject here on your website.
https://www.jimjeans.com/
Your style is unique in comparison to other folks I have read stuff from. I appreciate you for posting when you have the opportunity, Guess I’ll just bookmark this page.
https://hackerone.com/fun88lgbt
Aw, this was an incredibly good post. Taking the time and actual effort to create a great article… but what can I say… I procrastinate a whole lot and never manage to get anything done.
https://sk.gravatar.com/sunwinrepair
Having read this I thought it was extremely informative. I appreciate you spending some time and energy to put this short article together. I once again find myself spending way too much time both reading and commenting. But so what, it was still worth it!
https://dadazpharma.com/question/sunwin-cong-game-sun-win-uy-tin-sunwin-repair/
An impressive share! I’ve just forwarded this onto a friend who has been doing a little research on this. And he in fact ordered me lunch simply because I discovered it for him… lol. So allow me to reword this…. Thank YOU for the meal!! But yeah, thanks for spending some time to talk about this issue here on your site.
https://opentutorials.org/profile/172669
wonderful post, very informative. I’m wondering why the other specialists of this sector don’t understand this. You should continue your writing. I am sure, you have a great readers’ base already! rent a car kosovo
https://veilstep1.bravejournal.net/the-hidden-dangers-of-undetected-leakages-why-leak-detection-is-necessary
drug addiction is a menace to the society, it destroys lives and it destroys the community::
https://www.webwiki.fr/wimbledonleakdetection.londonleakdetection.net/index.html
That would be some inspirational stuff. Couldn’t know that opinions is usually this varied. Many thanks lots of enthusiasm to give such information here.
https://atavi.com/share/wr5dowzry7nl
This blog really is good. How was it made ?
https://www.metooo.co.uk/u/669a0a2a57db9822bdd5e19f
Thanks for all of your work on this blog. My mother really loves managing investigations and it’s really obvious why. A lot of people know all of the compelling method you create very important strategies on this web blog and as well recommend response from visitors on the matter so my daughter is now studying so much. Take pleasure in the rest of the new year. Your carrying out a fantastic job.
https://diigo.com/0wvgns
This is really interesting, You’re a very skilled blogger. I have joined your feed and look forward to seeking more of your magnificent post. Also, I have shared your web site in my social networks!
https://tupalo.com/en/users/7040271
This is a really good tip particularly to those new to the blogosphere. Simple but very accurate information… Many thanks for sharing this one. A must read article.
https://livesexarena.com
i frequent hair salons because i always want to keep my hair in top shape..
https://www.dermandar.com/user/threadocean2/
Hey there guys, newbie here. I’ve lurked about here for a little while and thought I’d take part in! Looks like you’ve got quite a good place here
https://olderworkers.com.au/author/cherrymcclanahan370sassmails-com/
There’s definately a great deal to find out about this subject. I like all the points you made.
https://rakyatkecil.online/
After looking into a handful of the articles on your website, I seriously appreciate your technique of writing a blog. I book-marked it to my bookmark webpage list and will be checking back in the near future. Take a look at my website too and let me know your opinion.
https://rakyatkecil.online/
??? ??????? ????? ????? ???? ???? ????? ??????? ?????? ???? ?????? ????
https://peatix.com/user/23087180
Are not they in a hurry? Do not they want to find the outpost? Need not Kirk get back to the ship? Yet they sit there, having a talk and barbecue around a log fire.
http://lovewiki.faith/index.php?title=barrerafarmer6823
Last month, when i visited your blog i got an error on the mysql server of yours.,`’,”
https://willysforsale.com/author/timebill9/
you’re really a good webmaster. The website loading speed is incredible. It seems that you are doing any distinctive trick. Furthermore, The contents are masterwork. you have performed a great process on this topic!
https://heavenarticle.com/author/parrotfine5-437256/
Youre so cool! I dont suppose Ive read anything like this before. So nice to find any individual with some unique thoughts on this subject. realy thank you for beginning this up. this website is something that is needed on the net, someone with a little originality. useful job for bringing one thing new to the web!
http://wiki.iurium.cz/index.php?title=westergaarderickson0951
Spot on with this write-up, I truly feel this website needs a lot more attention. I’ll probably be back again to see more, thanks for the info.
https://convertidor-mp3-de-a-yout62602.blogdomago.com/28293814/las-principales-herramientas-libres-para-transformar-youtube-a-formato-mp3
Hello there! This blog post couldn’t be written any better! Looking through this article reminds me of my previous roommate! He always kept preaching about this. I most certainly will forward this post to him. Pretty sure he’ll have a good read. Thank you for sharing!
https://hellcasepromocode.com/
I went over this internet site and I believe you have a lot of fantastic information, saved to favorites (:.
https://www.metooo.it/u/669ad5906ffe32118a142e21
Will you mind generally if I mention a couple of your blogposts providing that I give you credit and even sources returning to your web sites? My web-site is in the similar market as your own and my users will profit from several of the help and advice your site offer in this article. Please be sure to let me know if it is okay for you. Kind regards!
https://notabug.org/beamcatsup8
i’ve always been watching How I Met Your Mother, this comedy show is really great~
https://glamorouslengths.com/author/ferryyew9
Way cool! Some very valid points! I appreciate you writing this post and the rest of the website is also really good.
https://kktix.com/user/3990107
I was very pleased to discover this web site. I need to to thank you for ones time for this wonderful read!! I definitely liked every bit of it and i also have you bookmarked to check out new information in your website.
https://www.beatstars.com/whitescreendevOYZ/about
An outstanding share! I’ve just forwarded this onto a friend who was doing a little research on this. And he actually bought me dinner simply because I discovered it for him… lol. So allow me to reword this…. Thanks for the meal!! But yeah, thanx for spending time to talk about this issue here on your web site.
https://entrarr.com/vipto/
This site really has all of the info I needed concerning this subject and didn’t know who to ask.
https://www.jimjeans.com/custom-jeans/denim-jackets
I blog often and I seriously thank you for your content. This article has really peaked my interest. I will book mark your site and keep checking for new information about once a week. I subscribed to your Feed as well.
https://www.jimjeans.com/custom-jeans/denim-shorts
Greetings, Might I grab your page snapshot and employ it on my personal blog site?
http://mozillabd.science/index.php?title=oliverosborn2770
Duties of property management include accepting rent, responding to and addressing maintenance issues, ,
https://anekdotoes.ru/user/cocoajury6/
Who designed your website. I think you did a good job.
https://aprelium.com/forum/profile.php?mode=viewprofile&u=peonybudget0
What¡¦s Happening i’m new to this, I stumbled upon this I’ve found It positively helpful and it has helped me out loads. I am hoping to give a contribution & aid different customers like its aided me. Good job.
https://squareblogs.net/peanutkiss0/avoid-expensive-water-damages-with-leak-discovery-solutions
stainless kitchen sinks serves me better and they are stain resistant too*
https://www.hulkshare.com/creditbutton9/
That is a good tip particularly to those new to the blogosphere. Short but very accurate info… Thank you for sharing this one. A must read article.
https://casinogmsdeluxe.com/
Oh my goodness! Impressive article dude! Thanks, However I am encountering problems with your RSS. I don’t understand the reason why I am unable to subscribe to it. Is there anybody having similar RSS problems? Anyone that knows the answer can you kindly respond? Thanks!!
https://casinogmsdeluxe.com/
This situation document appears to redeem a good deal of audience. Determine how to market it? The idea provides a amazing completely unique distort onto stuff. Reckon offering anything proper or alternatively great offer information about is central to the subject.
https://www.webwiki.com/hammersmithleakdetection.londonleakdetection.net/index.html
Keep up the wonderful piece of work, I read few posts on this web site and I believe that your blog is very interesting and has sets of fantastic info .
https://www.webwiki.ch/highgateleakdetection.londonleakdetection.net/index.html
Good post. I learn something new and challenging on sites I stumbleupon every day. It will always be helpful to read through articles from other writers and practice a little something from their sites.
https://thaclassifieds.com/alternative-to-backpage/
thank you for a really fascinating read, i hope you would do a follow up article considering i can never go through enough on this topic
https://fileforum.com/profile/veilbutton5/
Wow, incredible blog format! How lengthy have you been blogging for? you make running a blog glance easy. The full glance of your site is fantastic, as smartly the content material!
https://www.metooo.io/u/669a450f57db9822bdd62097
When I originally commented I appear to have clicked on the -Notify me when new comments are added- checkbox and from now on whenever a comment is added I receive four emails with the exact same comment. Is there a way you can remove me from that service? Thank you.
http://www.shobiphotography.com/
This is a topic which is near to my heart… Best wishes! Exactly where are your contact details though?
https://www.wallspot.org/ca/artist/profile/whitescreendev/
Everything is very open with a clear clarification of the challenges. It was truly informative. Your site is extremely helpful. Thank you for sharing!
https://writexo.com/share/n7actqw
I think other web-site owners should take this website as a model – very clean and excellent style and design, as well as the content. You are an inspriation in this topic!
https://vuf.minagricultura.gov.co/Lists/Informacin20Servicios20Web/DispForm.aspx?ID=8614777
There are very plenty of details like that to think about. This is a fantastic point out retrieve. I provide thoughts above as general inspiration but clearly you will find questions including the one you talk about the place that the most essential factor will likely be doing work in honest good faith. I don?t know if guidelines have emerged about such thinggs as that, but I am sure that the job is clearly defined as a reasonable game. Both youngsters glance at the impact of simply a moment’s pleasure, for the rest of their lives.
https://zenwriting.net/rootleg4/the-ultimate-guide-to-leak-detection-protect-your-building-now
Everything is very open with a clear clarification of the challenges. It was really informative. Your site is useful. Thanks for sharing!
https://butterflykisses.store/collections/baby-turbans
The posh distributed could be described as distinctive; customers are actually yearning for bags is a Native aspirations. Which strange surroundings is built that is to market diversity furthermore importance with travel and leisure market trends. hotels special offers
https://www.dermandar.com/user/peonyclover3/
Hello, I do think your blog may be having browser compatibility problems. When I look at your website in Safari, it looks fine however, if opening in IE, it’s got some overlapping issues. I merely wanted to give you a quick heads up! Aside from that, great website.
https://butterflykisses.store/products/blue-green-pink-purple-yellow-peach-colour-twisted-ribbon-bow-headband
Hello there! I could have sworn I’ve visited your blog before but after browsing through some of the posts I realized it’s new to me. Nonetheless, I’m certainly happy I discovered it and I’ll be bookmarking it and checking back often!
https://hypothes.is/users/mibetyoga
hollywood movies are always big budgeted and they have some great graphics and pretty actresses too,,
https://olderworkers.com.au/author/norrisbendsen286sassmails-com/
This is a topic that’s near to my heart… Thank you! Where are your contact details though?
https://writexo.com/6623one
I blog often and I really appreciate your content. This great article has truly peaked my interest. I will book mark your blog and keep checking for new information about once per week. I subscribed to your RSS feed as well.
https://linkmix.co/24885910
Wow this definitely takes me back, where are your contact details hmm?
https://www.webwiki.co.uk/actonleakdetection.londonleakdetection.net/index.html
my baby enjoys playing on the baby swing, baby swings can really make your baby happy~
https://unsplash.com/@sampanwoman4
Oh my goodness! Awesome article dude! Many thanks, However I am going through issues with your RSS. I don’t understand why I can’t subscribe to it. Is there anybody else getting the same RSS issues? Anyone who knows the answer will you kindly respond? Thanx!!
https://wmart.kz/forum/user/170972/
oral oxcarbazepine – buy trileptal 600mg sale levoxyl medication
I discovered your site site on google and check many of your early posts. Preserve inside the really good operate. I extra the RSS feed to my MSN News Reader. Seeking toward reading far more within you at a later time!…
https://www.webwiki.fr/walthamstowleakdetection.londonleakdetection.net/index.html
Greetings! Very useful advice in this particular article! It is the little changes that make the largest changes. Thanks for sharing!
https://dglonet.com/rikviptours
Well I truly enjoyed reading it. This subject offered by you is very helpful for accurate planning.
https://www.webwiki.ch/walthamstowleakdetection.londonleakdetection.net/index.html
camping have been the best activity that we can have during the summer, i love to roast marshmallows on a campfire..
https://www.hulkshare.com/cinemacatsup8/
It’s nearly impossible to find knowledgeable folks on this topic, but the truth is could be seen as do you know what you are dealing with! Thanks
http://shenasname.ir/ask/user/bikeappeal2
Way cool! Some extremely valid points! I appreciate you writing this post plus the rest of the site is also really good.
https://qiita.com/shakibalhasan
Way cool! Some extremely valid points! I appreciate you penning this post plus the rest of the site is extremely good.
https://mzansicontainers.co.za
I have been surfing online more than three hours today, yet I never found any interesting article like yours. It’s pretty worth enough for me. Personally, if all website owners and bloggers made good content as you did, the net will be much more useful than ever before.
https://www.webwiki.at/roehamptonleakdetection.londonleakdetection.net/index.html
Have you tried twitterfeed on your blog, i think it would be cool.”*.“
https://www.webwiki.co.uk/raynesparkleakdetection.londonleakdetection.net/index.html
It really is rare to come across a specialist in whom you may have some confidence. In the world in the present day, nobody genuinely cares about showing others the best way in this matter. How fortunate I am to have found a real wonderful blog as this. It’s people like you exactly who make a true difference nowadays through the concepts they write about.
https://www.webwiki.it/shoreditchleakdetection.londonleakdetection.net/index.html
Some genuinely interesting details you have written. Assisted me a lot, just what I was looking for : D.
https://tupalo.com/en/users/7031310
If you happen to acquiring a substantial repayment, you have to keep in mind what quantity of money you could be deducting coming from paydays or maybe spending money on for quarterly income taxes.
https://atavi.com/share/wqck3qz1t1lor
You can receive such stock market tips via paid membership at an online trading platform.
http://firstbaptistloeb.org/System/Login.asp?Referer=https://himitsukichi-store.net/articles/6ecs7d/
Good work, I was doing a google search and your site came up for short sales in Oviedo, FL but anyway, I have had a pleasant time reading it, keep it up!
https://www.northwestu.edu/?URL=https://nottinghillleakdetection.londonleakdetection.net/index.html
I have observed that in the world the present day, video games are classified as the latest rage with children of all ages. There are times when it may be unattainable to drag the kids away from the games. If you want the best of both worlds, there are plenty of educational activities for kids. Thanks for your post.
https://www.webwiki.nl/newmaldenleakdetection.londonleakdetection.net/index.html
Generally Are generally Diet ‘s an very affordable and flexible food regimen product suitable for induced the boycott . endeavouring to fast and as a result subsequently conserve a vibrant lifespan. lose weight
https://olderworkers.com.au/author/newellpage534sassmails-com/
some stores have really bad customer service while others have topnotch custmer service,,
http://shenasname.ir/ask/user/templebudget5
I undoubtedly didn’t understand that. Learnt some thing new nowadays! Thanks for that.
https://wayranks.com/author/eightbill8-511799/
I would like to thank you for the efforts you have put in penning this site. I’m hoping to check out the same high-grade content from you in the future as well. In truth, your creative writing abilities has motivated me to get my own site now 😉
https://forum.acronis.com/it/user/685153
Can I just say thats a relief to get a person that truly knows what theyre discussing on the web. You actually understand how to bring a concern to light and produce it important. The diet need to read this and can see this side with the story. I cant believe youre not more well-liked since you undoubtedly contain the gift.
http://153.126.169.73/question2answer/index.php?qa=user&qa_1=iraqleg4
BR sells their items under five applications with name of ice cream, cakes, sundaes, beverages and prepacks. They have other promotional packages individually or as subprogram of any other programs.
https://thegadgetflow.com/user/sheridanwooten840
I together with my friends came reading the nice information and facts on your website and all of the sudden I got a terrible suspicion I had not expressed respect to the web blog owner for those strategies. Those young men became absolutely happy to study all of them and have now simply been tapping into these things. Appreciate your being simply accommodating as well as for going for some amazing resources millions of individuals are really desperate to know about. My personal honest regret for not expressing gratitude to earlier.
https://www.metooo.io/u/668a6551a6e8b311b1527cd8
I just could not depart your web site prior to suggesting that I actually enjoyed the standard information a person provide for your visitors? Is going to be back often in order to check up on new posts
https://wayranks.com/author/creditstamp4-499018/
This is the best weblog for anyone who desires to find out about this topic. You notice a lot its virtually laborious to argue with you (not that I really would want aHa). You positively put a new spin on a topic thats been written about for years. Nice stuff, simply great!
https://www.webwiki.it/hollowayleakdetection.londonleakdetection.net/index.html
There’s definately a great deal to know about this subject. I like all of the points you’ve made.
https://casino5588.com
There’s certainly a great deal to know about this topic. I like all of the points you made.
https://casino5588.com
I was very pleased to find this web site. I need to to thank you for your time due to this fantastic read!! I definitely savored every little bit of it and I have you bookmarked to see new information in your web site.
https://tubidy69135.canariblogs.com/a-newcomer-s-book-to-tubidy-s-more-advanced-elements-44143709
Fantastic goods from you, man. I have understand your stuff previous to and you’re just too excellent. I really like what you’ve acquired here, certainly like what you are stating and the way in which you say it. You make it entertaining and you still take care of to keep it wise. I can’t wait to read much more from you. This is actually a wonderful web site.
https://fileforum.com/profile/capcrack1/
Good info. Lucky me I discovered your blog by accident (stumbleupon). I have bookmarked it for later.
https://badgarnituur.nl
This is really stimulating, You’re a truly capable blogger. I’ve signed up with your feed additionally expect reading your excellent write-ups. Moreover, We’ve shared your webpage with our social networking sites.
https://kingranks.com/author/sackleg1-612181/
Thanks a lot for sharing this with all folks you actually know what you’re talking about! Bookmarked. Please additionally seek advice from my site =). We may have a link trade arrangement between us!
https://www.metooo.es/u/6686bb9326ad05118bd06021
Greetings! Very helpful advice within this article! It is the little changes which will make the most significant changes. Thanks a lot for sharing!
https://neukjepaard.nl/
My spouse and i got quite joyous when Chris could finish off his investigations through the ideas he had out of the web page. It is now and again perplexing to simply possibly be giving for free secrets that many some people might have been selling. And we also realize we have the writer to thank for that. These explanations you have made, the simple web site navigation, the relationships you can give support to foster – it’s got mostly exceptional, and it’s really letting our son and the family do think the situation is interesting, which is wonderfully pressing. Many thanks for the whole thing!
https://tupalo.com/en/users/7030123
I think other site proprietors should take this website as an model, very clean and excellent user genial style and design, let alone the content. You’re an expert in this topic!
https://www.webwiki.nl/hackneyleakdetection.londonleakdetection.net/index.html
When I originally commented I clicked the -Notify me when new surveys are added- checkbox and from now on whenever a comment is added I am four emails using the same comment. Will there be however you may remove me from that service? Thanks!
https://www.webwiki.nl/harlesdenleakdetection.londonleakdetection.net
I hope you never stop! This is one of the best blogs Ive ever read. Youve got some mad skill here, man. I just hope that you dont lose your style because youre definitely one of the coolest bloggers out there. Please keep it up because the internet needs someone like you spreading the word.
https://peatix.com/user/23024932
After looking into a number of the blog articles on your website, I honestly appreciate your way of blogging. I book marked it to my bookmark site list and will be checking back soon. Take a look at my website as well and let me know your opinion.
https://animecartoonstickers.net
I absolutely love your website.. Great colors & theme. Did you create this site yourself? Please reply back as I’m planning to create my own personal site and would like to learn where you got this from or exactly what the theme is named. Thank you.
https://www.besttaste.com.sg/
I really want to thank you for yet another great informative post, I’m a loyal reader to this blog and I can’t tell you how much valuable tips I’ve learned from reading your content. I really appreciate all the effort you put into this great blog.
https://www.metooo.it/u/6689f571a6e8b311b1522d13
Excellent blog here! Also your web site loads up fast! What host are you using? Can I get your affiliate link to your host? I wish my website loaded up as quickly as yours lol
https://notabug.org/ferrybill2
Prince of Persia is the best, i really like the lead actor and also the princess, the princess is very pretty.,
https://www.webwiki.nl/finsburyparkleakdetection.londonleakdetection.net/index.html
It’s difficult to find knowledgeable people during this topic, but you appear to be what happens you are talking about! Thanks
https://www.mapleprimes.com/users/sampangrouse1
Excellent read, I just passed this onto a colleague who was doing a little research on that. And he just bought me lunch because I found it for him smile Thus let me rephrase that: Thank you for lunch!
https://timestamp9.bloggersdelight.dk/2024/07/05/avoid-water-damage-with-regular-leak-discovery-upkeep/
Nice post. I discover something more challenging on diverse blogs everyday. It will always be stimulating to read content from other writers and employ a little from their site. I’d choose to use some together with the content in this little blog regardless of whether you do not mind. Natually I’ll provide a link on the internet weblog. Appreciate your sharing.
https://qooh.me/peanutclover2
Reading your post made me think. Mission accomplished I guess. I will write something about this on my blog. …
https://rentry.co/f5apcwt5
They are adequately qualified to provide answers to a number of questions that the investor might need answers for.
https://www.dimar-group.ru:443/bitrix/rk.php?goto=https://enavicom.net/
I dugg some of you post as I thought they were extremely helpful handy
https://wikimapia.org/external_link?url=https://earlsfieldleakdetection.londonleakdetection.net/index.html
The the next occasion I just read a weblog, I hope so it doesnt disappoint me as much as this blog. After all, It was my choice to read, but I really thought youd have something intriguing to state. All I hear is actually a lot of whining about something that you could fix if you ever werent too busy looking for attention.
https://www.longisland.com/profile/bikejury6
cheap hytrin 1mg – order flomax online priligy for sale online
It is best to participate in a contest for among the best blogs on the web. I will suggest this web site!
https://www.webwiki.nl/claptonleakdetection.londonleakdetection.net/index.html
Good info, good to be knowledge and distributed to the public
http://www.sorumatix.com/user/alarmfrown3
Regards for all your efforts that you have put in this. Very interesting information.
https://squareblogs.net/sampanlarch7/leak-detection-101-top-devices-and-methods-to-determine-pipes-issues
Thanks , I have recently been searching for info approximately this subject for a long time and yours is the greatest I’ve discovered till now. But, what in regards to the conclusion? Are you positive in regards to the supply?
https://www.multichain.com/qa/index.php?qa=user&qa_1=cinemafrown0
Found at a corner on Mohammed Ali Road, this location has two doors. When you get inside of and go up, there seem to be rooms following rooms just after rooms. It is all perplexing, but just let the waiters guideline you. As soon as settled, consider some time to take a look at the menu. There are exceptional “Tawa-taka-tak” goods and “Raan” dishes. You can get a crack at paya soup, seekh kebabs, chicken tandoori and chicken afghani. Seekh kebabs are superior. The tandoori rotis are exceptional. They also have destinations where they serve other things like snacks, faloodas, kulfis etc.
https://www.metooo.io/u/668e4aae26ad05118bd80f48
Excellent read, I just passed this onto a friend who was doing a little study on that. And he really bought me lunch because I discovered it for him smile So let me rephrase that: Thanks for lunch!
https://www.strumentazioneoftalmica.it/author/pisceskiss3
there are portable wine coolers which also fit in a small office space. i use them in my home office**
http://www.stes.tyc.edu.tw/xoops/modules/profile/userinfo.php?uid=2028026
I would like to thnkx for the efforts you’ve put in writing this website. I am hoping the same high-grade blog post from you in the upcoming as well. In fact your creative writing skills has encouraged me to get my own web site now. Really the blogging is spreading its wings rapidly. Your write up is a good example of it.
https://www.webwiki.it/catfordleakdetection.londonleakdetection.net/index.html
I blog frequently and I seriously thank you for your content. Your article has truly peaked my interest. I am going to take a note of your blog and keep checking for new details about once per week. I subscribed to your Feed too.
https://www.jimjackets.com/custom-jackets/suit-jackets
I truly love your website.. Excellent colors & theme. Did you develop this site yourself? Please reply back as I’m looking to create my own personal blog and would like to know where you got this from or just what the theme is called. Cheers!
https://www.jimjackets.com/custom-jackets/satin-jackets
very nice put up, i definitely love this website, keep on it
https://zenwriting.net/canoelarch4/drip-discovery-saving-your-home-and-your-cash
There are some interesting points at some point in this post but I do not know if they all center to heart. There exists some validity but I most certainly will take hold opinion until I look into it further. Very good article , thanks so we want a lot more! Added onto FeedBurner likewise
https://www.dermandar.com/user/peanutcatsup5/
cooking is my passion and a hobby for me, besides, i love to eat lots of foods*
https://www.longisland.com/profile/capclover6
I appreciate your wordpress design, wherever did you obtain it from?
https://cocoafine5.edublogs.org/2024/07/14/auto-draft/
My favorite city out of all I’ve been to, no doubt about it that its St Gallen Switzerland. Switzerland just has this nice connotation about it. Something I absolutely love, it is peacefull and comforting.
http://ezproxy.cityu.edu.hk/login?url=https://bromleyleakdetection.londonleakdetection.net/index.html
I’ve also been meditating on the very same matter myself recently. Happy to see another person on the same wavelength! Nice article.
https://www.webwiki.it/brentfordleakdetection.londonleakdetection.net/index.html
I rattling lucky to find this website on bing, just what I was looking for : D too saved to favorites .
https://www.webwiki.it/brentfordleakdetection.londonleakdetection.net/index.html
I’m impressed, I must say. Actually rarely should i encounter a weblog that’s both educative and entertaining, and let me tell you, you’ve hit the nail within the head. Your thought is outstanding; the thing is something that too little consumers are speaking intelligently about. I’m happy that we came across this during my hunt for some thing in regards to this.
https://blogfreely.net/rootemery4/drip-discovery-101-tips-and-tricks-for-diy-homeowners
It hard to find knowledgeable individuals on this matter, however you sound like you understand what you are talking about! Thanks
https://wayranks.com/author/routerwoman0-518468/
I really appreciate this post. I have been looking all over for this! Thank goodness I found it on Bing. You’ve made my day! Thank you again
https://p3dm.ru/user/eightfine3/
Can I just now say what a relief to seek out one who in fact knows what theyre dealing with on-line. You actually understand how to bring a concern to light and make it important. Lots more people need to see this and understand why side in the story. I cant believe youre less common since you also certainly hold the gift.
https://mcgee-parrish-3.blogbright.net/leak-detection-your-finest-protection-versus-water-damage
Howdy sir, you have a really nice blog layout ,
https://www.webwiki.com/bermondseyleakdetection.londonleakdetection.net/index.html
This is my first time I have visited your site. I found a lot of interesting information in your blog. From the tons of comments on your posts, I guess I am not the only one! keep up the great work.
https://is.gd/9cZ1ap
I’m sure we have a trouble with your websites utilising Safari web browser.
https://moiafazenda.ru/user/cocoaclover1/
been using these things. We appreciate you getting really accommodating and then for utilizing certain amazing themes most people are really desirous to be
https://blogfreely.net/sampanbat7/stealthy-leakages-exactly-how-to-spot-common-signs-of-water-damages
clay garden pots are great but if you want a cheaper alternative, you can always use those plastic garden pots`
https://www.dermandar.com/user/bikecatsup7/
Thanks for all of your work on this web site. Debby enjoys engaging in research and it is easy to understand why. My spouse and i hear all concerning the
https://glamorouslengths.com/author/clientstep7
I must express my passion for your generosity for people who must have assistance with this particular niche. Your very own commitment to getting the message up and down had become extraordinarily valuable and have constantly permitted associates like me to get to their ambitions. The helpful guideline denotes so much a person like me and additionally to my colleagues. Thanks a ton; from each one of us.
https://willysforsale.com/author/airbuswine2/
I have discovered that smart real estate agents all over the place are getting set to FSBO Advertising and marketing. They are acknowledging that it’s more than merely placing a sign post in the front area. It’s really regarding building relationships with these retailers who later will become consumers. So, when you give your time and energy to encouraging these retailers go it alone – the “Law associated with Reciprocity” kicks in. Good blog post.
https://willysforsale.com/author/alarmyew7/
Subsequently, after spending many hours on the internet at last We’ve uncovered an individual that definitely does know what they are discussing many thanks a great deal wonderful post
https://www.fruitpickingjobs.com.au/forums/users/veilkiss0/
Hi! I just would like to give a huge thumbs up for the great info you have here on this post. I will be coming back to your blog for more soon.
https://posteezy.com/lost-and-discovered-how-leak-detection-can-save-you-time-and-money
You’re so interesting! I don’t suppose I have read a single thing like this before. So great to find someone with a few original thoughts on this topic. Seriously.. many thanks for starting this up. This site is one thing that is required on the internet, someone with a bit of originality.
https://bonus-sans-depot.casino/casinos-en-ligne/kings-chance-casino/
Oh my goodness! Impressive article dude! Thank you so much, However I am having troubles with your RSS. I don’t understand the reason why I can’t subscribe to it. Is there anybody having similar RSS problems? Anybody who knows the solution will you kindly respond? Thanks.
https://www.klikx.net/
Howdy! This article could not be written any better! Going through this article reminds me of my previous roommate! He continually kept talking about this. I’ll forward this post to him. Fairly certain he’ll have a good read. Many thanks for sharing!
https://www.klikx.net/
After looking at a number of the articles on your site, I really like your way of blogging. I book marked it to my bookmark webpage list and will be checking back in the near future. Take a look at my website as well and tell me your opinion.
https://soundcloudto.com/
May I simply say what a relief to uncover somebody that truly understands what they are discussing online. You definitely realize how to bring an issue to light and make it important. More people ought to read this and understand this side of your story. It’s surprising you’re not more popular because you certainly possess the gift.
https://soundcloudto.com/
This web site certainly has all the information and facts I wanted about this subject and didn’t know who to ask.
https://hasthip.com/collections/diamond-painting-kit
Very nice blog post. I absolutely love this site. Thanks!
https://hasthip.com/collections/wall-hanger
Hello there! This blog post couldn’t be written much better! Looking through this article reminds me of my previous roommate! He constantly kept preaching about this. I am going to forward this information to him. Fairly certain he’s going to have a great read. Thank you for sharing!
https://trip.tsip.universitasbumigora.ac.id/
After looking at a number of the blog posts on your website, I truly appreciate your way of blogging. I saved it to my bookmark website list and will be checking back soon. Please check out my web site too and tell me your opinion.
https://trip.tsip.universitasbumigora.ac.id/
There is definately a lot to learn about this topic. I love all of the points you made.
https://atlasbladi.com/cgi-sys/suspendedpage.cgi
I blog frequently and I truly appreciate your information. Your article has really peaked my interest. I’m going to take a note of your blog and keep checking for new details about once a week. I opted in for your Feed too.
https://music26159.blogoxo.com/28777759/a-straightforward-key-for-tubidy-introduced
Having read this I thought it was rather informative. I appreciate you taking the time and effort to put this information together. I once again find myself spending a significant amount of time both reading and posting comments. But so what, it was still worthwhile.
https://atlasbladi.com/cgi-sys/suspendedpage.cgi
There is certainly a great deal to know about this topic. I love all of the points you made.
https://www.lifetechnology.com/pages/health-news
I seriously love your site.. Very nice colors & theme. Did you build this site yourself? Please reply back as I’m looking to create my very own website and want to learn where you got this from or just what the theme is called. Thank you!
https://chromewebstore.google.com/detail/galileo-fx-news-notifier/aodfibmfglljaebgpbhfipejfnlblmio
This is a topic which is near to my heart… Many thanks! Where are your contact details though?
https://chromewebstore.google.com/detail/galileo-fx-news-notifier/aodfibmfglljaebgpbhfipejfnlblmio
Can I simply just say what a comfort to discover someone who really knows what they are talking about over the internet. You definitely realize how to bring a problem to light and make it important. More people need to look at this and understand this side of the story. I can’t believe you aren’t more popular given that you surely possess the gift.
https://crappie-fishing-in-ohio.blogspot.com
Good post. I am going through some of these issues as well..
https://helpful-engineering-insights.blogspot.com
Greetings! Very helpful advice within this post! It’s the little changes that will make the most important changes. Many thanks for sharing!
https://franciscoxiqxg.aboutyoublog.com/29485241/ytmp3-judgment-best-youtube-to-mp3-downloader-in-2024
May I simply say what a comfort to uncover someone that truly knows what they’re discussing on the net. You actually understand how to bring a problem to light and make it important. A lot more people need to check this out and understand this side of your story. I was surprised that you aren’t more popular since you most certainly have the gift.
https://www.canadavisa.com/canada-immigration-discussion-board/members/iwin68shop.1215667/
Having read this I believed it was very informative. I appreciate you taking the time and energy to put this informative article together. I once again find myself spending a lot of time both reading and posting comments. But so what, it was still worthwhile!
https://digitaltibetan.win/wiki/User:Iwin68shop
Howdy, There’s no doubt that your web site could be having browser compatibility problems. Whenever I take a look at your site in Safari, it looks fine however, if opening in IE, it’s got some overlapping issues. I merely wanted to give you a quick heads up! Apart from that, fantastic blog!
https://iwin68.shop/game-bai/
I enjoy reading a post that can make men and women think. Also, thanks for allowing for me to comment.
https://iwin68.shop/author/tom-dwan/
After looking over a number of the blog articles on your web page, I really like your technique of writing a blog. I added it to my bookmark site list and will be checking back in the near future. Please check out my website too and let me know your opinion.
https://www.jimjackets.com/
This site certainly has all the information and facts I wanted about this subject and didn’t know who to ask.
https://www.jimjackets.com/
Hello there! I just would like to give you a huge thumbs up for your excellent information you have got here on this post. I’ll be coming back to your web site for more soon.
https://winkienglish.edu.vn/
Very good article! We will be linking to this great content on our site. Keep up the great writing.
https://winkienglish.edu.vn/
You have made some decent points there. I looked on the internet for more info about the issue and found most people will go along with your views on this website.
https://newpolitic.com/recommended-korean-baccarat-sites-5/
Good day! I just want to offer you a huge thumbs up for the great information you’ve got right here on this post. I am coming back to your web site for more soon.
https://newpolitic.com/recommended-korean-baccarat-sites-5/
I really like reading an article that will make people think. Also, many thanks for allowing me to comment.
https://bc163.cc/
Hello! I just want to offer you a huge thumbs up for the excellent info you’ve got right here on this post. I’ll be returning to your blog for more soon.
https://bc163.cc/
I was able to find good info from your articles.
https://weblicht.sfs.uni-tuebingen.de/weblichtwiki/api.php?action=https://codyxkqc537.edublogs.org/2024/07/20/must-see-temples-in-kyoto-a-simple-definition-2/ travel japan insurance
The next time I read a blog, Hopefully it won’t fail me just as much as this one. I mean, Yes, it was my choice to read, nonetheless I actually thought you’d have something interesting to say. All I hear is a bunch of moaning about something you could possibly fix if you were not too busy searching for attention.
https://www.myessaywriter.ai/
Pretty! This has been an extremely wonderful post. Thanks for providing this info.
http://x-ray.ucsd.edu/mediawiki/api.php?action=https://dominickoiyv.bloggersdelight.dk/2024/07/16/10-undeniable-reasons-people-hate-japan-travel-planning/ {japan travel|travel japan|japan travel guide|esim japan travel|travel insurance japan|travel to japan|japan travel sim|japan travel app|japan web travel|japan official travel app|japan travel blog|japan travel insurance|japan travel web|travel japan website|esim for japan travel|travel insurance in japan for foreigners|travel japan web|japan travel navitime|japan travel planner|rakuten travel japan|japan travel by navitime|ptt japan travel|e travel japan registration|japan travel agency|navitime japan travel|travel in japan|travel quotes japan|travel agency in japan|caption for japan travel|japan travel sim card|cute japan travel quotes|travel requirements from japan to philippines 2023|travel agency in japan for foreigners|sim card japan travel|japan travel tips|japan quotes travel|japan travel sim 使えない|japan travel qr code|bcd travel japan|e travel japan|e travel japan to philippines|japan e travel|japan travel recommend|japan travel quotes|japan travel kk|japan travel ptt|japan travel website|japan travel esim|e travel pass japan|travel sim japan|solo travel japan|e travel registration japan|travel japan wifi|japan wonder travel|travel agency japan|japan travel requirements 2023|travel itinerary sample japan|japan travel map|japan travel card|travel sim card in japan|travel japan qr code|travel japan insurance|japan travel sim 日本人|japan to philippines travel requirements|e travel qr code japan|luxury travel japan|japan hands free travel|japan travel english|japan travel restrictions|japan travel plan|e travel pass japan requirements|navitime for japan travel|travel itinerary japan|japan travel itinerary|luggage free travel japan|verizon travel pass japan|travel adapter japan|hands free travel japan|travel to philippines from japan requirements|travel to australia from japan|japan travel pass|japan travel captions|japan travel kyoto|japan hands-free travel|travel insurance japan to europe|travel insurance from japan|travel sim card japan|japan travel news|travel insurance for japan|travel esim japan|travel
I really like reading an article that will make men and women think. Also, thanks for allowing me to comment.
http://notoprinting.xsrv.jp/feed2js/feed2js.php?src=https://codyxkqc537.edublogs.org/2024/07/20/20-questions-you-should-always-ask-about-hidden-gems-in-hokkaido-before-buying-it/ {japan travel|travel japan|japan travel guide|esim japan travel|travel insurance japan|travel to japan|japan travel sim|japan travel app|japan web travel|japan official travel app|japan travel blog|japan travel insurance|japan travel web|travel japan website|esim for japan travel|travel insurance in japan for foreigners|travel japan web|japan travel navitime|japan travel planner|rakuten travel japan|japan travel by navitime|ptt japan travel|e travel japan registration|japan travel agency|navitime japan travel|travel in japan|travel quotes japan|travel agency in japan|caption for japan travel|japan travel sim card|cute japan travel quotes|travel requirements from japan to philippines 2023|travel agency in japan for foreigners|sim card japan travel|japan travel tips|japan quotes travel|japan travel sim 使えない|japan travel qr code|bcd travel japan|e travel japan|e travel japan to philippines|japan e travel|japan travel recommend|japan travel quotes|japan travel kk|japan travel ptt|japan travel website|japan travel esim|e travel pass japan|travel sim japan|solo travel japan|e travel registration japan|travel japan wifi|japan wonder travel|travel agency japan|japan travel requirements 2023|travel itinerary sample japan|japan travel map|japan travel card|travel sim card in japan|travel japan qr code|travel japan insurance|japan travel sim 日本人|japan to philippines travel requirements|e travel qr code japan|luxury travel japan|japan hands free travel|japan travel english|japan travel restrictions|japan travel plan|e travel pass japan requirements|navitime for japan travel|travel itinerary japan|japan travel itinerary|luggage free travel japan|verizon travel pass japan|travel adapter japan|hands free travel japan|travel to philippines from japan requirements|travel to australia from japan|japan travel pass|japan travel captions|japan travel kyoto|japan hands-free travel|travel insurance japan to europe|travel insurance from japan|travel sim card japan|japan travel news|travel insurance for japan|travel esim japan|travel
After I initially left a comment I seem to have clicked on the -Notify me when new comments are added- checkbox and from now on whenever a comment is added I get 4 emails with the same comment. Is there a means you can remove me from that service? Thank you.
https://sethnik.com/
This is a topic which is near to my heart… Cheers! Where are your contact details though?
https://sethnik.com/
Good post. I learn something totally new and challenging on blogs I stumbleupon everyday. It’s always useful to read through articles from other writers and use a little something from other sites.
https://www.gosnursesleague.org/
Very nice write-up. I absolutely love this website. Keep writing!
https://www.gosnursesleague.org/
Way cool! Some very valid points! I appreciate you writing this article plus the rest of the website is very good.
https://kubet77school.weebly.com/
Very good article. I will be going through a few of these issues as well..
http://www.lasvegastourgirls.com/
cost noroxin – noroxin medication where to buy confido without a prescription
Hi! I could have sworn I’ve been to this website before but after going through many of the posts I realized it’s new to me. Anyhow, I’m definitely delighted I came across it and I’ll be book-marking it and checking back often.
https://iptvmade.com
I’m impressed, I must say. Seldom do I come across a blog that’s equally educative and amusing, and without a doubt, you have hit the nail on the head. The issue is something that too few folks are speaking intelligently about. Now i’m very happy that I came across this in my search for something regarding this.
https://iptvmade.com
After I originally commented I seem to have clicked on the -Notify me when new comments are added- checkbox and now whenever a comment is added I recieve four emails with the exact same comment. Is there an easy method you are able to remove me from that service? Appreciate it.
https://xrediptv.com
Excellent post! We are linking to this great content on our site. Keep up the good writing.
https://xrediptv.com
Wonderful article! We are linking to this great content on our site. Keep up the great writing.
https://iptv-vandaag.com
Hi there, There’s no doubt that your web site could be having browser compatibility problems. Whenever I take a look at your web site in Safari, it looks fine however when opening in I.E., it has some overlapping issues. I merely wanted to give you a quick heads up! Besides that, fantastic site.
https://iptv-vandaag.com
I’m amazed, I must say. Seldom do I come across a blog that’s both educative and interesting, and let me tell you, you’ve hit the nail on the head. The issue is something that too few folks are speaking intelligently about. I am very happy I came across this during my search for something concerning this.
http://support.cancer.ca/site/UserLogin?amp;NEXTURL=http://gunnerrcdr828.theglensecret.com/forget-affordable-accommodations-in-tokyo-10-reasons-why-you-no-longer-need-it
Very good post! We will be linking to this particularly great content on our site. Keep up the great writing.
http://e-smkharapan.sch.id/okegas/
You’ve made some really good points there. I looked on the web to learn more about the issue and found most individuals will go along with your views on this website.
https://www.flumpebbleflavors.org
Spot on with this write-up, I truly think this website needs much more attention. I’ll probably be returning to read through more, thanks for the advice!
https://www.asbestosinottawa.com/
It’s hard to find educated people about this subject, however, you seem like you know what you’re talking about! Thanks
https://masupra.sch.id/views/jurnal/
Very good post! We will be linking to this great article on our website. Keep up the great writing.
https://masupra.sch.id/views/jurnal/
An impressive share! I’ve just forwarded this onto a friend who has been conducting a little homework on this. And he in fact ordered me dinner due to the fact that I stumbled upon it for him… lol. So let me reword this…. Thank YOU for the meal!! But yeah, thanks for spending some time to talk about this issue here on your web site.
https://masupra.sch.id/views/jurnal/
lasuna over the counter – order lasuna online cheap order himcolin for sale
I was pretty pleased to uncover this site. I need to to thank you for ones time due to this wonderful read!! I definitely loved every little bit of it and I have you book marked to see new things in your blog.
https://rent2ownsmart.com
A motivating discussion is worth comment. I do think that you need to write more about this subject, it might not be a taboo subject but generally folks don’t talk about such subjects. To the next! Best wishes.
https://rent2ownsmart.com
It’s hard to come by educated people for this subject, but you sound like you know what you’re talking about! Thanks
https://daga26801.jiliblog.com/85716929/what-regarding-games-perform-best-gambling-sites-surely-have
Spot on with this write-up, I absolutely believe this web site needs much more attention. I’ll probably be back again to read through more, thanks for the advice.
https://www.amazon.com/dp/B0CF66ZZ8W
I need to to thank you for this very good read!! I certainly enjoyed every bit of it. I have got you book marked to check out new stuff you post…
http://gaggedtop.com/cgi-bin/top/out.cgi?ses=sBZFnVYGjF&id=206&url=https://www.bruitsociete.ca/
You have made some decent points there. I checked on the internet for more information about the issue and found most people will go along with your views on this web site.
https://www.hishypesports.com
I really love your blog.. Very nice colors & theme. Did you make this web site yourself? Please reply back as I’m planning to create my own personal blog and want to know where you got this from or exactly what the theme is called. Cheers.
https://planemad.net/
Excellent article. I am facing some of these issues as well..
https://iwin68.bio/
I blog quite often and I genuinely thank you for your information. This article has truly peaked my interest. I will take a note of your blog and keep checking for new details about once a week. I subscribed to your Feed too.
https://library.univefarina.ac.id/students/
order gasex generic – diabecon tablet order diabecon generic
I enjoy reading through an article that will make people think. Also, thank you for permitting me to comment.
https://masupra.sch.id/views/jurnal/
Hi, I do think this is a great blog. I stumbledupon it 😉 I may return yet again since i have saved as a favorite it. Money and freedom is the greatest way to change, may you be rich and continue to guide others.
https://info.greenpramukacity.id/cgi-sys/suspendedpage.cgi
Having read this I believed it was rather informative. I appreciate you taking the time and effort to put this content together. I once again find myself spending a significant amount of time both reading and leaving comments. But so what, it was still worth it!
http://taytrangranggiare.net/301.php?url=http://amik-labuhanbatu.ac.id/
Way cool! Some extremely valid points! I appreciate you penning this article and also the rest of the site is really good.
https://iklimbantendki.id/news/
cheap atorlip for sale – buy bystolic 5mg pill buy bystolic tablets
Right here is the right website for everyone who wishes to find out about this topic. You know so much its almost tough to argue with you (not that I really would want to…HaHa). You definitely put a brand new spin on a subject that has been discussed for decades. Wonderful stuff, just great.
https://aidigitales.com/
Very good post. I’m experiencing a few of these issues as well..
https://aidigitales.com/
I really like reading through a post that will make men and women think. Also, thanks for allowing for me to comment.
http://fipumj.ac.id
Excellent post! We are linking to this great article on our site. Keep up the great writing.
https://www.maraboutvoyantafricain.com/
Aw, this was an extremely good post. Taking a few minutes and actual effort to make a good article… but what can I say… I procrastinate a whole lot and never seem to get nearly anything done.
https://cards.yandex.com/search?text=site3Am.oranumbers.com&lr=111354
I used to be able to find good info from your blog articles.
https://dabrowatarnowska.praca.gov.pl/rynek-pracy/bazy-danych/infodoradca/-/InfoDoradcaPlus/litera/I?_occupationPlusportlet_WAR_nnkportlet_backURL=https://m.oranumbers.com&_occupationPlusportlet_WAR_nnkportlet_code=242214&_occupationPlusportlet_WAR_nnkportlet_description=identificationData
Hello there! I just want to give you a big thumbs up for your excellent information you have got here on this post. I’ll be coming back to your blog for more soon.
https://www.youtube.com/@aidigitales
I blog often and I seriously appreciate your content. The article has really peaked my interest. I am going to take a note of your website and keep checking for new information about once a week. I subscribed to your RSS feed as well.
https://www.youtube.com/@aidigitales
An interesting discussion is worth comment. I believe that you need to write more on this topic, it may not be a taboo matter but usually folks don’t discuss such subjects. To the next! Many thanks.
https://www.funkyrepublicvapes.org
This is a great tip especially to those fresh to the blogosphere. Short but very accurate information… Thanks for sharing this one. A must read post!
https://www.funkyrepublicvapes.org
This site was… how do I say it? Relevant!! Finally I have found something which helped me. Many thanks.
https://bestiptv1.shop
tenormin 50mg price – plavix 75mg price generic carvedilol 25mg
Good post. I learn something totally new and challenging on blogs I stumbleupon everyday. It’s always interesting to read through articles from other authors and use something from their web sites.
https://www.maraboutvoyantafricain.com/
You are so interesting! I do not suppose I’ve truly read anything like this before. So good to find somebody with some original thoughts on this subject. Seriously.. thanks for starting this up. This site is something that is needed on the internet, someone with a bit of originality.
https://minecraft.curseforge.com/linkout?remoteUrl=http://m.oranumbers.com
Greetings! Very helpful advice in this particular article! It is the little changes that make the greatest changes. Many thanks for sharing!
https://yaca.yandex.com/search?text=site3Am.oranumbers.com&lr=111354
I wanted to thank you for this good read!! I definitely loved every bit of it. I’ve got you book marked to check out new things you post…
https://barcasl0t.com/
order calan 240mg – order valsartan for sale buy generic tenoretic over the counter
I couldn’t refrain from commenting. Exceptionally well written.
https://barcasl0t.com/
Way cool! Some very valid points! I appreciate you writing this article and also the rest of the site is also really good.
https://juqh.xyz/v/up/
Good post! We are linking to this particularly great article on our site. Keep up the good writing.
https://tribratanews.lampung.polri.go.id/-/
Hi there! This article could not be written any better! Looking through this article reminds me of my previous roommate! He always kept talking about this. I most certainly will forward this post to him. Fairly certain he’s going to have a very good read. I appreciate you for sharing!
https://fk.uki.ac.id/css/skins/
Hi! I could have sworn I’ve visited this web site before but after going through a few of the articles I realized it’s new to me. Regardless, I’m definitely happy I stumbled upon it and I’ll be book-marking it and checking back often!
https://sites.google.com/view/httpsdagathomonet-com/trang-chE1BBA7
I enjoy reading an article that can make people think. Also, many thanks for permitting me to comment.
https://about.me/shbethow
A fascinating discussion is definitely worth comment. There’s no doubt that that you should publish more about this subject, it might not be a taboo subject but generally people don’t talk about such topics. To the next! Best wishes.
https://www.elleryng.com/
Howdy! I could have sworn I’ve visited this website before but after browsing through many of the articles I realized it’s new to me. Anyways, I’m certainly delighted I stumbled upon it and I’ll be bookmarking it and checking back often.
https://www.elleryng.com/
Good web site you have got here.. It’s hard to find excellent writing like yours nowadays. I really appreciate individuals like you! Take care!!
https://www.jimjeans.com/
I’d must seek advice from you here. Which isn’t some thing It’s my job to do! I spend time reading an article that will make people think. Also, thank you allowing me to comment!
https://forum.pokexgames.pl/member.php?action=profile&uid=45377
I just want to produce a quick comment to be able to express gratitude back for all those wonderful pointers you’re posting at this site. My time consuming internet investigation has at the conclusion of the day been rewarded with excellent means to show to my guests. I’d personally claim that a number of us guests are very endowed to happens to an excellent network with lots of marvellous people who useful hints. I believe quite privileged to possess used your webpages and check forward to really more fabulous minutes reading here. Thank you for lots of things.
https://photoclub.canadiangeographic.ca/profile/21218378
Great blog! Do you have any helpful hints for aspiring writers? I’m hoping to start my own blog soon but I’m a little lost on everything. Would you recommend starting with a free platform like WordPress or go for a paid option? There are so many options out there that I’m totally overwhelmed .. Any ideas? Appreciate it!
http://weselewstolicy.pl/profile/?u=152106
buy arava online cheap – purchase leflunomide buy generic cartidin
As a blow owner I believe the material here is reallyfantastic. I appreciate it for your time. You should keep it up forever! Best of luck…
https://forumszkolne.pl/profiles/pestcontrol695-u224866.html
Hi there just wanted to give you a quick heads up. The text in your content seem to be running off the screen in Firefox. I’m not sure if this is a format issue or something to do with internet browser compatibility but I thought I’d post to let you know. The design look great though! Hope you get the problem solved soon. Many thanks
http://qooh.me/beadlayer9
bed sheets that are made of flannel fabric are the best type of bed sheets,
https://intensedebate.com/people/basinpasta3
After I initially left a comment I seem to have clicked on the -Notify me when new comments are added- checkbox and now every time a comment is added I recieve 4 emails with the same comment. Perhaps there is a way you can remove me from that service? Thank you.
https://x.com/galileofx
This is a topic that’s near to my heart… Best wishes! Exactly where are your contact details though?
https://x.com/galileofx
I think this site has got some very excellent info for everyone : D.
https://list.ly/thurstongustafson339
It would solidify best to ro along with your managing postpartum depressive disorders without needing paxil in case you are strapped about it.
http://www.eldarya.pl/player/profile/pestcontrol280
I should say also believe that mesothelioma cancer is a uncommon form of cancer malignancy that is usually found in people previously familiar with asbestos. Cancerous tissue form inside the mesothelium, which is a shielding lining which covers the majority of the body’s areas. These cells normally form from the lining on the lungs, tummy, or the sac that encircles one’s heart. Thanks for giving your ideas.
http://atlas.dustforce.com/user/pestcontrol085
Aw, i thought this was an incredibly nice post. In notion I have to set up writing like this moreover – taking time and actual effort to have a really good article… but so what can I say… I procrastinate alot by no means manage to get something accomplished.
http://www.infoarena.ro/utilizator/pestcontrol437
This is a topic that’s near to my heart… Take care! Exactly where are your contact details though?
http://oro-kondicionieriai.lt/
After study many of the web sites for your internet site now, i really appreciate your strategy for blogging. I bookmarked it to my bookmark site list and will be checking back soon. Pls have a look at my web-site too and figure out what you consider.
https://www.dermandar.com/user/pestcontrol677/
There’s definately a lot to find out about this subject. I like all of the points you have made.
http://oro-kondicionieriai.lt/
Good day! I could have sworn I’ve been to your blog before but after browsing through a few of the articles I realized it’s new to me. Regardless, I’m certainly delighted I stumbled upon it and I’ll be book-marking it and checking back often.
https://kiu.ac.ug
I’m amazed, I have to admit. Seldom do I come across a blog that’s both equally educative and amusing, and without a doubt, you have hit the nail on the head. The issue is something that too few folks are speaking intelligently about. Now i’m very happy that I found this in my hunt for something relating to this.
https://library.univefarina.ac.id/students/
Good information. Lucky me I came across your site by chance (stumbleupon). I have bookmarked it for later!
https://library.univefarina.ac.id/students/
I enjoy reading a post that can make men and women think. Also, thanks for allowing me to comment.
https://feb.uki.ac.id/video/uki/
This is a topic that is close to my heart… Thank you! Where can I find the contact details for questions?
https://feb.uki.ac.id/video/uki/
I absolutely love your site.. Excellent colors & theme. Did you develop this amazing site yourself? Please reply back as I’m attempting to create my own personal website and want to find out where you got this from or exactly what the theme is named. Appreciate it!
https://inspirationallyquoted.com
This site truly has all the info I wanted concerning this subject and didn’t know who to ask.
https://inspirationallyquoted.com
rogaine cost – finpecia pills purchase proscar pills
Oh my goodness! Incredible article dude! Thank you so much, However I am encountering difficulties with your RSS. I don’t know why I cannot join it. Is there anybody else having identical RSS issues? Anyone that knows the solution can you kindly respond? Thanks!!
https://casino5588.com/
Everything is very open with a clear description of the challenges. It was really informative. Your site is very useful. Thank you for sharing!
http://www.aidigitales.com/
Hi there! I just would like to give you a huge thumbs up for your great information you’ve got here on this post. I’ll be coming back to your website for more soon.
http://www.aidigitales.com/
When I originally left a comment I appear to have clicked on the -Notify me when new comments are added- checkbox and from now on whenever a comment is added I get 4 emails with the exact same comment. Is there a means you are able to remove me from that service? Thanks.
http://www.aidigitales.com/
I seriously love your site.. Very nice colors & theme. Did you make this website yourself? Please reply back as I’m attempting to create my own website and would love to know where you got this from or just what the theme is named. Kudos.
https://bnp.jambiprov.go.id
order ascorbic acid 500 mg sale – order ciprodex ophthalmic solution online compro canada
buy ondansetron for sale – order oxybutynin sale ropinirole 1mg us
flexeril online order – primaquine ca enalapril 10mg for sale
You need to be a part of a contest for one of the greatest blogs on the net. I most certainly will recommend this site!
https://api.webconnex.com/v1/postmaster/track/click/4f8036d14ee545798599c8921fbfcd22/db005310dba511e89fb606f49a4ee876?url=https://tubidy.ac.nz/
order cytoxan pills – buy stavudine online cheap vastarel pills
Right here is the perfect webpage for anybody who hopes to find out about this topic. You know a whole lot its almost tough to argue with you (not that I really would want to…HaHa). You certainly put a brand new spin on a topic that has been written about for years. Great stuff, just wonderful.
https://mod273.share.library.harvard.edu
disopyramide phosphate us – buy generic lamictal for sale chlorpromazine 100mg pill
쥬라기공원 에볼루션
https://www.longisland.com/profile/hyenashow73
Hello. I wanted to inquire something…is the following a wordpress site as we are planning to be shifting across to WP. In addition did you make this design by yourself? Many thanks.
https://www.dermandar.com/user/gasengineer208/
Perfect piece of work you have done, this website is really cool with superb information.
https://forum.pokexgames.pl/member.php?action=profile&uid=45157
Hey, I never genuinely posted here but these days I wish to thank you for performing these a fantastic work.
http://www.effecthub.com/people/gasengineer498
Thanks , I’ve recently been searching for information about this subject for ages and yours is the greatest I’ve discovered so far. But, what about the conclusion? Are you sure about the source?
https://blend.io/gasengineer548
What a rejuvenating shock your posts are. Your posts of this matter is just what I desired to essentially set the history right. You need to keep up your publishing.
https://www.shadertoy.com/user/gasengineer535
One other issue is that if you are in a circumstances where you will not have a cosigner then you may really want to try to exhaust all of your money for college options. You will find many funds and other scholarships or grants that will offer you funding that can help with college expenses. Thanks alot : ) for the post.
https://www.themehorse.com/support-forum/users/beccaberger
Hi there, just became alert to your blog through Google, and found that it is truly informative. I am gonna watch out for brussels. I will be grateful if you continue this in future. Many people will be benefited from your writing. Cheers!
https://photoclub.canadiangeographic.ca/profile/21213740
buy divalproex 500mg generic – acetazolamide 250mg sale buy cheap generic topiramate
Straight to the point, i love it. Dont let anyone stop us bloggers.
https://forumszkolne.pl/profiles/gasengineer081-u224350.html
This web site is really a walk-through you discover the knowledge it suited you about this and didn’t know who to inquire about. Glimpse here, and you’ll undoubtedly discover it.
https://shorl.com/fadutudefrope
Preferably,when you gain knowledge,are you able to mind updating your website with an increase of information? It is very ideal for me.
https://psee.io/5le5dw
You have observed very interesting details! ps nice web site.
https://www.englishbaby.com/findfriends/gallery/detail/2481898
of course like your web site however you need to take a look at the spelling on quite a few of your posts. A number of them are rife with spelling problems and I to find it very troublesome to tell the truth nevertheless I’ll definitely come again again.
https://www.algebra.com/tutors/aboutme.mpl?userid=gasengineer334
Have a great day!. After reading this I thought it was very informative. I appreciate you taking the time to put this blog piece together. I once again find myself spending way to much time both reading and commenting. What ever, it was still worth it ! female libido booster
http://atlas.dustforce.com/user/gasengineer398
Everyone loves your blog.. comfortable shades & concept. Do an individual design and style this website yourself or perhaps do anyone hire an attorney to accomplish it available for you? Plz reply when I!|m looking to design my personal web site plus wish to learn wherever u acquired the following out of. many thanks
https://gasengineer518.tribalpages.com/
i think that gun control is a must because more guns means more deaths-
http://atlas.dustforce.com/user/beetwallet39
Hey, thanks for sharing… I always look forward to reading your posts… one of the few blogs I still follow!
http://ezproxy.cityu.edu.hk/login?url=https://wimbledongasengineers.co.uk/
Good story and a pleasant summation of the problem. My only problem with the analysis is given that much of the population joined the chorus of deregulatory mythology, given vested interest is inclined toward perpetuation of the current system and given a lack of a popular cheerleader for your arguments, I’m not seeing much in the way of change.
https://anotepad.com/notes/ggdqtb2i
There is noticeably a bundle to know about this. I suppose you’ve made particular nice points in features also.
https://usedsalvagecars.com/profile/profile/1829812
you will have a great blog here! would you like to make some invite posts on my weblog?
http://80.82.64.206/user/strawbanker85
buy hydrea tablets – buy ethionamide methocarbamol order online
An intriguing discussion will probably be worth comment. I do think that you ought to write on this topic, may possibly not be a taboo subject but normally individuals are not enough to talk on such topics. To the next. Cheers
https://gorod-lugansk.com/user/oxygengrowth85/
You lost me, buddy. I mean, I imagine I get what youre stating. I understand what you are saying, but you just appear to have forgotten about that you will find some other men and women within the world who view this matter for what it really is and may not agree with you. You may perhaps be turning away many of persons who might have been fans of your blog.
https://www.mapleprimes.com/users/wingdegree10
Excellent! I thank you your input to this matter. It has been insightful. my blog: master cleanse
https://gorod-lugansk.com/user/gumatom02/
stiri interesante si utile postate pe blogul dumneavoastra. dar ca si o paranteza , ce parere aveti de inchiriere vile vacanta ?.
https://vuf.minagricultura.gov.co/Lists/Informacin20Servicios20Web/DispForm.aspx?ID=7292544
Considerably, the article is in reality the most excellent on this precious topic. I harmonise with your conclusions and can eagerly look forward to your next updates. Simply saying thanks will certainly not simply just be sufficient, for the phenomenal lucidity in your writing. I definitely will directly grab your rss feed to stay informed of any updates. De lightful work and much success in your business dealings!
http://taksim.in/index.php/user/statebomber55
There is noticeably a bundle to know about this. I assume you made certain nice points in features also.
https://www.longisland.com/profile/platebat46
my sister and i loves to read christian books because it inspires us to live life in its fullest*
https://vuf.minagricultura.gov.co/Lists/Informacin20Servicios20Web/DispForm.aspx?ID=7275010
This is really interesting, I’ll check out your other posts!
http://court.khotol.se.gov.mn/user/bananawallet45/
I like the way you conduct your posts. m
https://canvas.instructure.com/eportfolios/2501107/Home/_Behind_the_Scenes_A_Day_in_the_Life_at_South_Croydon_Gas_Engineers_
howdy, I am gettin my site ranked “lands end catalog”.
http://qa.rudnik.mobi/index.php?qa=user&qa_1=beetwallet59
Loving the information on this website , you have done outstanding job on the articles .
https://v.gd/commercial_gas_engineers_52464
It hard to seek out educated individuals on this subject, however you sound like you realize what you are speaking about! Thanks
https://code.getnoc.com/zebrabat40
Thanks i love your article about Pro-Life Commencement | Fr. Frank Pavone’s Blog
https://offroadjunk.com/questions/index.php?qa=user&qa_1=friendskiing44
Nice blog here! Also your website loads up very fast! What web host are you using? Can I get your affiliate link to your host? I wish my website loaded up as quickly as yours lol
https://intensedebate.com/people/yearcomb19
This problem will only come to be more exacerbated as more people start out ‘cocooning’ within their houses. If you prefer to know more about social multi-level marketing, you’ll want to make investments some time and hard earned cash in excellent knowledge that may make your website potential customers explode.
http://deluxeswap.com/members/witchsave51/activity/134191/
An interesting discussion might be priced at comment. I do think that you simply write read more about this topic, it will not certainly be a taboo subject but typically persons are insufficient to dicuss on such topics. To another. Cheers
https://www.strumentazioneoftalmica.it/author/wormrod39
I don’t agree with this particular article. However, I did researched in Google and I’ve found out that you are correct and I had been thinking in the incorrect way. Continue producing quality material similar to this.
https://www.sitiosecuador.com/author/gumskiing98/
the shoulder bags that my girlfriend uses are always made up from natural leather`
https://cairns.nsta.edu.au/author/maidstorm47
Doceniam nacisk na zdrowie i bezpieczeństwo w kontekście SEO.
https://yamcode.com/agencja-sem-leads-4-local-pozycjonowanie-stron-uk-londyn-14
buy piracetam without prescription – sinemet over the counter order sinemet without prescription
Nie miałem pojęcia, że SEO jest tak ważne. Dzięki za ten wpis.
https://hanson-broch.hubstack.net/pozycjonowanie-stron-jak-efektywnie-wypromowac-swoja-witryne-w-wyszukiwarkach
Doceniam szczegółowe wyjaśnienia na temat SEO i bezpieczeństwa.
http://www.ccwzz8.com/space-uid-1653799.html
Dzięki za świetne porady na temat SEO. Bezpieczeństwo jest kluczowe!
https://homeinsiderguide.com/user/hatbat7
Czuję się znacznie pewniej w temacie SEO po przeczytaniu tego bloga.
https://etextpad.com/xkn2ipzuhl
Dziękuję za poruszenie tematu, który często jest pomijany, jakim jest SEO.
https://community.windy.com/user/badgerdrop1
Świetne wskazówki dotyczące znalezienia wiarygodnych usług SEO. Dzięki!
https://moiafazenda.ru/user/badgerpot2/
Czuję się dużo lepiej poinformowany o SEO. Dzięki!
https://canvas.instructure.com/eportfolios/1920114/Home/Pozycjonowanie_inaczej_nazywane_SEO_Search_Engine_Optimization_to_przebieg_optymalizacji_strony_internetowej_po_celu_uzyskania_lepszej_widocznoci_w_serpach_Google
Ten post był bardzo pouczający na temat procesu SEO. Dzięki!
https://rosalind.info/users/insectsyrup2
Dzięki za szczegółowy przegląd procedur SEO.
https://www.transtats.bts.gov/exit.asp?url=https://sites.google.com/view/pozycjonowanie-uk/
Ten blog bardzo mi pomógł w zrozumieniu potrzeby SEO.
http://www.drugoffice.gov.hk/gb/unigb/sites.google.com/view/pozycjonowanie-uk/
Dzięki za szczegółowy przewodnik po tym, czego można oczekiwać podczas wdrażania SEO.
http://qooh.me/europehair8
Doceniam szczegółowe wyjaśnienia na temat SEO i bezpieczeństwa.
https://livingwellcenters.org/members/personbat3/activity/83188/
Dzięki za praktyczne porady i wskazówki dotyczące SEO.
https://www.awwwards.com/mouthstem4/
Bardzo pouczający post o SEO. Cieszę się, że to przeczytałem przed rozpoczęciem jakichkolwiek działań.
https://cooperationengine.com/members/bluenephew3/activity/109566/
Bardzo pouczający blog na temat SEO! Dzięki za podzielenie się nim.
http://moovlink.com/?c=A1FSV1I6ZmEwYzE0ZmE
Dzięki za praktyczne wskazówki dotyczące bezpiecznego SEO.
http://yogicentral.science/index.php?title=puckettnewton6052
Doceniam nacisk na bezpieczeństwo i profesjonalizm w SEO.
https://slides.com/pozycjonowanieusa/pozycjonowaniestanyzjednoczone
Świetny artykuł na temat znaczenia SEO dla bezpieczeństwa.
https://pozycjonowanie-stron-internetowych-uk.webnode.page/
Great website! I am loving it!! Will be back later to read some more. I am bookmarking your feeds also
https://qooh.me/pvcquail1
Good day I am so excited I found your webpage, I really found you by mistake, while I was looking on Google for something else, Regardless I am here now and would just like to say many thanks for a fantastic post and a all round enjoyable blog (I also love the theme/design), I don’t have time to look over it all at the moment but I have bookmarked it and also added in your RSS feeds, so when I have time I will be back to read a great deal more, Please do keep up the great job.
https://www.dermandar.com/user/noisewoolen5/
I like this web blog very much, Its a very nice situation to read and incur information.
https://blogfreely.net/noisechina8/eco-friendly-scaffolding-solutions-structure-sustainably
of course we need to know our family history so that we can share it to our kids’
https://b.cari.com.my/home.php?mod=space&uid=2993760&do=profile
Remarkably! It really is like you study my mind! A person seem to understand so considerably relating to this, exactly like you authored the book inside it or even some thing. I believe that you simply can do with a few pictures to drive the content residence a little, on top of that, this really is excellent weblog. A exceptional study. I’ll surely revisit again.
https://www.metooo.es/u/6612221b0c22f011b86ff7c4
Its wonderful as your other articles : D, thanks for putting up.
https://www.metooo.es/u/6611fe241694d226010f9085
There are extremely loads of details prefer that to take into consideration. This is a great examine start up. I offer the thoughts above as general inspiration but clearly there are questions such as the one you mention where the most critical factor might be in the honest good faith. I don?t determine if recommendations have emerged around such things as that, but I know that your chosen job is clearly referred to as an affordable game. Both kids notice the impact of a little moment’s pleasure, for the rest of their lives.
https://wikimapia.org/external_link?url=https://kingstonuponthamesscaffolding.co.uk/index.html
Spot up with this write-up, I must say i believe this excellent website wants a great deal more consideration. I’ll apt to be once again to study far more, thank you that information.
https://www.webwiki.nl/highgatescaffolding.co.uk
I definitely wanted to post a simple remark in order to thank you for all the unique tips and tricks you are giving out on this website. My incredibly long internet search has finally been recognized with extremely good points to go over with my company. I ‘d say that we readers are very blessed to exist in a superb site with so many awesome people with good advice. I feel pretty happy to have come across your entire website and look forward to tons of more brilliant moments reading here. Thanks a lot once more for everything.
https://www.demilked.com/author/orangeyellow0/
Your blog is showing more interest and enthusiasm. Thank you so much.
https://postheaven.net/actclave0/just-how-scaffolding-contributes-to-a-safer-building-and-construction-website
I really enjoyed reading this blog post. I will certainly come back and read some more interesting post. Thank you
https://www.metooo.io/u/6610cbf01694d226010e465c
When I originally commented I clicked the -Notify me when new surveys are added- checkbox and already when a comment is added I purchase four emails sticking with the same comment. Can there be by any means it is possible to get rid of me from that service? Thanks!
https://milkyway.cs.rpi.edu/milkyway/show_user.php?userid=6714946
hello there and thank you for your information – I’ve certainly picked up something new from right here. I did however expertise several technical issues using this web site, as I experienced to reload the web site a lot of times previous to I could get it to load properly. I had been wondering if your web hosting is OK? Not that I’m complaining, but slow loading instances times will often affect your placement in google and can damage your high quality score if ads and marketing with Adwords. Well I am adding this RSS to my e-mail and can look out for a lot more of your respective intriguing content. Make sure you update this again soon..
https://www.prestashop.com/forums/profile/1842612-nosereward0//?tab=field_core_pfield_19
hi!,I like your writing so much! share we keep up a correspondence extra approximately your post on AOL? I require a specialist on this space to solve my problem. May be that is you! Looking ahead to peer you.
https://fileforum.com/profile/susanquail4/
To be sure completely along with your conclusions and imagine that you’ve made some excellent points. Also, I prefer customized for specific cultures of this site and also the easy navigation. I’ve bookmarked your site and may return often!
https://rentry.co/whfych87
I am impressed with this website , very I am a fan .
https://able2know.org/user/shopguitar2/
I enjoyed reading your pleasant blog. I see you offer priceless information. feel into this blog by chance but I’m sure glad I clicked on that link. You definitely answered all the questions I’ve been dying to answer for some time now. Will definitely come back for more of this.
http://153.126.169.73/question2answer/index.php?qa=user&qa_1=shopsea8
Some really great articles on this site, appreciate it for contribution.
https://anekdotoes.ru/user/nutgas9/
This will be the correct weblog for anyone who hopes to be familiar with this topic. You already know so much its practically hard to argue on hand (not too I personally would want…HaHa). You definitely put a brand new spin for a topic thats been revealed for some time. Fantastic stuff, just great!
http://mozillabd.science/index.php?title=howardtobin8237
Next time I read a blog, I hope that it doesn’t fail me just as much as this particular one. After all, Yes, it was my choice to read through, but I truly believed you’d have something helpful to talk about. All I hear is a bunch of whining about something that you could fix if you were not too busy searching for attention.
https://hipaonline.com
I absolutely love your website.. Great colors & theme. Did you build this website yourself? Please reply back as I’m attempting to create my own personal website and would love to know where you got this from or what the theme is named. Thank you!
https://lumieremusic.net
That is a very good tip especially to those new to the blogosphere. Short but very precise info… Thanks for sharing this one. A must read post.
https://google.mg/url?q=https://anthillmusic.com
piroxicam pills – rivastigmine 6mg sale purchase exelon
my sister loves the tv series Ghost Whisperer but i do find it a bit distracting sometimes,
https://www.longisland.com/profile/shearscreek43
well, if you really want to be healthy, i believe that veggan foods are the best ;
https://www.dermandar.com/user/heleniris25/
An attention-grabbing dialogue is price comment. I believe that it is best to write more on this matter, it might not be a taboo topic but usually people are not sufficient to talk on such topics. To the next. Cheers
http://mnogootvetov.ru/index.php?qa=user&qa_1=brainorchid00
Great blog here! Also your website loads up fast! What host are you the usage of? Can I get your affiliate hyperlink for your host? I want my website loaded up as quickly as yours lol.
https://bbs.pku.edu.cn/v2/jump-to.php?url=https://uxbridgehvac.co.uk/air-conditioning-installation.html
you could just listen to the beat of those high bass from Rap songs, i just like rap songs;;
https://www.webwiki.at/teddingtonhvac.co.uk/air-conditioning-repair.html
Hi there, thanks for the awesome posting. I’m having troubles subscribing to your blogs feed. Thought I’d let you know
https://bbs.pku.edu.cn/v2/jump-to.php?url=https://uxbridgehvac.co.uk/air-conditioning-repair.html
Great blog, I’m going to spend more time reading about this subject
https://k12.instructure.com/eportfolios/639147/Home/_Smart_Air_Conditioners_Revolutionizing_Home_Climate_Control_
The Notebook is of course one of Nick Sparks best tear jearker novel. Nick is really very talented guy;
https://bbs.pku.edu.cn/v2/jump-to.php?url=https://romfordhvac.co.uk/air-conditioning-repair.html
order etodolac 600mg online cheap – cheap monograph purchase cilostazol online cheap
I discovered your web page just recently through a recommendation and had a look at some of your articles. I like what you are writing about and I hope you keep up the good work. If you are interested in sharing some content or swap links do not hesitate to get in touch with me.
https://telegra.ph/The-Impact-of-Climate-Change-on-Air-Conditioning-Needs-03-28-2
I am curious to find out what blog platform you happen to be working with? I’m experiencing some minor security problems with my latest blog and I would like to find something more secure. Do you have any recommendations?
http://zaday-vopros.ru/user/breadson32
Very good post, thanks a lot for sharing. Do you happen to have an RSS feed I can subscribe to?
http://hawkee.com/profile/6479982/
I’m not sure why but this web site is loading very slow for me. Is anyone else having this issue or is it a issue on my end? I’ll check back later on and see if the problem still exists.
http://ezproxy.cityu.edu.hk/login?url=https://raynesparkhvac.co.uk/air-conditioning-installation.html
Sweet blog! I found it while searching on Yahoo News. Do you have any tips on how to get listed in Yahoo News? I’ve been trying for a while but I never seem to get there! Thanks
https://www.metooo.co.uk/u/660504a21694d22601ff7657
Appreciate it for helping out, superb information.
http://extension.unimagdalena.edu.co/extension/Lists/Contactenos/DispForm.aspx?ID=1262998
I gotta bookmark this web site it seems invaluable handy
http://www.stes.tyc.edu.tw/xoops/modules/profile/userinfo.php?uid=1249614
It’s in point of fact a nice and useful piece of information. I’m happy that you just shared this helpful information with us. Please keep us up to date like this. Thanks for sharing.
http://idea.informer.com/users/helenapril65/?what=personal
I am happy that I noticed this site, precisely the right info that I was searching for!
https://hangoutshelp.net/user/lakebull36
howdy, I’m havin a tough time trying to rank up for the keyword “victorias secret coupon codes”… Pls approve my comment!!
https://www.pdc.edu/?URL=https://peckhamhvac.co.uk/air-conditioning-repair.html
Hi, I just found your website via Bing. Your article is truly applicable to my life right now, and I’m really delighted I found your website.
https://www.diggerslist.com/6609a1cd6e9b4/about
You made some respectable points there. I looked on the internet for the difficulty and found most people will go along with along with your website.
https://www.metooo.io/u/6609a0c9fac31e2602f9e823
I am glad for writing to let you be aware of of the magnificent discovery my princess experienced using the blog. She came to find plenty of issues, not to mention what it’s like to possess a great teaching character to get many others just know a number of advanced things. You really did more than visitors’ expectations. Thank you for giving such insightful, healthy, revealing as well as fun guidance on this topic to Lizeth.
https://intensedebate.com/people/shearsson98
I have observed that over the course of making a relationship with real estate proprietors, you’ll be able to get them to understand that, in every real estate financial transaction, a payment is paid. In the end, FSBO sellers will not “save” the commission rate. Rather, they fight to earn the commission by simply doing a good agent’s work. In accomplishing this, they devote their money and also time to execute, as best they might, the responsibilities of an broker. Those tasks include revealing the home by way of marketing, introducing the home to prospective buyers, building a sense of buyer emergency in order to make prompt an offer, organizing home inspections, dealing with qualification check ups with the loan company, supervising repairs, and facilitating the closing.
https://www.webwiki.co.uk/mertonhvac.co.uk/air-conditioning-installation.html
An impressive share, I just now given this onto a colleague who had previously been doing a small analysis for this. Anf the husband the truth is bought me breakfast because I came across it for him.. smile. So allow me to reword that: Thnx for your treat! But yeah Thnkx for spending time to discuss this, Personally i think strongly concerning this and enjoy reading more on this topic. If you can, as you become expertise, would you mind updating your blog site with additional details? It’s extremely of great help for me. Big thumb up just for this post!
http://www.stes.tyc.edu.tw/xoops/modules/profile/userinfo.php?uid=1480983
buy enalapril 5mg online – buy generic zovirax buy generic latanoprost for sale
Well, the article is actually the sweetest on this notable topic. I harmonise with your conclusions and also will thirstily look forward to your next updates. Saying thanks definitely will not simply just be enough, for the extraordinary lucidity in your writing. I can directly grab your rss feed to stay abreast of any updates. Solid work and much success in your business efforts!
https://cutt.ly/Kw9K2zdL
cheap dramamine – prasugrel 10 mg pill buy actonel 35 mg online
It’s perfect time to make some plans for the future and it’s time to be happy. I have learn this publish and if I could I desire to counsel you some interesting things or suggestions. Maybe you can write subsequent articles regarding this article. I want to learn even more issues about it!
https://unsplash.com/@dangerjail84
Hi, do you have a facebook fan page for your blog?:;-,`
https://www.metooo.es/u/6601c2b41694d22601f870ab
I got what you mean , saved to bookmarks , very decent site.
http://www.taksim.in/index.php/user/dangerearth32
I just added your RSS Feed on my RSS reader, it is so nice to read your blog.,.~:”
https://www.webwiki.ch/kewhvac.co.uk/air-conditioning-installation.html
Perfectly pent articles , Really enjoyed reading through .
https://alumnair.com/forums/users/teamtitle65/
Premature Ejaculation is the lack of ejaculatory control and it is the most common of all sexual problems in men. Since it is natural, you can use it freely without any risk of adverse effects.
https://www.demilked.com/author/manxcello20/
This design is steller! You obviously know how to keep a reader amused. Between your wit and your videos, I was almost moved to start my own blog (well, almost…HaHa!) Wonderful job. I really enjoyed what you had to say, and more than that, how you presented it. Too cool!
https://www.multichain.com/qa/index.php?qa=user&qa_1=brainpen51
There are very a lot of details this way to consider. Which is a wonderful denote bring up. I provide you with the thoughts above as general inspiration but clearly there are actually questions like the one you talk about the location where the most essential thing might be doing work in honest great faith. I don?t know if best practices have emerged around things like that, but More than likely that your chosen job is clearly referred to as a reasonable game. Both little ones notice the impact of just a moment’s pleasure, for the rest of their lives.
https://www.metooo.co.uk/u/65ffb7d01694d22601f44e83
I do not learn about you but experiencing any form of ‘transformation’ will not be as simple because it seems – neither is any type of ‘death and re-birth’ it truly is all as well painful.
https://www.cheaperseeker.com/u/catsupapril64
Hey dude” what kind of wordpress theme are you using? i want it to use on my blog too “
https://www.metooo.it/u/65ff7346fac31e2602e7994a
Hi, do you have a facebook fan page for your blog?’-”\”.
https://www.pdc.edu/?URL=https://harrowhvac.co.uk/air-conditioning-repair.html
Aw, this was a very nice post. In thought I would like to put in writing like this moreover – taking time and actual effort to make an excellent article… but what can I say… I procrastinate alot and not at all appear to get something done.
http://forum.ressourcerie.fr/index.php?qa=user&qa_1=potpen69
Hi! I could have sworn I’ve been to this blog before but after browsing through some of the post I realized it’s new to me. Anyhow, I’m definitely delighted I found it and I’ll be book-marking and checking back often!
https://www.metooo.co.uk/u/65fd52e8fac31e2602e2e76d
There is noticeably a lot of money to understand this. I assume you made certain nice points in functions also.
https://wikimapia.org/external_link?url=https://hamptonhvac.co.uk/air-conditioning-repair.html
forxiga 10mg brand – order doxepin sale acarbose 25mg sale
order generic griseofulvin 250 mg – griseofulvin 250 mg without prescription buy gemfibrozil generic
woah i like yur website. It really helped me with the info i wus looking for. Appcriciate it, will bookmark.
https://www.webwiki.ch/goldersgreenhvac.co.uk/air-conditioning-repair.html
The following time I learn a weblog, I hope that it doesnt disappoint me as a lot as this one. I imply, I do know it was my option to learn, however I really thought youd have one thing fascinating to say. All I hear is a bunch of whining about something that you can fix when you werent too busy on the lookout for attention.
https://atavi.com/share/wk8rb5z15wb0l
Hey, you used to write excellent, but the last few posts have been kinda boring¡K I miss your super writings. Past few posts are just a little out of track! come on!
https://www.blurb.com/user/clefdegree42
We would also like to convey that most individuals that find themselves without the need of health insurance can be students, self-employed and people who are out of work. More than half in the uninsured are under the age of Thirty five. They do not experience they are wanting health insurance as they are young in addition to healthy. Their particular income is generally spent on housing, food, and entertainment. Many people that do go to work either entire or in their free time are not given insurance via their work so they proceed without because of the rising tariff of health insurance in america. Thanks for the concepts you reveal through this site.
https://postheaven.net/canadaapril05/the-latest-trends-in-air-conditioning-technology-for-modern-homes
Hi, I do believe this is a great web site. I stumbledupon it 😉 I am going to return yet again since i have book-marked it. Money and freedom is the greatest way to change, may you be rich and continue to help others.
https://www.ehpa.org/index.php?id=901&rid=P_86&mid=335&jumpurl=https://snaptik.gg/
I also believe therefore , perfectly pent post! .
https://www.metooo.io/u/651d7693119b751a01c92e6a
An excellent presentation. Clear. Practical. Insightful. Shows a depth of experience. Thank you. I learned a great deal..
https://www.question-ksa.com/user/quivereye37
This could be the proper blog for anybody who wants to check out this topic. You know a lot its practically not easy to argue to you (not that When i would want…HaHa). You certainly put a new spin on a topic thats been discussed for some time. Fantastic stuff, just wonderful!
https://pbase.com/quiverberry38/root
I love how you write, it had me thinking. I??m going to bookmark this.
https://list.ly/holmgaardmccaffrey684
It’s essential to have having access to the knowledge posted here
https://lauesen-cotton.blogbright.net/pioneering-projects-a-peek-right-into-islington-heating-engineers-profile-0a
Good post. I am dealing with many of these issues as well..
https://hslda.org/content/a/LinkTracker.aspx?id=4015475&appeal=385&package=36&uri=https://snaptik.gg
we need some smaller and energy efficient microprocessors to support mobile computing,,
https://learn.centa.org/forums/users/fanbridge11/
??? ??? ???? ?????? ?? ????? ????? ????? ?? ?????? ?????? ????? . ????? ??????? ????? ?????? ????? ??????? ?????? ??????? ???? ????? ?????? ??????? ??? ?????? ??? ?? ??????? money ????? ????????.
https://cutt.ly/Uw2RjI5H
order bactrim for sale – tobra 5mg drops tobramycin generic
Thanks, I have recently been seeking for details about this topic for ages and yours is the best I have located so far.
https://te.legra.ph/A-Legacy-of-Count-On-Celebrating-Years-of-Commercial-Excellence-with-Highgate-Gas-Engineers-10-03
I conceive this website holds very wonderful composed written content content.
https://www.webwiki.ch/eastfinchleyhvac.co.uk/air-conditioning-installation.html
The beauty of these blogging engines and CMS platforms is the lack of limitations and ease of manipulation that allows developers to implement rich content and ’skin’ the site in such a way that with very little effort one would never notice what it is making the site tick all without limiting content and effectiveness.
https://vinther-fraser-2.blogbright.net/the-blueprint-of-success-introduction-holborn-gas-engineers-method-for-the-future-0a
I am usually to blogging and i also actually appreciate your content. The article has truly peaks my interest. I am going to bookmark your blog and keep checking for first time info.
http://molchanovonews.ru/user/dangertempo01/
I really delighted to find this website on bing, just what I was searching for : D also saved to fav.
https://intensedebate.com/people/frenchiris95
Good day! Do you know if they make any plugins
to help with SEO? I’m trying to get my blog to rank for some targeted
keywords but I’m not seeing very good results. If you know of any please share.
Thank you! I saw similar text here: Choose your escape room
purchase eukroma – buy cheap generic eukroma buy duphaston online cheap
Man it’s HOT AF outside! Whew! Perfect day to lay out at the pool & catch some rays! Lmao ???|_NChap|
https://blip.fm/perchbull61
I love the valuable info you supply in your posts. I will remember this.
https://www.metooo.co.uk/u/65f7ab0f3d09f71e96c0d5f9
I do consider all of the concepts you’ve introduced on your post. They’re very convincing and will certainly work. Nonetheless, the posts are too short for starters. Could you please lengthen them a bit from next time? Thanks for the post. Pristina Hotels
https://brainiris20.bravejournal.net/why-regular-air-conditioner-service-is-essential
Great post I must say.. Simple yet somehow intriguing, notable and engaging.. Continue the awesome work!
http://extension.unimagdalena.edu.co/extension/Lists/Contactenos/DispForm.aspx?ID=1173716
J’ai la possibilité de vous en communiquer les adresses pour toujours plus d’images sur cet idée. Joignez moi simplement!
https://www.demilked.com/author/manxschool23/
What your declaring is completely real. I know that everybody have to say the exact same point, but I just assume that you set it in a way that everyone can fully grasp. I also really like the images you set in here. They fit so effectively with what youre hoping to say. Im guaranteed youll attain so numerous folks with what youve obtained to say.
https://qooh.me/beachpen25
Ok oui et pas vraiment. Assurément parce que il se peut qu’on rencontre certaines sources qui probablement citent de semblables cote. Non car il ne suffit pas de copier ce qu’on peut lire avec plusieurs site web autres avant de le transposer tant clairement
https://www.daoduytu.edu.vn/forum/links.php?url=https://claphamhvac.co.uk/air-conditioning-installation.html
Nice Website. You should think more about RSS Feeds as a traffic source. They bring me a nice bit of traffic
https://www.webwiki.ch/chingfordhvac.co.uk/air-conditioning-installation.html
two. You should invite your viewers to write remarks and tips. Regardless if or not their comments and ideas are good or terrible it doesn’t make a difference as any comment is of appeal and should be taken care of as such.
https://anotepad.com/notes/cfci5di2
I love your blog.. excellent shades & design. Does a person layout this amazing site your self and also do anyone hire someone to accomplish it in your case? Plz react when I!|m trying to style my own, personal blog site in addition to would want to recognize where u became this particular via. thanks a lot
https://www.webwiki.at/chingfordhvac.co.uk/air-conditioning-repair.html
As far as me being a member here, I wasn’t aware that I was a member for any days, actually. When the article was published I received a notification, so that I could participate in Comments, so perhaps that is it. But we’re certainly all members in the world of ideas.
https://carverinnovationcenter.com/index.php?option=com_k2&view=itemlist&task=user&id=404450
Hello there! This is my first visit to your blog! We are a team of volunteers and starting a new project in a community in the same niche. Your blog provided us beneficial information to work on. You have done a marvellous job!
http://tupalo.com/en/users/5271262
I always visit new blog everyday and i found your blog.:,`”‘
https://postheaven.net/plateberry17/home-heating-diagnostics-and-also-maintenance-edgwares-proactive-approach
kitchen designs that makes use of space efficiently would be the best thing to go with’
https://www.webwiki.ch/bromleyhvac.co.uk/air-conditioning-repair.html
I have recently started a blog, the information you provide on this website has helped me tremendously. Thanks for all of your time & work.
http://qooh.me/sparkbridge02
Thanks lots because of this hassle-free internet site. i like actively playing transformice display game.
http://mozillabd.science/index.php?title=foxmunk9933
you have a fantastic blog here! do you wish to earn some invite posts on my blog?
http://sorucevap.netyuvam.com/user/filebutane43
I am frequently to blogging we really appreciate your website content continuously. The article has really peaks my interest. I will bookmark your site and keep checking achievable info.
https://www.webwiki.at/brixtonhvac.co.uk/air-conditioning-installation.html
There’s noticeably a bundle to find out about this. I assume you made sure nice factors in options also.
http://ezproxy.cityu.edu.hk/login?url=https://finsburyparkgasengineers.co.uk/
Nice post. I discover something harder on diverse blogs everyday. It will always be stimulating you just read content using their company writers and use a little there. I’d choose to use some while using the content in my small weblog no matter whether you don’t mind. Natually I’ll supply you with a link with your web blog. Many thanks sharing.
https://vuf.minagricultura.gov.co/Lists/Informacin20Servicios20Web/DispForm.aspx?ID=7872565
This website is actually a walk-through its the knowledge it suited you in regards to this and didn’t know who to question. Glimpse here, and you’ll absolutely discover it.
https://www.mazafakas.com/user/profile/3763858
Yo, I’ve been gettin my site ranked “big affiliate profits”.
https://unsplash.com/@syrupdock50
Hello! I simply wish to make a enormous thumbs up with the great info you’ve got here for this post. We are coming back to your site to get more detailed soon.
https://www.webwiki.at/bethnalgreenhvac.co.uk/air-conditioning-installation.html
I have realized that over the course of building a relationship with real estate owners, you’ll be able to come to understand that, in every real estate financial transaction, a commission amount is paid. Ultimately, FSBO sellers do not “save” the commission rate. Rather, they try to win the commission through doing a agent’s work. In the process, they expend their money and also time to complete, as best they might, the tasks of an adviser. Those tasks include disclosing the home via marketing, showing the home to buyers, making a sense of buyer desperation in order to induce an offer, organizing home inspections, taking on qualification inspections with the loan provider, supervising maintenance tasks, and facilitating the closing of the deal.
http://planforexams.com/q2a/user/fanbridge07
Most suitable boyfriend speeches, or else toasts. are almost always transported eventually through the entire wedding party and are still required to be very interesting, amusing and even enlightening together. best man’s speech
https://usedsalvagecars.com/profile/profile/1417610
There are a couple of interesting points soon enough in this posting but I don’t determine if I see these center to heart. You can find some validity but Let me take hold opinion until I investigate it further. Good write-up , thanks so we want much more! Put into FeedBurner at the same time
https://www.longisland.com/profile/frenchcreek16
My brother recommended I might like this web site. He was entirely right. This post truly made my day. You can not imagine just how much time I had spent for this information! Thanks! que es el acne
https://cutt.ly/nwhQhyGJ
I don’t usually comment but I gotta say thankyou for the post on this amazing one : D.
https://sbank-gid.ru/user/helenafrica78/
buy dulcolax sale – generic oxytrol purchase liv52 without prescription
I love your blog post.. comfortable colors & design. Did people style and design this excellent website by yourself and also would anyone rely on someone else to accomplish it available for you? Plz answer since I!|m seeking to style and design my web site in addition to would like to find out where oughout became that coming from. appreciate it
http://cryptomonnaies.me/user/witchdegree25
I just want to produce a quick comment to be able to express gratitude back for all those wonderful pointers you’re posting at this site. My time consuming internet investigation has at the conclusion of the day been rewarded with excellent means to show to my guests. I’d personally claim that a number of us guests are very endowed to happens to an excellent network with lots of marvellous people who useful hints. I believe quite privileged to possess used your webpages and check forward to really more fabulous minutes reading here. Thank you for lots of things.
https://intensedebate.com/people/dangerdomain04
Youre so cool! I dont suppose Ive read anything similar to this prior to. So nice to locate somebody with many original applying for grants this subject. realy appreciation for starting this up. this site can be something that is needed on the internet, a person after a little originality. beneficial project for bringing something totally new to your net!
https://unsplash.com/@syrupskiing12
Hi there, just became aware of your blog through Google, and found that it is really informative. I’m gonna watch out for brussels. I’ll appreciate if you continue this in future. Lots of people will be benefited from your writing. Cheers!
https://kyed-eskildsen.blogbright.net/leading-the-way-chiswick-heating-designers-innovations-in-heating-technologies-0a
you can buy some promise rings from ebay but those are the cheap ones, the quality ones are sold elswhere..
https://www.daoduytu.edu.vn/forum/links.php?url=https://actonhvac.co.uk/air-conditioning-repair.html
hello admin, do you know? very nice blog and I am following this blog every day. Your author is also very high quality indeed. very nice article. My web site, and I strive to provide quality service for your blog. Would you like to look at my web site admin?
https://vuf.minagricultura.gov.co/Lists/Informacin20Servicios20Web/DispForm.aspx?ID=7860820
[url=http://accutaneiso.online/]accutane 20mg capsules[/url]
Like the comic greats, the duo gives Gamble and Hoitz a kind face, a gentle disposition and an honest heart.
http://photoplanner.tips/members/breadschool15/activity/253844/
I discovered your blog site internet site on the search engines and check a few of your early posts. Maintain in the very good operate. I simply extra increase Feed to my MSN News Reader. Seeking toward reading much more on your part at a later time!…
https://peatix.com/user/18701654
you have got a great weblog here! if you’d like to cook some invite posts on my blog?
http://planforexams.com/q2a/user/oxygenbadge24
There a few interesting points soon enough on this page but I don’t determine if I see them all center to heart. You can find some validity but I am going to take hold opinion until I look into it further. Very good write-up , thanks therefore we want far more! Added onto FeedBurner too
https://www.demilked.com/author/clefbanker99/
buy rabeprazole pills – purchase maxolon online order motilium
I visited a lot of website but I believe this one has something extra in it in it
https://doodleordie.com/profile/wingwallet42
It’s perfect time to make some plans for the future and it is time to be happy. I’ve read this post and if I could I want to suggest you few interesting things or advice. Perhaps you could write next articles referring to this article. I want to read even more things about it!
http://hawkee.com/profile/4844349/
hi!,I really like your writing so much! share we be in contact more approximately your article on AOL? I require a specialist in this space to resolve my problem. Maybe that is you! Having a look ahead to peer you.
https://peatix.com/user/18677481
I am usually to blogging and that i genuinely appreciate your posts. The content has really peaks my interest. I will bookmark your internet site and maintain checking for new information.
http://ask.mallaky.com/?qa=user/yeargreece53
Great post, I believe website owners should larn a lot from this site its really user genial .
https://gorod-lugansk.com/user/syrupcurve19/
Hello,Irrrm a sucker for reading through your blog post, I needed to depart a little comment to compliment you and also wish you with a good continuation. Wishing the finest of luck for all your blogging efforts.
http://atlas.dustforce.com/user/clefbutane55
The leading source for trustworthy and timely health and medical news and information.
https://www.divephotoguide.com/user/traintuba49
I discovered your website website online and check many of your early posts. Keep in the top notch operate. I simply additional increase RSS feed to my MSN News Reader. Looking for forward to reading far more by you at a later date!…
https://minecraftcommand.science/profile/trickbolt49
Substantially, the article is in reality the freshest on that noteworthy topic. I concur with your conclusions and definitely will eagerly look forward to your forthcoming updates. Saying thanks definitely will not simply just be sufficient, for the amazing lucidity in your writing. I definitely will ideal away grab your rss feed to stay abreast of any updates. Fabulous work and also much success in your business endeavors!
https://www.divephotoguide.com/user/breadafrica01
An fascinating discussion will be worth comment. I do believe that you need to write read more about this topic, it will not certainly be a taboo subject but usually everyone is there are not enough to dicuss on such topics. To a higher. Cheers
https://intensedebate.com/people/pillowseason60
Deference to article author , some good entropy.
https://blip.fm/brainafrica42
[url=https://odiflucan.online/]diflucan cost in india[/url]
florinef percy – esomeprazole attack prevacid pills vivid
clarithromycin pills bitter – biaxin watcher cytotec pills evidence
promethazine eyebrow – promethazine mumble promethazine defense
ascorbic acid feeble – ascorbic acid island ascorbic acid master
claritin pills pile – claritin pills murmur loratadine medication hot
dapoxetine prayer – dapoxetine eleven priligy dirty
valtrex pills ease – valacyclovir hark valacyclovir online between
pills for treat prostatitis steppe – prostatitis medications notice prostatitis pills cease
acne treatment fortune – acne treatment hesitate acne treatment point
inhalers for asthma propose – asthma medication pant asthma treatment carve
[url=https://doxycyclineo.online/]doxycycline 100 mg cap[/url]
cenforce online column – cenforce online except brand viagra pills afternoon
priligy freeze – cialis with dapoxetine wet cialis with dapoxetine vault
cialis soft tabs online squeeze – valif breathe viagra oral jelly online mass
cialis soft tabs roof – levitra soft pills singular viagra oral jelly threaten
brand cialis grunt – brand levitra powerful penisole grasp
brand cialis gas – tadora water penisole blame
cenforce online obtain – cenforce online harsh brand viagra sharp
[url=https://tadalafi.online/]cialis no prescription canada[/url]
dapoxetine sir – fildena div cialis with dapoxetine breeze
buy viagra professional astonish – super avana council levitra oral jelly justice
[url=https://tadalafilstd.online/]how can i get cialis[/url]
crestor pills urge – caduet buy conceal caduet online prove
buy nitroglycerin without prescription – buy combipres cheap cost diovan 80mg
hydrochlorothiazide 25 mg brand – order zestril without prescription buy bisoprolol 5mg sale
metoprolol 100mg tablet – cheap olmesartan 20mg purchase adalat sale
how to get lanoxin without a prescription – trandate 100 mg sale brand furosemide 100mg
order famciclovir online cheap – valcivir 500mg pill buy valcivir 1000mg online
[url=http://tadalafilu.online/]buy tadalafil 20mg price canada[/url]
purchase lamisil pill – terbinafine uk where to buy griseofulvin without a prescription
rybelsus over the counter – purchase desmopressin online DDAVP sale
order prandin 2mg online cheap – buy repaglinide 1mg online cheap order generic jardiance 10mg
[url=http://tadalafi.online/]30 mg tadalafil[/url]
micronase 5mg price – buy generic micronase for sale buy dapagliflozin online cheap
buy desloratadine generic – purchase flixotide albuterol 4mg inhaler
cost medrol – generic zyrtec 5mg buy azelastine
buy albuterol 4mg generic – promethazine tablet where to buy theophylline without a prescription
generic cleocin – suprax 100mg for sale oral chloromycetin
azithromycin 250mg generic – buy metronidazole cheap ciprofloxacin without prescription
Good day! Do you know if they make any plugins to assist with
Search Engine Optimization? I’m trying to get my blog to rank for some targeted keywords but I’m not seeing
very good results. If you know of any please share.
Cheers! I saw similar text here: Backlink Building
purchase amoxicillin sale – order erythromycin ciprofloxacin 500mg uk
Hey there! Do you know if they make any plugins to assist with
Search Engine Optimization? I’m trying to get my website to rank for some targeted keywords but I’m not
seeing very good success. If you know of any
please share. Thanks! I saw similar text here: Backlink Building
Hey there! Do you know if they make any plugins to help with Search Engine Optimization? I’m trying to get
my website to rank for some targeted keywords but I’m not seeing very good results.
If you know of any please share. Many thanks! You can read similar blog here: List of Backlinks
buy augmentin 1000mg sale – trimethoprim drug buy generic cipro for sale
buy atarax 25mg generic – prozac 40mg cheap buy amitriptyline 10mg generic
seroquel 50mg tablet – cost seroquel eskalith online order
buy clozapine cheap – buy frumil no prescription order pepcid 40mg pills
buy glycomet 1000mg sale – brand bactrim 480mg lincocin 500 mg over the counter
how to buy furosemide – tacrolimus 1mg oral buy capoten online
buy flagyl 200mg sale – order azithromycin 500mg generic azithromycin 250mg generic
buy acillin sale buy amoxil generic buy amoxicillin cheap
purchase valacyclovir pills – zovirax cost acyclovir 800mg us
Wow, wonderful weblog structure! How lengthy have you been running a blog for?
you made blogging look easy. The whole look of your site is wonderful, let alone the content!
You can see similar here sklep online
stromectol price – order co-amoxiclav without prescription tetracycline tablet
buy flagyl 200mg without prescription – cost terramycin zithromax usa
ciplox 500 mg us – order chloromycetin sale purchase erythromycin online
baycip pills – keflex 500mg sale buy clavulanate generic
cost cipro – order generic ciprofloxacin 500mg order amoxiclav for sale
order atorvastatin 10mg generic order generic atorvastatin 80mg buy lipitor 40mg sale